
【题目】某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2 . 已知该反应中H2O2只发生如下过程:H2O2﹣→O2 .
(1)该反应中的还原剂是 .
(2)该反应中,发生还原反应的过程是→ .
(3)写出该反应的化学方程式,并用单线桥法标出电子转移的方向和数目 .
(4)如反应转移了0.3mol电子,则产生的气体在标准状况下体积为 .
【答案】
(1)H2O2
(2)H2CrO4;Cr(OH)3
(3)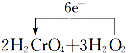 =2Cr(OH)3↓+3O2↑+2H2O
=2Cr(OH)3↓+3O2↑+2H2O
(4)3.36 L
【解析】解:(1)由信息H2O2﹣→O2中可知,O元素的化合价由﹣1价升高到0,则H2O2为还原剂,故答案为:H2O2;(2)氧化剂发生还原反应,含元素化合价降低的物质为氧化剂,则Cr元素的化合价降低,即还原反应的过程为H2CrO4→Cr(OH)3 , 故答案为:H2CrO4;Cr(OH)3;(3)该反应中O元素失电子,Cr元素得到电子,2molH2CrO4反应转移电子为2mol×(6﹣3)=6mol,则用单线桥法标出电子转移的方向和数目为 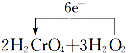 =2Cr(OH)3↓+3O2↑+2H2O,故答案为:
=2Cr(OH)3↓+3O2↑+2H2O,故答案为: 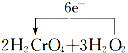 =2Cr(OH)3↓+3O2↑+2H2O;(4)由2H2CrO4+3H2O2═2Cr(OH)3↓+3O2↑+2H2O可知,生成3mol气体转移6mol电子,则转移了0.3mol电子,则产生的气体的物质的量为
=2Cr(OH)3↓+3O2↑+2H2O;(4)由2H2CrO4+3H2O2═2Cr(OH)3↓+3O2↑+2H2O可知,生成3mol气体转移6mol电子,则转移了0.3mol电子,则产生的气体的物质的量为 ![]() mol=0.15mol,其在标准状况下体积为0.15mol×22.4L/mol=3.36L,故答案为:3.36L. (1)由H2O2只发生如下过程H2O2﹣→O2可知,利用该过程中O元素的化合价由﹣1价升高到0来分析;(2)氧化剂发生还原反应,利用元素的化合价降低来分析;(3)由失去电子的元素指向得到电子的元素,并标出电子转移的总数来用单线桥法标出电子转移的方向和数目;(4)由反应可知生成3mol气体转移6mol电子,以此来计算.
mol=0.15mol,其在标准状况下体积为0.15mol×22.4L/mol=3.36L,故答案为:3.36L. (1)由H2O2只发生如下过程H2O2﹣→O2可知,利用该过程中O元素的化合价由﹣1价升高到0来分析;(2)氧化剂发生还原反应,利用元素的化合价降低来分析;(3)由失去电子的元素指向得到电子的元素,并标出电子转移的总数来用单线桥法标出电子转移的方向和数目;(4)由反应可知生成3mol气体转移6mol电子,以此来计算.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】【化学选修3:物质结构与性质】A﹣I为原子序数递增的前4周期的元素,已知A原子的最外层电子是次外层电子数的2倍,D为周期表中电负性最大的元素,F与C位于同一主族,E与G在周期表的位置是上下相连,两元素所在主族中所有元素都是金属,H为应用最广泛的金属;I处于周期表中的第二副族.请回答下列问题:(以下问题中的所有原子都必须在上述元素中寻找)
(1)B单质分子中σ与π键数目比为;B、C、D第一电离能由小到大的顺序为;(填写元素符号)
(2)H元素原子的价层电子排布式为 , H3+离子可以与上述元素中的三种形成的某阴离子生成血红色络合物;该阴离子又与A﹣I元素中的某些原子形成的分子互为等电子体,这种分子的化学式为(写一种即可),该阴离子空间构型为;
(3)D与G可以形成如图的晶胞,则黑点表示的是元素(填写元素符号),该元素原子在该晶胞中的配位数为;
(4)若将上述晶胞圆圈对应的原子所在上下两层平面原子,按两条相互垂直的对角线上各去掉该原子2个(共去掉4个),并将小点和圆圈对应的元素更改为另外两种元素,则这个晶胞化学式为 , 若再将留下的所有原子换成另外一种新元素的原子,则成为另外一种晶胞,该晶胞中成键原子键角为;
(5)已知,F单质晶体的原子堆积为ABAB型,那么,该晶体的空间利用率为如果F单质的摩尔质量为M,晶胞棱长为a,晶胞高度为c则,该晶体密度表达式为(阿伏加德罗常数用NA表示,不化简)如果F的原子半径为R,用R表示的晶胞高度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将20.0g质量分数为14.0%的KNO3溶液跟30.0g质量分数为24.0%的KNO3溶液混合,得到的密度为1.15g·cm-3的混合溶液。计算:
(1)混合后溶液的质量分数___________。
(2)混合后溶液的物质的量浓度_____________。
(3)在1000g水中需溶解_____________摩尔KNO3才能使其浓度恰好与上述混合后溶液的浓度相等?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家在研究金属矿物质组分的过程中,发现了Cu﹣Ni﹣Fe等多种金属互化物.
(1)鉴别某种金属互化物是晶体还是非晶体的方法是 .
(2)已知高温下Cu2O比CuO更稳定,试从铜原子核外电子变化角度解释其原因 .
(3)镍能与类卤素(SCN)2反应生成Ni(SCN)2 . (SCN)2分子中硫原子的杂化方式是 , σ键和π键数目之比为;类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H﹣S﹣C≡N)的沸点低于异硫氰酸(H﹣N═C═S)的沸点,其原因是 .
(4)立方FeO晶体的结构如图1所示,设晶胞边长为a cm,密度为b gcm﹣3 , 则阿伏加德罗常数可表示为(用含a、b的式子表示).人工制备的FeO晶体常存在缺陷(如图2),已知某氧化物样品组成为Fe0.96O,该晶体中Fe3+与Fe2+的离子个数之比为 . 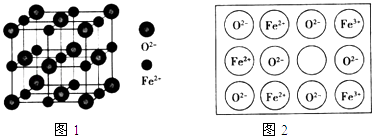
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾在不同的条件下发生的反应如下:MnO ![]() +5e﹣+8H+═Mn2++4H2O ①
+5e﹣+8H+═Mn2++4H2O ①
MnO ![]() +3e﹣+2H2O═MnO2↓+4OH﹣②
+3e﹣+2H2O═MnO2↓+4OH﹣②
MnO ![]() +e﹣═MnO42﹣(溶液绿色)③
+e﹣═MnO42﹣(溶液绿色)③
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的影响.
(2)将SO2通入高锰酸钾溶液中,发生还原反应的离子反应过程为→ .
(3)将PbO2投入到酸性MnSO4溶液中搅拌,溶液变为紫红色.下列说法正确的是a.氧化性:PbO2>KMnO4
b.还原性:PbO2>KMnO4
c.该反应可以用盐酸酸化
(4)将高锰酸钾逐滴加入到硫化钾溶液中发生如下反应,其中K2SO4和S的物质的量之比为3:2,完成下列化学方程式(横线上填系数,括号内填物质):①KMnO4+K2S+═K2MnO4+K2SO4+S↓+ .
②若生成6.4g单质硫,反应过程中转移电子的物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属材料在日常生活以及生产中有着广泛的运用。下列关于金属的一些说法不正确的是( )
A. 合金的性质与其成分金属的性质不完全相同
B. 工业上金属Mg、Al都是用电解熔融的氯化物制得的
C. 金属冶炼的本质是金属阳离子得到电子变成金属原子
D. 越活泼的金属越难冶炼
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是元素周期表的一部分,根据给定的元素回答下列问题
(1)K的元素符号是;
(2)D元素的外围电子排布图是 , 在其化合物中,最高正价是;
(3)C元素的原子结构示意图是;
(4)A与L、B与L都分别能形成原子个数比为1:1的化合物,A与L(1:1)的化合物是分子(填极性或非极性),B与L(1:1)的化合物的电子式是;
(5)G、H、L原子的第一电离能由高到低的顺序是(填元素符号);
(6)J单质的一种白色同分异构体的空间构型是;
(7)E元素在元素周期表中的位置是 , 在其化合物中,常有+2、+3价的2种离子,+3的离子比较稳定,其原因是;
(8)A与B的化合物的熔点比A与L的化合物的熔点高,其原因是;
(9)A的单质与L的单质与B的最高价氧化物的水化物溶液能组成燃烧电池,写出该种电池的负极的电极反应式;
(10)F元素的最高价氧化物与M元素的最高价氧化物的水化物反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验误差分析错误的是( )
A.滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
B.用容量瓶配置溶液,定容时俯视刻度线,所配溶液浓度偏小
C.用湿润的pH试纸测稀碱液的pH,测定值偏小
D.测定中和反应反的应热时,将碱液缓慢倒入酸中,所测温度值偏小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com