
【题目】A、B、C、D、E、F、G、H八种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B、C、D为同一周期,A与E,B与G,D与H分别为同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5个,D的最外层电子数是F的2倍,C和D的最外层电子数之和为11。请回答下列问題:
(1)以上八种元素中非金厲所形成的最简单气态氢化物稳定性最弱的是_________(填化学式),E、F、H 所形成的简单离子的半径由大到小的顺序为_________(用离子符号表示)
(2)一定条件下,A的单质气体与C的单质气体充分反应生成W气体,W的结构式_____。由A、D两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为_____。固体化合物E2D2与化合物E2H的水溶液按物质的量比1:1反应生成单质H的离子方程式为________________。
(3)G是非金厲元素,其单质在电子工业中有重要应用,请写出G的最髙价氧化物与B的单貭在高温下发生置换反应的化学反应方程式____________________。
(4)10L的密闭容器中,通入2mol的HD2气体和1molD2的气体单质,一定条件下反应后生成HD3气体,当反应达到平衡时,单质D的浓度为0.01mol·L-1,同时放出约177KJ的热量,则平衡时HD2的转化率为____________;该反应的热化学方程式____________。
【答案】(1)SiH4;S2-Na+>Al3+
(2)![]() :
:![]() ;Na2O2+2H2O+S2-=S↓+2Na++4OH-
;Na2O2+2H2O+S2-=S↓+2Na++4OH-
(3)SiO2+2C![]() Si+2CO↑
Si+2CO↑
(4)90%;2SO2(g)+O2(g)![]() 2SO3(g); △H=-196.7kJ·mol-1
2SO3(g); △H=-196.7kJ·mol-1
【解析】试题分析:A、B、C、D、E、F、G、H八种元素分布在三个不同的短周期,它们的原子序数依次增大,则A为氢元素;A与E同一主族,E原子序数比A至少大4,可推知E为Na;B、C、D为同一周期,应处于第二周期,E、F、G、H都处于第三周期,令F的最外层电子数为x,其质子数为10+x,则D原子最外层电子数为2x,质子数为2+2x,由于F的质子数比D多5,则有:10+x-(2-2x)=5,解得x=3,故F为Al、D为O,C、D、F三种元素的原子序数之和为28,则C的原子序数=28-8-13=7,故C为N;D与H分别为同主族,则H为S;B与G同主族,结合原子序数可知,处于ⅣA族,故B为C、G为Si。
(1)以上八种元素中的非金属中Si的非金属性最弱,其形成的最简单气态氢化物SiH4稳定性最弱;电子层结构相同核电荷数越大离子半径越小,电子层越多离子半径越大,故离子半径S2->Na+>Al3+;
(2)一定条件下,氢气与氮气充分反应可生成气体W为NH3,其结构式为![]() ;由H、O两元素可以组成X、Y两种化合物,X在一定条件下可以分解生成Y,则X为H2O2、Y为H2O,H2O2分子中O原子之间形成1对共用电子对,H原子与O原子之间形成1对共用电子对,其电子式:
;由H、O两元素可以组成X、Y两种化合物,X在一定条件下可以分解生成Y,则X为H2O2、Y为H2O,H2O2分子中O原子之间形成1对共用电子对,H原子与O原子之间形成1对共用电子对,其电子式:![]() ;固体化合物Na2O2与化合物Na2S的水溶液按物质的量之比1:1反应生成单质S,同时生成NaOH,该反应的离子方程式为Na3O2+2H2O+S2-=S↓+2Na++4OH-;
;固体化合物Na2O2与化合物Na2S的水溶液按物质的量之比1:1反应生成单质S,同时生成NaOH,该反应的离子方程式为Na3O2+2H2O+S2-=S↓+2Na++4OH-;
(3)二氧化硅与碳在高温下反应生成CO与Si,化学反应方程式为:SiO2+2C![]() 2CO↑+Si;
2CO↑+Si;
(4)在10L的密闭容器中,通入2mol SO2气体和1mol O2气体,一定温度下反应后生成SO3气体,当反应达到平衡时,O2的浓度为0.01molL-1,则:
2SO2(g)+O2(g)![]() 2SO3(g)
2SO3(g)
开始(mol/L):0.2 0.1 0
变化(mol/L):0.18 0.09 0.18
平衡(mol/L):0.02 0.01 0.18
故平衡时SO2的转化率为![]() ×100%=90%;
×100%=90%;
参加反应二氧化硫的物质的量![]() =196.7kJ,该反应的热化学方程式为:2SO2(g)+O2(g)
=196.7kJ,该反应的热化学方程式为:2SO2(g)+O2(g)![]() 2SO3(g)△H=-196.7kJ/mol。
2SO3(g)△H=-196.7kJ/mol。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列各组中的反应,属于同一反应类型的是
A.由溴丙烷水解制丙醇;由丙烯与水反应制丙醇
B.由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸
C.由氯代环己烷消去制环己烯;由丙烯加溴制![]() 二溴丙烷
二溴丙烷
D.由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从含铜废料(如:覆铜板、印刷线路板及铅冰铜等)中提取铜,既可提高资源的利用率又可减少重金属污染。
(1)废覆铜板(Cu和Sn组成)可用CuSO4和H2SO4混合溶液作电解质溶液,直接电解回收精铜,阳极上发生的电极反应为 。
(2)废印刷线路板中的铜常用含盐酸的FeCl3溶液或H2O2-HCl- NaCl混合溶液浸取回收。
①用FeCl3溶液浸取铜时发生反应的离子方程式为 ;若加盐酸不足,反应一段时间后线路板表面有红褐色沉淀,产生红褐色沉淀的原因是 。
②将粉碎后的废印刷线路板放入三口烧瓶中,分别加入由0.3mol·L-1盐酸、0.5mol·L-1NaCl及不同浓度的H2O2组成的混合溶液,在温度、搅拌速率及固液比等均相同时,铜的浸取率随H2O2的浓度和时间的变化如图-1所示。当c(H2O2)= 0 mol·L-1时,也有少量的铜被浸出,其原因是 。
③用H2O2-HCl- NaCl混合溶液浸取时,其浸取过程包括:
(Ⅰ)Cu+H2O2+2H+=Cu2++2H2O
(Ⅱ)Cu2++Cu![]() 2Cu+
2Cu+
(Ⅲ)Cu++nCl-![]() CuCln(n-1)-
CuCln(n-1)-
(Ⅳ)2CuCln(n-1)-+2H++H2O2=2Cu2++2H2O+2nCl-
其他条件相同时,增大下列离子浓度可以加速Cu从废电路板中浸出的是 (填序号)。
a.Na+ b.Cu2+ c.Cl- d.OH-

(3)铅冰铜(PbS、Cu2S及FeS的混合物)可用HCl-H2O2混合溶液浸取。
①Cu2S被HCl-H2O2混合溶液浸取得到硫酸铜和氯化铜溶液的化学方程式为 。
②若由H2SO4代替HCl-H2O2中的HCl,其他条件相同,铜的浸取率随硫酸浓度的变化如图-2所示。当H2SO4浓度大于3.1mol·L-1时,硫酸浓度越大,铜的浸取率反而越小,其原因可能是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是病人输液用的葡萄糖(分子式为C6H12O6)注射液的标签上的部分内容。据标签所提供的信息,以下说法错误的是 ( )

A. 该注射液中葡萄糖的质量分数是5%
B. 葡萄糖的摩尔质量为180g·mol-1
C. 该注射液的密度约为1g·mL-1
D. 该注射液中葡萄糖的物质的量浓度约为0.014 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有些化学反应反应速率很慢且副反应较多,测定这些反应的焓变可运用( )
A. 盖斯定律 B. 勒夏特列原理
C. 阿伏加德罗定律 D. 质量守恒定律
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A.高温下,0.2mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA
B.室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C.氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA
D.5NH4NO3 ![]() 2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75 NA
2HNO3+4N2↑+9H2O反应中,生成28gN2时,转移的电子数目为3.75 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知1 mol白磷完全转化为红磷放出29.2 kJ热量,下列两个反应:P4(白,s)+5O2(g)=2P2O5(s)ΔH=-Q1,4P(红,s)+5O2(g)=2P2O5(s)ΔH=-Q2,Q1与Q2的关系是
A.Q1=Q2 B.Q1<Q2 C.Q1>Q2 D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应∶2NO2![]() 2NO+O2在密闭容器中反应,达到平衡状态的标志是
2NO+O2在密闭容器中反应,达到平衡状态的标志是
①单位时间内生成n mol O2的同时生成2n mol NO2 ②单位时间内生成n mol O2 的同时,生成2n mol NO ③用NO2、NO、O2 的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态 ④混合气体的颜色不再改变的状态 ⑤混合气体的密度不再改变的状态 ⑥ 混合气体的平均相对分子质量不再改变的状态
A.①④⑥ B.②③⑤ C.①③④ D.①②③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,向一带活塞的密闭容器中充入2molA和1molB,发生下列反应:2A(g)+B(g)![]() 2C(g) △H< 0,达到平衡后,在t1时刻改变条件,化学反应速率随时间变化如图。下列对t1时刻改变条件的推测中正确的是
2C(g) △H< 0,达到平衡后,在t1时刻改变条件,化学反应速率随时间变化如图。下列对t1时刻改变条件的推测中正确的是
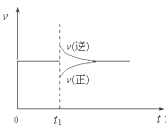
A、保持压强不变,升高反应温度
B、保持温度不变,增大容器体积
C、保持温度和容器体积不变,充入1molC(g)
D、保持温度和压强不变,充入1molC(g)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com