
【题目】金属镍在电池和电镀等工业上具有广泛的用途,可镍也具有很强的毒性,若不进行回收处理,将对环境造成很大的影响,以下是以电镀废渣为原料获得NiSO46H2O的过程,已知,废渣中除含金属镍外,主要含有:Cu、Zn、Fe、Mg等元素的化合物。
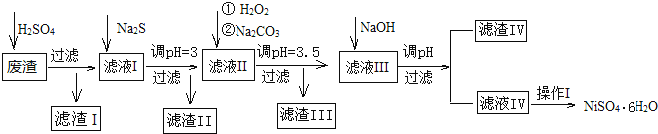
部分阳离子以氢氧化物或硫化物的形式完全沉淀时溶液的pH见表.
沉淀物 | Fe(OH)3 | Fe(OH)2 | CuS | ZnS | FeS | NiS | Al(OH)3 | Mg(OH)2 | Ni(OH)2 |
pH | 3.2 | 9.7 | ≥-0.42 | ≥2.5 | ≥7 | ≥7.5 | ≥5 | ≥8 | ≥8.5 |
(1)往废渣中加H2SO4酸浸,提高酸浸效率的方法有__(至少写出2点)。
(2)加Na2S同时调溶液的pH为3,目的是除去铜、锌等杂质,则往滤液Ⅱ中加入H2O2的反应的离子方程式为___。
(3)操作Ⅰ包括以下过程:__、__、过滤、洗涤、干燥.该洗涤过程不能用水洗涤,应该用__洗涤,目的是___。干燥有低温干燥和高温干燥,能否用高温干燥___,理由是____。
(4)滤液Ⅲ中加入NaOH溶液的目的是调节溶液的pH为8以除去Al3+以及少量的Mg2+,若向含有Mg2+、Al3+的溶液中滴加NaOH溶液,常温下当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Al3+)=__。{已知:25℃时,Ksp[Mg(OH)2]=5.0×10-14;Ksp[Al(OH)3]=2.0×10-33}。
【答案】搅拌、升温、适当增加硫酸浓度、废渣粉碎等 2Fe2++H2O2+2H+=2Fe3++2H2O 冷却 结晶 酒精 既能洗涤沉淀表面残余的溶液又有利晶体的干燥并减少NiSO4﹒6H2O晶体的损失 否 温度过高会使NiSO4﹒6H2O晶体失去部分或全部结晶水 2.5×1013
【解析】
根据流程图:废渣(除含镍外,还含有Cu、Zn、Fe、Mg等元素的化合物杂质),在硫酸溶解后过滤,除去不溶于硫酸的杂质铜等,滤液含有二价铁离子、铜离子、锌离子、镁离子等杂质,加入硫化钠调节pH=3,根据表格信息可除去铜离子、锌离子,然后加H2O2是将二价铁氧化成三价铁,再通过调节pH值3.5使三价铁以氢氧化物的沉淀而除去,滤液Ⅲ加入NaOH溶液的目的是调节溶液的pH为8以除去Al3+以及少量的Mg2+,滤液Ⅳ含有可溶性硫酸盐,为Na2SO4、NiSO4,经冷却结晶、过滤、洗涤,干燥得NiSO4﹒6H2O。
(1)根据影响反应速率的因素,搅拌、升温、适当增加硫酸浓度、废渣粉碎等,都可加快反应速率,所以提高酸浸效率的方法有:搅拌、升温、适当增加硫酸浓度、废渣粉碎等;
(2)滤液Ⅱ中加入H2O2的目的是将二价铁氧化成三价铁,再通过调节pH值3.5使三价铁以氢氧化物的沉淀而除去,反应的离子方程式是2Fe2++H2O2+2H+=2Fe3++2H2O;
(3)从溶液中得到晶体,可经过溶解、蒸发浓缩、冷却结晶、过滤、洗涤等操作,NiSO4﹒6H2O晶体易溶于水,洗涤过程不能用水洗涤,应用酒精洗涤,既能洗涤沉淀表面残余的溶液又有利晶体的干燥并减少NiSO4﹒6H2O晶体的损失;干燥应低温干燥,因温度过高会使NiSO4﹒6H2O晶体失去部分或全部结晶水。
(4)当两种沉淀共存且溶液的pH=8时,c(H+)=10-8mol/L, c(OH-)=10-6mol/L,根据25℃时,Ksp[Mg(OH)2]=c(Mg2+)×c2(OH-)=5.0×10-14,可计算出c(Mg2+)=![]() =5.0×10-2mol/L;Ksp[Al(OH)3]=c(Al3+)×c3(OH-)=2.0×10-33,可计算出c(Al3+)=
=5.0×10-2mol/L;Ksp[Al(OH)3]=c(Al3+)×c3(OH-)=2.0×10-33,可计算出c(Al3+)=![]() =2.0×10-15mol/L,所以c(Mg2+):c(Al3+)=2.5×1013。
=2.0×10-15mol/L,所以c(Mg2+):c(Al3+)=2.5×1013。


 名校通行证有效作业系列答案
名校通行证有效作业系列答案科目:高中化学 来源: 题型:
【题目】利用下图装置(夹持装置略)制取和收集纯净、干燥的氨气,并探究氨气的性质。
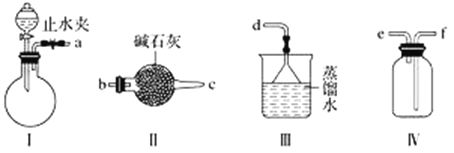
(1)关闭装置Ⅰ中的止水夹,向分液漏斗中加适量水,打开活塞,说明Ⅰ气密性良好的现象是______________________。
(2)利用装置Ⅰ制取氨气,不能选用的试剂为浓氨水和________(填字母)。
A.氢氧化钠 B.碱石灰 C.硝酸钾 D.生石灰
(3)根据实验要求,仪器连接的顺序(用字母编号表示):a接________、________接________、______接______。______
(4)收集氨气,按如图装置进行NH3性质的探究实验。
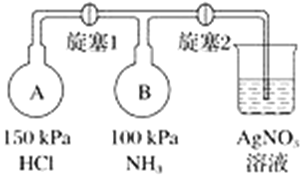
①打开旋塞1,B瓶中的现象是_________________________________________,原因是_____________________________________________,稳定后,关闭旋塞1;
②再打开旋塞2,B瓶中的现象是__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现用Na2SO4固体来配制480mL0.2mol·L-1的Na2SO4溶液。可供选择的仪器如图:
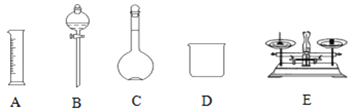
(1)如图所示的仪器中配制溶液不需要的是__ (填选项),配制上述溶液还需用到的玻璃仪器是___、__ (填仪器名称)。
(2)使用容量瓶之前必须进行的操作是___。(填选项)
A.检查气密性 B.检查是否漏水 C.烘干
(3)经计算,需Na2SO4的质量为___g。
(4)你选用的容量瓶规格为___mL。
(5)配制溶液时,一般可分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容
其操作顺序:②→__→__→__→__→__→__(填序号)。___
(6)在配制过程中,其他操作都准确,定容时俯视刻度线会使所配溶液浓度__(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在家中进行化学实验,按照图1连接好线路后发现灯泡不亮,按照图2连接好线路后发现灯泡亮,由此得出的结论正确的是
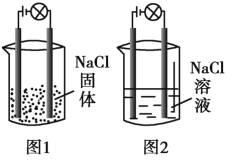
A. NaCl固体中没有离子
B. 图2中NaCl在电流的作用下电离出大量的离子
C. NaCl溶液中水电离出大量的离子
D. 图2工作时发生了氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第三代混合动力车,可以用电动机、内燃机或二者结合推动车轮。汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在下坡时,电池处于充电状态。
(1)混合动力车目前一般使用镍氢电池,该电池中镍的化合物为正极,储氢金属(以M表示)为负极,碱液(主要为KOH)为电解质溶液。镍氢电池充放电原理如图1所示,其总反应式为H2+2NiOOH![]() 2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH___ (填“增大”、“减小”或“不变”),该电极的电极反应式为___。
2Ni(OH)2。根据所给信息判断,混合动力车上坡或加速时,乙电极周围溶液的pH___ (填“增大”、“减小”或“不变”),该电极的电极反应式为___。
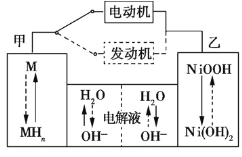
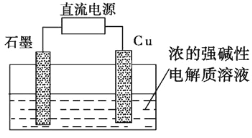
图1 图2
(2)Cu2O是一种半导体材料,可通过如图2所示的电解装置制取,电解总反应式为2Cu+H2O![]() Cu2O+H2↑,阴极的电极反应式是________。用镍氢电池作为电源进行电解,当电池中有1 mol H2被消耗时,Cu2O的理论产量为___g。
Cu2O+H2↑,阴极的电极反应式是________。用镍氢电池作为电源进行电解,当电池中有1 mol H2被消耗时,Cu2O的理论产量为___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

下列叙述不正确的是( )
A.试剂X可以是氢氧化钠溶液
B.反应①过滤后所得沉淀为氧化铁
C.图中所示转化反应包含氧化还原反应
D.反应②的化学方程式为2NaAlO2+3H2O+CO2=2Al(OH)3↓+Na2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某校化学实验兴趣小组为了验证在实验室制备Cl2的过程中有水蒸气和HCl挥发出来,同时证明Cl2的某些性质,甲同学设计了如图所示的实验装置(支撑用的铁架台省略),请按要求回答下列问题。
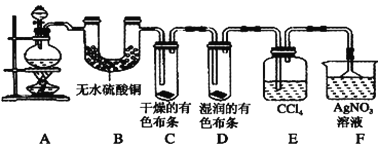
(1) 实验室制备Cl2所用的化学药品是________。
写出该反应的离子方程式,并用单线桥表示电子转移情况_____________________ ,此反应中每转移0.8mol电子,消耗Hcl____mol
(2)①装置B的作用是_______
②装置C和D出现的不同现象说明的问题是___
③装置E的作用是_______
(3)乙同学认为甲同学的实验有缺陷,不能确保最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液中的气体只有一种,乙同学提出应该在装置___与___之间(填装置字母序号)增加一个装置,所增加装置里面的试剂可以为___(填字母序号)。
A.湿润的碘化钾淀粉试纸 B.浓硫酸 C.湿润的红色布条 D.饱和食盐水
Ⅱ.洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂。
①工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为:_____________。
②漂白粉的有效成分是________________________。
③漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中错误的是( )
A. 在煤中添加石灰石作脱硫剂
B. 将废弃塑料热裂解处理,可获得乙烯、丙烯等化工原料
C. 用催化法处理汽车尾气中的CO和NO:CO+NO![]() C+NO2
C+NO2
D. 利用二氧化碳等原料合成聚碳酸酯类可降解塑料代替聚乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大量资金。请回答钢铁腐蚀与防护过程中的有关问题。
(1)钢铁的电化学腐蚀原理如图所示:

①写出石墨电极的电极反应式______;
②将该装置作简单修改即可成为钢铁电化学防护的装置,请在如图虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向。______
③写出修改后石墨电极的电极反应式______。
(2)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式_____。
(3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图:

①A电极对应的金属是__(写元素名称),B电极的电极反应式是____。
②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为___ mol。
③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com