
【题目】常温下,CH3COOH和NH3·H2O的电离常数均为1.8×10-5mol·L-1。向20mL浓度均为0.1mol·L-1 NaOH和NH3·H2O的混合液中滴加等物质的量浓度的CH3COOH溶液,所得混合液的电导率与加入CH3COOH溶液的体积(V)关系如图所示。下列说法错误的是

A. M点:c(Na+)>c(CH3COO-)>c(NH3·H2O)>c(NH4+)
B. 溶液呈中性的点处于N、P之间
C. 已知1g3≈0.5,P点的pH=5
D. P点:3[c(CH3 COO-)+ c(CH3COOH)]=2[ c(Na+)+c(NH4+)+c(NH3·H2O)]
【答案】D
【解析】
溶液中离子浓度越大,溶液的电导率越大,向混合溶液中加入等物质的量浓度的CH3COOH溶液时,发生反应的先后顺序是NaOH+CH3COOH→CH3COONa+H2O、NH3H2O+CH3COOH→CH3COONH4 +H2O,体积在0-20时,溶液的电导率减小,M点最小,因为溶液体积增大导致M点离子浓度减小,M点溶液中溶质为CH3COONa、NH3H2O,继续加入醋酸溶液,NH3H2O是弱电解质,生成的CH3COONH4是强电解质,导致溶液中离子浓度增大,溶液的电导率增大,N点时醋酸和一水合氨恰好完全反应生成醋酸铵,N点溶液中溶质为CH3COONa、CH3COONH4,且二者的物质的量相等,电导率达到最大,继续加入醋酸,溶液的体积增大,离子的浓度减小,电导率逐渐减小,据此分析解答。
A.M点溶液中溶质为等物质的量浓度的CH3COONa、NH3H2O,CH3COONa水解,NH3H2O电离,但CH3COONa水解程度小于NH3H2O电离程度,c(Na+)>c(CH3COO-)>c(NH3·H2O)>c(NH4+),故A正确
B.体积为20时NaOH和醋酸恰好完全反应、体积为40时醋酸和一水合氨恰好完全反应;醋酸钠溶液呈碱性、醋酸铵溶液呈中性,要使混合溶液呈中性,应该使醋酸稍微过量,所以要使溶液呈中性,加入醋酸的体积应该大于40mL,应该在N、P之间,故B正确;
C.加入醋酸60mL时,溶液中的溶质为CH3COONa、CH3COONH4、CH3COOH,且三者的物质的量浓度相等,该溶液为缓冲溶液,溶液的pH=pKa-lg![]() =-lg1.8×10-5-lg
=-lg1.8×10-5-lg![]() =6-lg9=6-2lg3≈5,故C正确;
=6-lg9=6-2lg3≈5,故C正确;
D.加入醋酸60mL时,溶液中的溶质为CH3COONa、CH3COONH4、CH3COOH,且三者的物质的量浓度相等,根据物料守恒,c(CH3COO-)+ c(CH3COOH)= c(Na+)+c(NH4+)+ c(NH3·H2O)+ c(Na+)=2c(Na+)+c(NH4+)+c(NH3·H2O),故D错误;
答案选D。


 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
【题目】工业废水中含有的![]() 和CrO42-会对水体产生很大的危害,这种工业废水必须净化处理。一种处理含铬废水的工艺流程如下:
和CrO42-会对水体产生很大的危害,这种工业废水必须净化处理。一种处理含铬废水的工艺流程如下:
![]()
下列说法不正确的是
A. ①中,酸化后发生反应为![]()
B. ②中,反应的氧化剂与还原剂的物质的量之比为3∶1
C. ③中,所得沉淀Cr(OH)3中含有Fe(OH)3
D. ③中调pH所用物质可以是NH3或Fe2O3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某种微生物燃料电池工作原理如图所示。下列有关该电池的说法中,正确的是
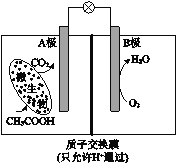
A.外电路电子从B极移向A极
B.溶液中H+由B极区移向A极区
C.电池工作一段时间后B极区溶液的pH减小
D.A极电极反应式为:CH3COOH - 8e-+2H2O=2CO2 +8H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积恒为0.5 L的密闭容器中,一定量的氮气和氢气进行如下化学反应:N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,其化学平衡常数K与t的关系如下表:
2NH3(g) ΔH<0,其化学平衡常数K与t的关系如下表:
t/℃ | 200 | 300 | 400 |
K | K1 | K2 | 0.5(mol·L-1)-2 |
请完成下列问题:
(1)试比较K1、K2的大小,K1________K2(填“>”、“=”或“<”)。
(2)下列各项能做为判断该反应达到化学平衡状态的依据的是_____(填字母序号)。
a.容器内N2、H2、NH3的浓度之比为1∶3∶2
b.v正(N2)=3v逆(H2)
c.容器内压强保持不变
d.混合气体的密度保持不变
(3)400 ℃时,反应2NH3(g)![]() N2(g)+3H2(g)的平衡常数K为____。当测得NH3、H2、N2的物质的量分别为3 mol、1 mol、2 mol时,则该反应的v正(N2)___ v逆(N2)(填“>”、“=”或“<”)。
N2(g)+3H2(g)的平衡常数K为____。当测得NH3、H2、N2的物质的量分别为3 mol、1 mol、2 mol时,则该反应的v正(N2)___ v逆(N2)(填“>”、“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】N2O5是一种新型硝化剂,其性质和制备受到人们的关注。一定温度下,在2 L固定容积的密闭容器中发生反应:2N2O5(g)![]() 4NO2(g)+O2(g) ΔH>0。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示。下列说法中不正确
4NO2(g)+O2(g) ΔH>0。反应物和部分生成物的物质的量随反应时间变化的曲线如图所示。下列说法中不正确

A. 曲线a表示NO2的物质的量随时间的变化
B. 10 s时,v(正)>v(逆)
C. 20 s时反应达到平衡
D. 0~20 s内平均反应速率 v(O2)=0.05 mol·L-1·s-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】太阳能的开发利用在新能源研究中占据重要地位,单晶硅太阳能电池片在加工时,一般掺杂微量的铜、钴、硼、镓、硒等。回答下列问题:
(1)基态二价铜离子的电子排布式为______,已知高温下Cu2O比CuO更稳定,试从核外电子排布角度解释______。
(2)铜的某种氧化物晶胞如图,该晶胞中阴离子的个数为___________。

(3)铜与(SCN)2反应生成Cu(SCN)2,1 mol(SCN)2中含有π键的数目为___________,HSCN结构有两种,硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N=C=S)的原因是___________。
(4)BF3能与NH3反应生成BF3·NH3。B与N之间形成配位键,氮原子提供_____,在BF3·NH3中B原子的杂化方式为_______。
(5)Co的一种氧化物CoO2晶体的层状结构如图所示(小球表示Co原子,大球表示O原子)。下列用粗线画出的重复结构单元不能描述CoO2的化学组成是(填字母代号)。________

(6)六方氮化硼晶体结构与石墨晶体相似,层间相互作用力为___________。六方氮化硼在高温高压下,可以转化为立方氮化硼,其结构、硬度与金刚石相似,其晶胞如图,晶胞边长为361.5pm,立方氮化硼的密度是___________g·cm-3(只列算式,NA为阿伏加德罗常数的值)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏伽德罗常数的数值,下列说法中正确的是
①0.5mol O3与11.2L O2所含的分子数一定相等
②标准状况下,28g CO与N2的混合气体的体积约为22.4L
③通常状况下,NA个CO2分子占有的体积为22.4L
④常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
⑤常温下,4.4g的CO2和N2O(不反应)混合物中所含有的电子数为2.2NA
⑥标准状况下,22.4LH2O含有的分子数为NA
⑦在常温常压下,1molO2含有的原子数为2NA
A.①②③⑦B.②④⑤⑦C.①③⑤⑦D.②③④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国具有丰富的铜矿资源,请回答下列有关铜及其化合物的问题:
(1)请写出基态Cu原子的价电子排布式_________。焰火中的绿色是铜的焰色,基态铜原子在灼烧时价电子发生了_________ 而变为激发态。
(2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Il(Zn)______ Il(Cu)(填“大于”或“小于”),原因是___________。
(3)新型农药松脂酸铜具有低残留的特点,下图是松脂酸铜的结构简式:

请分析1个松脂酸铜中π键的个数___________加“*”碳原子的杂化方式为_____________。
(4)硫酸铜溶于氨水形成![]() 4深蓝色溶液。
4深蓝色溶液。
① ![]() 中阴离子的立体构型是_______。
中阴离子的立体构型是_______。
②在![]() 中
中![]() 之间形成的化学键称为_____,提供孤电子对的成键原子是_______________________。
之间形成的化学键称为_____,提供孤电子对的成键原子是_______________________。
③氨的沸点_________________(填“高于”或“低于”)膦;
(5)黄铜合金可以表示为![]() ,为面心立方晶胞,晶体密度为8.5
,为面心立方晶胞,晶体密度为8.5![]() ,求晶胞的边长___________(只写计算式,不求结果)
,求晶胞的边长___________(只写计算式,不求结果)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】祖母绿是四大名贵宝石之一,主要成分为Be3Al2Si6O18,含有微量的Cr、Ni、Fe元素而呈现各种颜色。回答下列问题:
(1)基态Ni2+的电子排布式为_______________;宝石中Si的杂化方式是____。
(2)成键元素电负性差值越大,化学键离子性百分数越高,在卤素与Al组成的化合物中,离子性百分数最高的化合物是______(填化学式)。
(3)六羰基铬[Cr(CO)6]用于制高纯度铬粉,它的沸点为220℃。Cr(CO)6的晶体类型是______,加热Cr(CO)6可得到高纯度铬粉和CO,反应破坏的作用力类型为_________。
(4)多数配离子显示颜色与d轨道的分裂能有关。分裂能是指配离子的中心原子(离子)的一个电子从较低能量的d轨道跃迁到较高能量的d轨道所需的能量(用Δ表示),它与中心离子的结构、电荷、配体有关。试判断分裂能Δ[Fe(H2O)63+] _____ Δ[Fe(H2O)62+](填“>”“<”或“=”),理由是___________________________。
(5)①氧化镍晶胞如图甲所示,A的原子坐标参数为:(0,0,![]() ),则底面面心B的原子坐标参数为_______________。
),则底面面心B的原子坐标参数为_______________。

②按图乙所示无限拓宽延长,NiO可形成“单层分子”,氧离子和镍离子均看着球体,其半径分别为a pm、b pm,“单层分子”截割出的最小重复结构单元在空间呈长方体,则离子在长方体内的空间利用率为____________(列出计算式即可)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com