
【题目】亚硝酸氯(ClNO)是有机合成中的重要试剂。可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+Cl2(g) ![]() 2ClNO(g)。
2ClNO(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酸氯,涉及如下反应:
①2NO2(g)+NaCl(s) ![]() NaNO3(s)+ClNO(g) K1
NaNO3(s)+ClNO(g) K1
②4NO2(g)+2NaCl(s) ![]() 2NaNO3(S)+2NO(g)+Cl2(g) K2
2NaNO3(S)+2NO(g)+Cl2(g) K2
③2NO(g)+Cl2(g) ![]() 2ClNO(g) K3
2ClNO(g) K3
则K3=________________;
(2)已知几种化学键的键能数据如下表(NO分子中氮氧键键能为630 kJ/mol,亚硝酸氯的结构为Cl-N=O):
化学键 | N | Cl-Cl | Cl-N | N=O |
键能/kJmol-1 | 630 | 243 | a | 607 |
则2NO(g)+Cl2(g) ![]() 2ClNO(g)反应的△H3和a的关系为△H3=________;
2ClNO(g)反应的△H3和a的关系为△H3=________;
(3)在1L的恒容密闭容器中充入2molNO(g)和1molCl(g),在不同温度下测得c(ClNO)与时间的关系如图A:
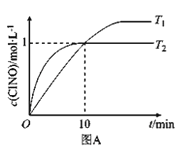
①由图A可判断T1________T2,该反应的△H________0(填“>”“<”或“=”);
②反应开始到10min时NO的平均反应速率v(NO)=________;
③T2时该反应的平衡常数K=____________;
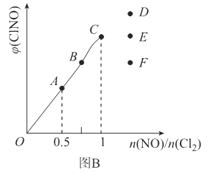
(4)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(Cl2)的变化如图B,则A、B、C三状态中,NO的转化率最大的是________点。
【答案】![]() (289-2a)kJ/mol < < 0.1mol/(Lmin) 2 A
(289-2a)kJ/mol < < 0.1mol/(Lmin) 2 A
【解析】
(1)根据盖斯定律分析计算K;
(2)根据△H=反应物的键能之和-生成物的键能之和计算判断;
(3)①温度越高,建立平衡需要的时间越短,由图象可知T2先达到平衡状态,且生成物的浓度小,结合温度对平衡的移动分析判断;②反应开始到10min时,先计算v(ClNO),再结合速率之比等于化学计量数之比计算;③根据三段式计算该反应的平衡常数K;
(4)若n(NO)不变,n(Cl2)越大,相当于单独充入氯气,平衡正向移动,NO的转化率越大,结合图像分析判断。
(1)①2NO2(g)+NaCl(s)NaNO3(s)+ClNO(g) K1,②4NO2(g)+2NaCl(s)2NaNO3(s)+2NO(g)+Cl2(g) K2,根据盖斯定律,将①×2-②可得:2NO(g)+Cl2(g)2ClNO(g),则平衡常数K3=![]() ,故答案为:
,故答案为:![]() ;
;
(2)2NO(g)+Cl2(g)2ClNO(g),△H=反应物的键能之和-生成物的键能之和=(2×630+243)-(2a+2×607)=(289-2a)kJ/mol,故答案为:(289-2a)kJ/mol;
(3)①温度越高,建立平衡需要的时间越短,根据图象可知T1<T2,降低温度c(ClNO)增大,说明平衡向正反应方向移动,说明正反应是放热反应,△H<0,故答案为:<;<;
②反应开始到10min时,c(ClNO)=1mol/L,则v(ClNO)=![]() =0.1mol/(Lmin),则NO的平均反应速率v(NO)=v(ClNO)=0.1mol/(Lmin),故答案为:0.1mol/(Lmin);
=0.1mol/(Lmin),则NO的平均反应速率v(NO)=v(ClNO)=0.1mol/(Lmin),故答案为:0.1mol/(Lmin);
③ 2NO(g)+Cl2(g)2ClNO(g)
起始(mol/L)21 0
反应(mol/L) 10.5 1
平衡(mol/L)10.5 1
T2时该反应的平衡常数K=![]() =2,故答案为:2;
=2,故答案为:2;
(4)若n(NO)不变,n(Cl2)越大,相当于单独充入氯气,平衡正向移动,NO的转化率越大,即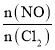 的比值越小,NO的转化率越大,根据图像,A、B、C三状态中,NO的转化率最大的是A点,故答案为:A。
的比值越小,NO的转化率越大,根据图像,A、B、C三状态中,NO的转化率最大的是A点,故答案为:A。


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源: 题型:
【题目】炭黑是雾霾中的重要颗粒物,研究发现它可以活化氧分子,生成活化氧,活化过程的能量变化模拟计算结果如图所示,活化氧可以快速氧化二氧化硫。下列说法错误的是
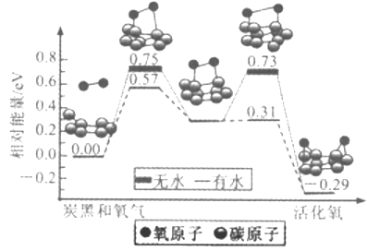
A. 氧分子的活化包括O-O键的断裂与C-O键的生成
B. 每活化一个氧分子放出0.29eV的能量
C. 水可使氧分子活化反应的活化能降低0.42eV
D. 炭黑颗粒是大气中二氧化硫转化为三氧化硫的催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50mL0.50mol·L﹣1盐酸与50mL0.55molL﹣1NaOH溶液在图示的装置中进行中和反应。通过测定反应过程中的热量可计算中和热。回答下列问题:

(1)实验中改用60mL0.50mol·L﹣1盐酸跟50mL0.55molL﹣1 NaOH溶液进行反应,与上述实验相比,所放出的热量___(填“相等”或“不相等”),所求中和热___(填“相等”或“不相等”),简述理由:___。
(2)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会___;用50mL0.50mol·L﹣1CH3COOH溶液(已知CH3COOH电离时吸热)进行上述实验,测得的中和热的数值会___。(均填“偏大”、“偏小”或“无影响”)
(3)平行地做一次这样的实验需要测定___次温度。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯的叠氮酸(HN3)是一种弱酸,常温下向25mL 0.1 mol/L NaOH溶液中加入0.2 mol/L HN3溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如下图。下列说法正确的是( )
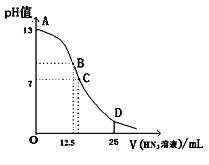
A. 该滴定过程中应用甲基橙作指示剂
B. 若B点pH=8,则c(HN3)=(10-6~10-8 )mol/L
C. 点D对应溶液中存在关系:c(HN3)>c(Na+)>c(N3-)
D. 沿曲线A→B→C的过程中,由水电离产生的c(OH-)逐渐减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题:
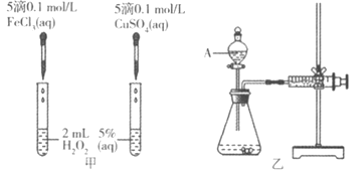
(1)定性如图甲可通过观察________________现象,定性比较得出结论。有同学提出将CuSO4改为CuCl2更为合理,其理由是________________
(2)定量如图乙所示,实验时均以生成40mL气体为准,其它可能影响实验的因素均已忽略。图中仪器A的名称为________________,实验中需要测量的数是________________
(3)加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如图所示。A、B、C、D各点反应速率由快到慢的顺序为________。
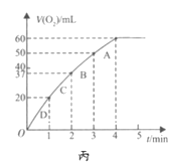
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池的反应原理如图所示。下列有关氢氧燃料电池的说法不正确的是
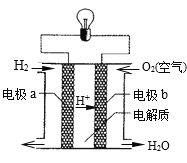
A.该电池中电极a是负极
B.该电池工作时化学能转化为电能
C.该电池的总反应为:2H2+O2=2H2O
D.外电路中电流由电极a通过导线流向电极b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中进行如下反应2SO2(g)+O2(g)![]() 2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol·L-1、0.1mol·L-1、0.2mol·L-1,当反应至正、逆反应速率相等时,可能存在的数据是( )
2SO3(g),已知反应过程中某一时刻SO2、O2、SO3的浓度分别为0.2mol·L-1、0.1mol·L-1、0.2mol·L-1,当反应至正、逆反应速率相等时,可能存在的数据是( )
A.SO2为0.4mol·L-1、O2为0.2mol·L-1B.SO2为0.25mol·L-1
C.SO2、SO3均为0.15mol·L-1D.SO3为0.4mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒容密闭容器中通入X并发生反应:2X(g)![]() Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
Y(g),温度T1、T2下X的物质的量浓度c(x)随时间t变化的曲线如图所示,下列叙述正确的是
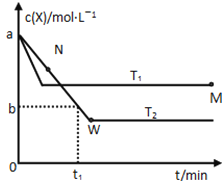
A.该反应进行到M点放出的热量大于进行到W点放出的热量
B.T2下,在0~t1时间内,υ(Y)=![]() mol/(L·min)
mol/(L·min)
C.M点的正反应速率υ正大于N点的逆反应速率υ逆
D.M点时再加入一定量的X,平衡后X的转化率减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com