
����Ŀ��Ϊȷ��Na2CO3��NaHCO3�������Ʒ����ɣ���ȡ�ķݸ���Ʒ����ˮ��ֱ���μ�����ͬŨ������60.0mL����ַ�Ӧ������CO2�����(������ɱ�״���µ������������CO2��ˮ�е��ܽ�)���±���
ʵ����� | I | II | III | IV |
�������(mL) | 60.0 | 60.0 | 60.0 | 60.0 |
��Ʒ����(g) | 2.96 | 3.70 | 5.18 | 6.66 |
CO2���(mL) | 672 | 840 | 896 | 672 |
��1����Ʒ�����ʵ���֮��n(NaHCO3)��n(Na2CO3)=___��
��2����������ʵ���Ũ��c(HCl)=___��
���𰸡�1��2 1.25mol/L
��������
��1�����������������֪��������Ʒ�������ӣ����ɶ�����̼�����������˵�������������������Na2CO3��NaHCO3����ȫ��Ӧ����ʽ���㣻
��2������ʵ����������֪����������㣬Na2CO3���ȷ�Ӧ����NaHCO3����ʽ���㡣
��1�����������������֪��������Ʒ�������ӣ����ɶ�����̼�����������˵�������������������Na2CO3��NaHCO3����ȫ��Ӧ���������Na2CO3��NaHCO3�����ʵ����ֱ�Ϊx��y�����106x+84y=2.96����x+y=![]() =0.03mol�������٢ڽ�ã�x=0.02mol��y=0.01mol��������Ʒ�����ʵ���֮��n��NaHCO3����n��Na2CO3��=0.01mol��0.02mol =1��2��
=0.03mol�������٢ڽ�ã�x=0.02mol��y=0.01mol��������Ʒ�����ʵ���֮��n��NaHCO3����n��Na2CO3��=0.01mol��0.02mol =1��2��
��2������ʵ����������֪����������㣬Na2CO3���ȷ�Ӧ����NaHCO3����6.66g��Ʒ�к���̼���ơ�̼�����Ƶ����ʵ����ֱ�Ϊ2x��x����106��2x+84x=6.66����ã�x=0.0225mol����6.66g��Ʒ�к���0.045mol̼���ơ�0.0225mol̼�����ƣ�����Ʒ���������У��ȷ�����ӦHCl+Na2CO3=NaHCO3+NaCl��0.045mol̼������ȫ��Ӧ����HCl�����ʵ���Ϊ0.045mol��̼������ȫ��Ӧ�����ٷ�����ӦNaHCO3+HCl=NaCl+H2O+CO2�������ɱ�״����672mL������̼����HCl�����ʵ���Ϊ��n(HCl)=n(CO2)=![]() =0.03mol������60mL�����к���HCl�����ʵ���Ϊ��0.045mol+0.03mol=0.075mol������������ʵ���Ũ��Ϊ��c(HCl)=
=0.03mol������60mL�����к���HCl�����ʵ���Ϊ��0.045mol+0.03mol=0.075mol������������ʵ���Ũ��Ϊ��c(HCl)=![]() =1.25mol/L��
=1.25mol/L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����20mLij���ʵ���Ũ�ȵ�AlCl3��Һ�еμ�2mol/LNaOH��Һʱ���õ���Al(OH)3�������������μ�NaOH��Һ�����(mL)��ϵ��ͼ��ʾ���Իش��������⣺
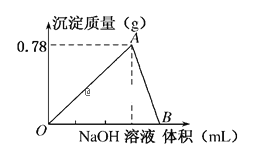
��1��ͼ��A���ʾ��������___����ʱ����NaOH��Һ�����Ϊ___mL��
��2��ͼ��B���ʾ��������___����ط�Ӧ�����ӷ���ʽΪ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ϊ��Ҫ�������ϣ��ڻ���������й㷺��Ӧ�á�
��1����̬Asԭ�ӵļ۲���ӵĵ���������ͼ��״Ϊ_____________������ͬ���ڵ�����Ԫ�صĻ�̬ԭ���У���һ����������Ϊ_____________����Ԫ�ط��š���
��2��Na3AsO3�����ڵ����������
��Na+����ɫ��Ӧ�ʻ�ɫ������Ԫ���ܲ�����ɫ��Ӧ����ԭ��Ϊ__________________________��
��Na3AsO3�����������ӵ����幹��Ϊ_____________��д��һ�����以Ϊ�ȵ�����ķ��ӣ�_____________���ѧʽ����
��3��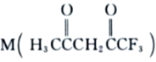 �����ںϳ�Ni2+�����壬M��Cԭ�ӵ��ӻ���ʽΪ___________��������
�����ںϳ�Ni2+�����壬M��Cԭ�ӵ��ӻ���ʽΪ___________��������![]() ������������Ŀ֮��Ϊ___________��
������������Ŀ֮��Ϊ___________��
��4��Ni��Ca����ͬһ���ڣ��Һ����������ӹ�����ͬ��������Ni���۵�ͷе���Ƚ���Ca�ĸߣ���ԭ��Ϊ___________�����־���Ni�ͷǾ���Ni����ɿ��Ŀ�ѧ����Ϊ___________��
��5��ij�����Ͻ�ľ����ṹ����ͼ��ʾ���谢���ӵ�������ֵΪNA����þ�����ܶ���=___________g��cm-3��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijδ֪��Һ���ܺ���Cl-��SO42-��CO32-��Mg2+��Al3+��K+��ȡ100mL����Һ����ʵ�飬���̼�¼�������ɴ˿�֪ԭ��Һ��
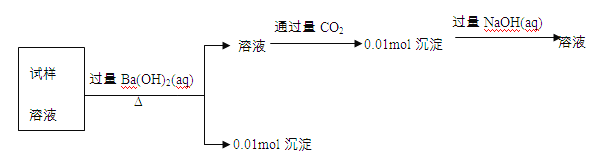
A��һ����Cl- B��һ����CO32- C��һ��û��K+ D��һ��û��Mg2+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��SO2��Na2S2O3��Na2S��Na2SO3�Ⱥ������ڹ�ҵ���й㷺����;�����������գ�
��1����ԭ�Ӻ�������Ų�ʽ____�������ӵĺ�����___��������ͬ�ĵ��ӡ�
��2��SO2���ӹ���Ϊ��V��������SO2��___��ѡ���������������Ǽ����������ӣ�����ˮ�е��ܽ�ȱ�����___��ѡ������������С������һ��������
��3����֯��������Ư����Na2S2O3��ȥ����ʱ���������·�Ӧ��___S2O32-+___Cl2+___H2O��___SO42-+___Cl-+___H+
��ƽ�÷�Ӧ����ʽ������Ӧ������2molSO42-����ת�Ƶ���____mol��
��4��Na2S�ֳƳ��������ӷ���ʽ˵��Na2S��Һ�ʼ��Ե�ԭ��___��
��5����ͼ��Na2SO3��Һ�и�����Ũ�ȵ���Դ�С��ϵʾ��ͼ�����У�����___���������ţ�����Na2SO3��Һ�и���Ũ�ȵ�ʽ��ϵ��ȷ����____��
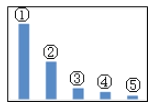
a.c(Na+)=c(SO32-)+2c(HSO3-)+2c(H2SO3)
b.c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-)
c.c(OH-)=c(HSO3-)+c(H+)+c(H2SO3)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ��Ӧ�����ֻ�����Ӧ���͵Ĺ�ϵ��ͼ��ʾ�������л�ѧ��Ӧ����3 �����( )

A.Cl2��2KBr = Br2��2KCl
B.2NaHCO3 ![]() Na2CO3+H2O+CO2��
Na2CO3+H2O+CO2��
C.4Fe(OH)2+O2+2H2O =4Fe(OH)3
D.2Na2O2+2H2O =4NaOH+ O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ơ�þ������![]() �ֱ����
�ֱ����![]() �������У�ͬ��ͬѹ�²������������֮���ǣ� ��
�������У�ͬ��ͬѹ�²������������֮���ǣ� ��
A.1��2��3B.3��2��1C.3��1��1D.1��1��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�NOx��CO�ȴ�����Ⱦ����Ĵ������Ա�����������Ҫ�����塣�ش��������⣺
��1��NOx��CO��Ӧ��������Ⱦ���������Ȼ�ѧ����ʽ����:��NO2(g)+CO(g)![]() CO2(g)+NO(g) ��H1=234.0 kJ��mol1����N2(g) +O2(g)
CO2(g)+NO(g) ��H1=234.0 kJ��mol1����N2(g) +O2(g)![]() 2NO(g)��H2=+179.5 kJ��mol1����2NO(g)+O2(g)
2NO(g)��H2=+179.5 kJ��mol1����2NO(g)+O2(g)![]() 2NO2(g) ��H3=112.3 kJ��mol1����Ӧ2NO2(g) +4CO(g)
2NO2(g) ��H3=112.3 kJ��mol1����Ӧ2NO2(g) +4CO(g)![]() N2(g)+4CO2(g)����H=__________ kJ��mol1��
N2(g)+4CO2(g)����H=__________ kJ��mol1��
��2����һ���¶��£���2 L�ĺ����ܱ������г���4.0 mol NO2��4.0 mol CO���ڴ��������·�����Ӧ��2NO2(g)+4CO(g)![]() N2(g) +4CO2(g)���������������£�
N2(g) +4CO2(g)���������������£�
0 min | 5 min | 10 min | 15 min | 20 min | |
c(NO2)/mol��L1 | 2.0 | 1.7 | 1.56 | 1.5 | 1.5 |
c(N2)/mol��L1 | 0 | 0.15 | 0.22 | 0.25 | 0.25 |
����0~10 min����CO2��Ũ�ȱ仯��ʾ�ķ�Ӧ����Ϊ______________��
��Ϊʹ�÷�Ӧ�ķ�Ӧ�����������д�ʩ�пɲ��õ���________(����ĸ����)��
a����Сѹǿ b���ʵ������¶� c������CO��Ũ�� d��ѡ���Ч����
��3�����ģ�ҵ�����ӽ���Ĥ�����ռ�ķ���,��ô������������ͼװ�õ���������Һ����ȡ������������������������ء�
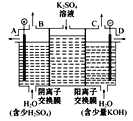
���õ��۵�������ӦʽΪ_______����ʱͨ�������ӽ���Ĥ��������____(����ڡ���С�ڡ����ڡ�)ͨ�������ӽ���Ĥ����������
���Ƶõ�����������Һ�ӳ���____(/span>�A����B����C����D��)������
�������Ƶõ�����������������������Һ���Ϊ����ȼ�ϵ��,���ظ����ĵ缫��ӦʽΪ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����̼���������PC������Ҫ�Ĺ������ϣ�ij��PC����(N)�ĺϳ�·�����£�
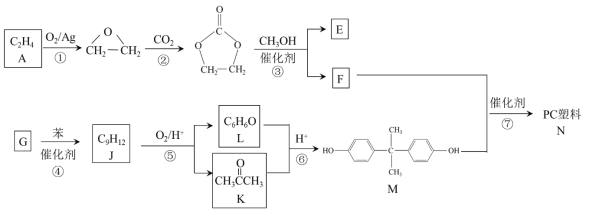
��֪��
i��R1COOR2 + R3OH![]() R1COOR3 + R2OH
R1COOR3 + R2OH
ii��R1CH=CHR2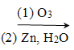 R1CHO + R2CHO
R1CHO + R2CHO
��1��A �к��еĹ�����������______��
��2���١��ڵķ�Ӧ���ͷֱ���______��______��
��3���۵Ļ�ѧ����ʽ��______��
��4�����Ǽӳɷ�Ӧ��G�ĺ˴Ź������������ַ壬G�Ľṹ��ʽ��______��
��5�����л��п������ɵ��л�����______��д��һ�ֽṹ��ʽ���ɣ���
��6���ߵĻ�ѧ����ʽ��______��
��7������ȩ�Ǻϳ������л����ԭ�ϡ�L��������ת���������Ʊ�����ȩ���ϳ�·�����£�

�м����1�Ľṹ��ʽ��______��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com