
【题目】下列各组物质互为同系物的是( )
A. 苯和乙炔 B. 甲苯和二甲苯
C. 硝基苯和三硝基甲苯 D. 乙烯和1,3-丁二烯
科目:高中化学 来源: 题型:
【题目】美国NASA曾开发一种铁—空气二次电池。该电池放电时,其原理如下图所示,电池反应为:2Fe+O2+2H2O===2Fe(OH)2。
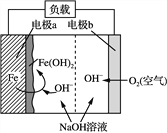
有关该电池放电时的说法正确的是( )
A. a极质量不变
B. b极为电池负极
C. 电子由a极经负载流向b极
D. 由电能转变为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. CH4、CCl4和CH3C1都是正四面体结构
B. 四氯化碳是一种常见的有机溶剂,密度比水小
C. 甲烷与氯气的取代反应,生成的产物中CH3C1最多
D. 标准状况下,2.24L一氯甲烷含有的分子数为6.02×1022
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气和氮气一定条件下反应生成氨气。已知 H-H 键、N≡N、H-N 键能分别为Q1、Q2 、Q3 kJmol-1。下列关系式中正确的是
A.3Q1 + 3Q2 < 2Q3
B.Q1+Q2 < Q3
C.3Q1 + Q2 < 6 Q3
D.3Q1 + Q2 < 2Q3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,只能表示一个化学反应的是( )
①CO32-+2H+=CO2↑+H2O
②Ba2++2OH-+2H++SO=BaSO4↓+2H2O
③Ag++Cl-=AgCl↓
④Fe+Cu2+=Fe2++Cu
⑤Cl2+H2O=H++Cl-+HClO
A.①③
B.②④
C.②⑤
D.只有⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温时,向1L固定容积的容器中充入0.1mol NO2,发生反应2NO2(g)![]() N2O4(g),下列叙述能说明该反应达到平衡状态的是
N2O4(g),下列叙述能说明该反应达到平衡状态的是
A. V(NO2)=2V(N2O4) B. 容器内的压强不变时
C. 容器中c(NO2)=c(N2O4)时 D. 容器中气体的总质量保持不变时
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.凡是盐在离子方程式中都要以离子的形式来表示
B.离子反应一定使溶液中所有离子的浓度都发生变化
C.复分解反应必须具备离子反应的某个条件
D.酸碱中和反应都能用离子方程式:H++OH-=H2O表示
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰的化合物种类较多,大多具有广泛的用途。
Ⅰ.MnO2是H2O2分解的良好的催化剂,它也具有较强的氧化性。某化学兴趣小组通过实验探究MnO2的性质。
该小组设计了如下4个方案以验证MnO2的氧化性,可行的是__________(填序号)。
把MnO2固体加入到稀盐酸中,观察是否有黄绿色气体生成
把MnO2固体加入到H2O2溶液中,观察是否有气泡产生
Na2SO3溶液中,加入MnO2固体,再滴加BaCl2溶液,观察是否有白色沉淀生成
FeSO4溶液中滴加几滴KSCN溶液,再加入MnO2固体,观察溶液是否变红
为研究溶液中MnO2的氧化能力与溶液酸碱性的关系,该小组同学设计了如下的对比实验:在室温下,取A、B、C三支试管,用同浓度同体积的KI溶液和质量、颗粒大小相同的MnO2固体反应,然后分别加入1mL0.2mol/L NaOH溶液、1mL水、1mL0.1mol/L稀硫酸。现象记录如表所示:
试管编号 | 实验现象 |
A | 溶液不变色 |
B | 溶液缓慢变浅棕褐色 |
C | 溶液迅速变棕褐色 |
①从以上实验中,我们可以得出的结论是_____________________。
②写出C试管中发生反应的离子方程式:_______________________。
Ⅱ.铁酸锰(MnFe2O4)可用于热化学循环分解水制氢,可有效缓解能源危机。MnFe2O4的制备工艺流程如图:

已知:Fe3+、Mn2+沉淀的pH如表格所示。
开始沉淀 | 完全沉淀 | |
Fe3+ | 2.7 | 4.2 |
Mn2+ | 8.3 | 10.4 |
步骤一中投入原料Fe(NO3)3和Mn(NO3)2的物质的量之比理论上应为_________________。
步骤二中需控制pH的范围是_________________。
步骤三中是否洗涤干净的判断方法是_____________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com