
【题目】实验室用下列仪器组装一套石油分馏的装置,并进行相关实验,可以得到汽油和煤油。

(1)写出下列仪器的名称:
①________;②________;③________。
(2)将以上仪器按从左到右的顺序,用字母a、b、c……进行连接:e接(____)接(____)接(____)接(____)接(____)接(____)接(____)接(____)接(____)。
(3)仪器②中A是________(填“进水口”或“出水口”,下同),B是________。
(4)蒸馏时,温度计水银球应在________(位置)。
(5)在①中注入原油后,加几片碎瓷片的目的是_______
(6)在实验结束后,为了探究石油中是否含有烯烃,某学生用③中的物质做了一个探究实验,其操作、现象及结论是________
【答案】蒸馏烧瓶 冷凝管 锥形瓶 c d a k l b f g w 进水口 出水口 蒸馏烧瓶支管口处 防止暴沸 用一支洁净的试管,取约2~3 mL容器③中的馏出物,再向试管中滴加3~4滴酸性KMnO4溶液(或溴水),若溶液颜色不消失,则石油中不含有烯烃;若溶液颜色消失,则石油中含有烯烃
【解析】
实验装置的一般安装顺序为“自下而上,从左到右”。冷凝管采用逆流原理,即上口为出水口,下口为进水口;温度计需要测定馏分的温度,所以温度计水银球与蒸馏烧瓶支管口应在同一水平线上,以保证水银球被馏分蒸气包围。
(1)蒸馏需要仪器有酒精灯、蒸馏烧瓶、铁架台、温度计、导管、冷凝管、橡胶管、牛角管、锥形瓶,根据常见仪器的名称可知,①为蒸馏烧瓶,②为冷凝管,③为锥形瓶;
(2)按组装仪器顺序从左到右,从下到上,该装置为蒸馏石油的装置,冷凝管在中间,并用铁架台固定冷凝管,右边为锥形瓶,故连接顺序为e接c接d接a接k接l接b接f接g接w;
(3)冷凝水应是下进上出,延长热量交换时间,使热量能更充分,即A口用于进水,B口用于出水;
(4)蒸馏装置的温度计插在蒸馏烧瓶中且下端在支管口处;
(5)防止烧瓶内液体受热不均匀而局部突然沸腾(爆沸)冲出烧瓶,需要在烧瓶内加入几块沸石;
(6)探究石油中是否含有烯烃的方法:用一支洁净的试管,取约2~3mL容器③中的馏出物,再向试管中滴加3~4滴酸性KMnO4溶液(或溴水),若溶液颜色不消失,则石油中不含有烯烃;若溶液颜色消失,则石油中含有烯烃。


科目:高中化学 来源: 题型:
【题目】下列说法正确的是 ( )
①增加水的量或温度,都可以加快镁跟水的反应速率。
②增加硫酸的浓度,一定可以加快锌与硫酸反应制取氢气的速率。
③对反应3H2(g) + N2(g) ![]() 2NH3(g),在一密闭容器中进行,充入氦气,则化学反应速率一定不改变。
2NH3(g),在一密闭容器中进行,充入氦气,则化学反应速率一定不改变。
④对于反应3KSCN(aq) + FeCl3(aq)![]() Fe(SCN)3(aq)+ 3KC l(aq),加入KCl固体,逆反应速率瞬时增大,随后正反应速率增大
Fe(SCN)3(aq)+ 3KC l(aq),加入KCl固体,逆反应速率瞬时增大,随后正反应速率增大
A. ①② B. ①④ C. ②④ D. 无
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学通过实验研究钠及其化合物的有关性质,请回答相关问题。
(1)实验室中少量的钠通常保存在____中,在实验室中取用钠的仪器是_____。
(2)将金属钠投入水中,发生反应的离子方程式为______________________。
(3)该同学在实验室欲配制500mL 0.1mol/L NaOH溶液。
①配制溶液时肯定不需要如下图所示仪器中的_____________(填字母),配制上述溶液还需要用到的玻璃仪器是_____________(填仪器名称)。

②配制溶液时有如下操作:a.溶解 b.摇匀 c.洗涤 d.冷却 e.称量 f.将溶液移至容量瓶g.定容,实验操作顺序正确的是________。
a. e→a→f→d→c→f→g→b b. e→a→d→f→c→f→g→b
c. e→a→f→d→c→f→b→g d. e→a→d→f→c→f→b→g
③该同学将所配制的NaOH溶液进行测定,发现浓度大于0.1mol/L。下列操作会引起所配浓度偏大的是______。
a.烧杯未进行洗涤
b.配制前,容量瓶中有少量蒸馏水
c.往容量瓶转移时,有少量液体溅出
d.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容
e.在容量瓶中定容时俯视容量瓶刻度线
f.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
④为中和100mL 2.3 mol·L-1 稀硫酸后显中性,需要加入______L 0.1mol/L NaOH溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以CO2和Na2O2为原料,制取纯净干燥的O2,实验装置如下:

下列说法不正确的是
A. 装置②中试剂可以是NaOH溶液
B. 装置③的作用是干燥O2
C. 收集氧气应选择装置a
D. 装置②、③之间应增加盛澄清石灰水的洗气瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列实验现象的说法不正确的是

A. 氨气是无色有刺激性气味的气体,密度比空气小
B. 实验1,由喷泉现象可知氨气极易溶于水且溶解速率快
C. 实验1,烧瓶溶液中的含氮微粒有:NH3、NH3·H2O和NH4+
D. 实验2,加热过程中温度和c(NH3·H2O)对NH3·H2O电离平衡移动方向的影响一致
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是元素周期表短周期的一部分,若A原子最外层的电子数比次外层的电子数少3,则下列说法中正确的是( )

A. D与C不能形成化合物
B. D的最高正价与B的最高正价相等
C. A、B、C的最高价氧化物对应的水化物酸性强弱的关系是C>B>A
D. D元素最高正价和最低负价的绝对值的代数和等于8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在恒温恒容装置中进行合成氨反应(正反应为放热反应),各组分浓度—时间图象如下。

①表示N2浓度变化的曲线是____(填序号)。
②前25 min内,用H2浓度变化表示的化学反应速率是____。该温度下该反应的平衡常数为____。
(2)在恒温恒压装置中进行工业合成氨反应,下列说法正确的是____(填序号)。
a.气体体积不再变化,则已平衡
b.气体密度不再变化,则已平衡
c.平衡后,压缩容器,会生成更多NH3
d.平衡后,往装置中通入一定量Ar,平衡不移动
(3)电厂烟气脱氮:主反应为①4NH3(g)+6NO(g)![]() 5N2(g)+6H2O(g) ΔH<0,副反应为②2NH3(g)+8NO(g)
5N2(g)+6H2O(g) ΔH<0,副反应为②2NH3(g)+8NO(g)![]() 5N2O(g)+3H2O(g) ΔH>0,平衡混合气中N2与N2O含量与温度的关系如图所示。
5N2O(g)+3H2O(g) ΔH>0,平衡混合气中N2与N2O含量与温度的关系如图所示。

请回答:在400~600 K时,平衡混合气中N2含量随温度的变化规律是____________________,导致这种规律的原因是__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中稀少而分散,常从精炼铜的阳极泥中提取硒。
(1)粗铜精炼时,通常用精铜作____极(填“阴”或“阳”)。
(2)硒在元素周期表中的位置如图所示:

Se原子结构示意图可表示为________。
②从原子结构角度解释硫与硒元素性质相似与不同的原因:同一主族________。
(3)阳极泥中的硒主要以Se和CuSe的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:
i.将含硒阳极泥与浓硫酸混合焙烧,产生SO2、SeO2的混合气体
ii.用水吸收i中混合气体,可得Se固体
① 请写出CuSe与浓H2SO4反应的化学方程式________。
② 焙烧过程产生的烟气中含有少量SeO2,可用NaOH溶液吸收,二者反应生成一种盐,该盐的化学式为_______。
③ 写出步骤ⅱ中的化学方程式_______。
(4)下列说法合理的是________。
a. SeO2既有氧化性又有还原性,其还原性比SO2强
b. 浓硒酸可能具有强氧化性、脱水性
c. 热稳定性:H2Se < HCl < H2S
d. 酸性:H2SeO4 < HBrO4 < HClO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含氮化合物与生产、生活、生命和环境息息相关。
(1)NO加速臭氧层被破坏,其反应过程如图所示。
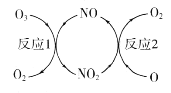
①NO的作用是________________________。
②已知:O3(g)+O(g) =2O2(g) △H=-143kJ·mol-1
反应l:O3(g)+NO(g) =NO2(g)+O2(g)△H1=-200.2kJ·mol-1
则反应2的热化学方程式为____________________________。
(2)肌红蛋白(Mb)是肌肉内储存氧的蛋白质,构成肌红蛋白的甘氨酸(H2NCH2COOH)是一种两性物质,在溶液中以三种离子形式存在,其转化关系如下 三种离子的物质的量分数(δ)与[
三种离子的物质的量分数(δ)与[![]() ]的关系如图所示。
]的关系如图所示。
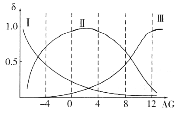
①溶液呈中性时,三种离子浓度由大到小的顺序为______________________。
②向AG=12的溶液中加入过量NaOH溶液时,主要反应的离子方程式为______________。
(3)肌红蛋白(Mb)可与O2结合生成MbO2:![]() 。37℃时测得肌红蛋白的结合度(α)与p(O2)的关系如下表。
。37℃时测得肌红蛋白的结合度(α)与p(O2)的关系如下表。
[结合度(α)指已与O2结合的肌红蛋白占总肌红蛋白的物质的量分数]
p(O2)/kPa | 0.50 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 | 6.00 |
α(MbO2)% | 50.0 | 66.7 | 80.0 | 85.7 | 88.9 | 90.9 | 92.3 |
①计算37℃时,上述反应的平衡常数K=__________kPa-1(气体和溶液中的溶质分别用分压和物质的量浓度表示)。
②37℃时,若空气中氧气分压为21.0 kPa,则人正常呼吸时α的最大值为________%(保留1位小数)。
③温度不变时,游客在山顶时体内MbO2的浓度比在山下________(填“高”或“低”)。
④研究发现,v正=k正·c(Mb)·p(O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com