
【题目】(1)质量之比为16∶7∶6的三种气体SO2、CO、NO,分子数之比为________;氧原子数之比为________;相同条件下的体积之比为________。
(2)标准状况下,1.7 g NH3的体积为________L,它与标准状况下________L H2S含有相同数目的氢原子。
(3)某气态氧化物的化学式为RO2,标准状况下,1.28 g该氧化物的体积为448 mL,则该氧化物的摩尔质量为__________,R的相对原子质量为________。
(4)在同温同压下,2 g CO2的体积为120 mL,而2 g A气体的体积为165 mL,则气体A的摩尔质量为________。标准状况下,11.2 L CO2和CO的质量是18 g,则其中含CO2的质量为________g,CO的体积为________。
(5)一储气瓶真空时质量为500 g。标准状况下,充满氧气后质量为508 g,装满某气体X后总质量为511 g。则该储气瓶的体积为________L,X的相对分子质量为________。
【答案】5∶5∶410∶5∶45∶5∶42.243.3664 g·mol-13232 g/mol115.6 L5.644
【解析】
(1)根据n=![]() 可知,质量比为16:7:6的三种气体 SO2、CO、NO的物质的量之比为
可知,质量比为16:7:6的三种气体 SO2、CO、NO的物质的量之比为
![]() :
:![]() :
:![]() =5:5:4,则分子数目之比为5:5:4,含有氧原子数目之比为5×2:5×1:4×1=10:5:4,相同条件下气体体积之比等于物质的量之比,故三者体积之比为5:5:4;(2)1.7g氨气的物质的量为
=5:5:4,则分子数目之比为5:5:4,含有氧原子数目之比为5×2:5×1:4×1=10:5:4,相同条件下气体体积之比等于物质的量之比,故三者体积之比为5:5:4;(2)1.7g氨气的物质的量为 ![]() =0.1mol,其体积为0.1mol×22.4L/mol=2.24L,设它与标准状况下VL硫化氢含有相同数目的氢原子,则0.1mol×3=
=0.1mol,其体积为0.1mol×22.4L/mol=2.24L,设它与标准状况下VL硫化氢含有相同数目的氢原子,则0.1mol×3= ![]() ×2,解得V=3.36L;(3)气体的物质的量为
×2,解得V=3.36L;(3)气体的物质的量为 ![]() =0.02mol,该氧化物的摩尔质量为
=0.02mol,该氧化物的摩尔质量为 ![]() =64gmol-1,又气体的摩尔质量与相对分子质量在数值上相等,R的相对原子质量为64-16×2=32;(4)(1)设A的摩尔质量为M,则2gA气体的物质的量n=
=64gmol-1,又气体的摩尔质量与相对分子质量在数值上相等,R的相对原子质量为64-16×2=32;(4)(1)设A的摩尔质量为M,则2gA气体的物质的量n=![]() ,二氧化碳的物质的量n′=
,二氧化碳的物质的量n′=![]() ,同温同压下,气体的体积之比等于物质的量之比,所以
,同温同压下,气体的体积之比等于物质的量之比,所以![]() :=
:=![]() =120:165,解得M=32(g/mol);标准状况下,11.2LCO2和CO的物质的量=
=120:165,解得M=32(g/mol);标准状况下,11.2LCO2和CO的物质的量=![]() =0.5mol,设二氧化碳的物质的量为x,一氧化碳的物质的量为y,则:
=0.5mol,设二氧化碳的物质的量为x,一氧化碳的物质的量为y,则:![]() ,解得x=0.25mol;y=0.25mol;则m(CO2)=nM=0.25mol×44g/mol=11g; V(CO)=nVm=0.25mol×22.4L/mol=5.6L;(5)氧气的质量为508g-500g=8g,其物质的量为
,解得x=0.25mol;y=0.25mol;则m(CO2)=nM=0.25mol×44g/mol=11g; V(CO)=nVm=0.25mol×22.4L/mol=5.6L;(5)氧气的质量为508g-500g=8g,其物质的量为![]() =0.25mol,氧气体积为0.25mol×22.4L/mol=5.6L,储气瓶的体积等于气体的体积,即储气瓶的体积为5.6L;X气体的质量为511g-500g=11g,相同条件下,相同体积的气体的物质的量相等,X的物质的量等于氧气物质的量,则X物质的量为0.25mol,故其摩尔质量为
=0.25mol,氧气体积为0.25mol×22.4L/mol=5.6L,储气瓶的体积等于气体的体积,即储气瓶的体积为5.6L;X气体的质量为511g-500g=11g,相同条件下,相同体积的气体的物质的量相等,X的物质的量等于氧气物质的量,则X物质的量为0.25mol,故其摩尔质量为![]() =44g/mol,故其相对分子质量为44。
=44g/mol,故其相对分子质量为44。


科目:高中化学 来源: 题型:
【题目】三氧化二镍是一种重要的电子元件材料、蓄电池材料。工业上利用含镍废料(以镍、铁、钙、镁合金为主)制取草酸镍(NiC2O4·2H2O),再高温煅烧草酸镍制取三氧化二镍。已知草酸的钙、镁、镍盐均难溶于水。根据下列工艺流程示意图回答问题。
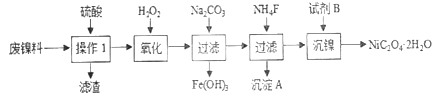
(1)操作1的名称为__________。
(2)保持其他条件相同,在不同温度下对废镍料进行“酸浸”,镍浸出率随时间变化如图。“酸浸”的适宜温度与时间分别为_______(填字母)。
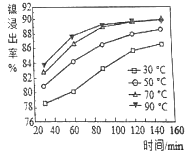
a.30℃、30min b.70℃、120min
c.90℃、150min d.90℃、120min
(3)沉淀A为CaF2和_________(填化学式)。
(4)试剂B的化学式为_________________。
(5)NiC2O4·2H2O样品经某稀酸酸化处理后,用稀KMnO4标准溶液滴定[在本实验条件下,Ni(Ⅱ)不能被氧化,其他物质不参与反应],通过测定草酸的量可测定NiC2O4·2H2O样品的纯度,滴定反应为:2MnO4-+6H++5H2C2O4=2Mn2++10CO2↑+8H2O。实验中称取0.183g样品,滴定时消耗了0.0400mol.L-1的KMnO4溶液8.00mL,则该样品中NiC2O4·2H2O的质量分数为_________。
(6)高温煅烧草酸镍制取三氧化二镍时会产生CO、CO2、水蒸气等混合气体。某同学设计如下实验流程进行检验。
混合气体![]() 现象
现象![]() 现象
现象![]()
![]() 现象
现象![]() 现象
现象
①试剂1的名称为____________。
②证明混合气体有CO的现象是_____________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向等物质的量浓度的NaC1、MgCl2、AlC13三种溶液中,加入足量的AgNO3溶液,产生的沉淀的质量比为3:2:1,则NaC1、MgCl2、AlC13三种溶液体积比为( )
A.9:3:1B.6:3:2C.3:2:1D.1:1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中,B、D、E、F、G是氧化物且B为红棕色固体,F、K是氢化物且F为常温常压下常见无色液体,C、H是日常生活中最常见的金属单质,J是黄绿色气体。O是白色沉淀且B、H、L、M、N、O中含有同种元素,I是基础化学工业的重要产品(图中部分反应物和生成物没有列出)。
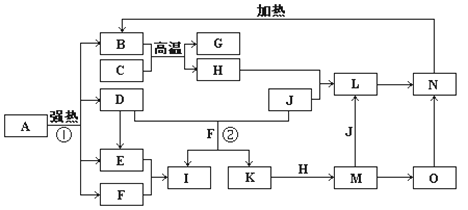
请按要求回答:
(1)写出G、L的化学式G:_____________________,L:______________________
(2)反应②的离子方程式 ________________________________________________。
(3)写出反应M→L的离子方程式为________________________________________。
(4)若将O敞口久置,变质过程中的现象为___________________________________
发生的化学方程式为__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在标准状况下,CO和CO2的混合气体共39.2 L,质量为61 g。则两种气体的物质的量之和为________mol。其中CO2为________mol,CO占总体积的________%。
(2)448 mL某气体在标准状况下的质量为1.28 g,则该气体的相对分子质量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25 ℃、101 kPa条件下,将15 L O2通入10 L CO和H2的混合气体中,使其完全燃烧,干燥后,恢复至原来的温度和压强。
(1)若剩余气体的体积是15 L,则原CO和H2的混合气体中V(CO)=________ L,V(H2)=________ L。
(2)若剩余气体的体积为a L,则原CO和H2的混合气体中V(CO)∶V(H2)=________。
(3)若剩余气体的体积为a L,则a的取值范围是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 常温常压下,16 g CH4中含有4NA个C—H键
B. 1 mol·L-1 NaCl溶液中含有NA个Na+
C. 1 mol Cu与足量的稀硝酸反应产生NA个NO分子
D. 标准状况下,22.4 L氦气中含有2NA个He原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知NaHSO3溶液显酸性,溶液中存在以下平衡:HSO3﹣+H2OH2SO3+OH﹣①HSO3﹣H++SO32﹣②,向0.1molL﹣1的NaHSO3溶液中分别加入以下物质,下列有关说法正确的是( )
A.加入少量金属Na,平衡①左移,平衡②右移,溶液中c(HSO3﹣)增大
B.加入少量Na2SO3固体,则c(H+)+c(Na+)=c(HSO3﹣)+c(OH﹣)+![]() c(SO32﹣)
c(SO32﹣)
C.加入少量NaOH溶液,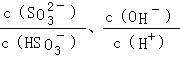 的值均增大
的值均增大
D.加入氨水至中性,则2c(Na+)=c(SO32﹣)>c(H+)=c(OH﹣)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com