
�ᾧõ���Ǿ���ǿ��õ�����������ϣ��������з�Ӧ·�ߺϳ�(���ַ�Ӧ������ȥ):
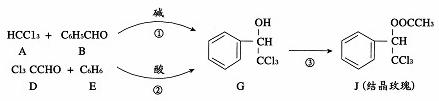
��ش���������.
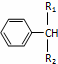
(1)A�������__________������Cl2��Ӧ����A��������__________��B�еĹ�������__________��
(2)��֪:B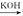 ���״�+������أ���Ӧ·�ߢٵõ��IJ����ˮ��ȡ����Һ���ܳ�ȥ�ĸ�������______________��
���״�+������أ���Ӧ·�ߢٵõ��IJ����ˮ��ȡ����Һ���ܳ�ȥ�ĸ�������______________��
(3)��֪: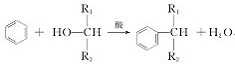 ����Ӧ·�ߢڵõ�һ�ָ������˴Ź���������4��壬�������շ�����֮��Ϊ____________��
����Ӧ·�ߢڵõ�һ�ָ������˴Ź���������4��壬�������շ�����֮��Ϊ____________��
(4 )G��ͬ���칹��L��FeCl3��Һ��ɫ��������������ˮ��Ӧδ����ɫ�������������ܷ�����ȥ��Ӧ����������ȥ��Ӧ��Ҫ������Ϊ__________����ȥ��Ӧ�����л���Ľṹ��ʽΪ____________��ֻдһ�֣���
(5)��Ӧ�۵Ļ�ѧ����ʽΪ____________________���÷�Ӧ�ķ�Ӧ����Ϊ___________________��
��֪ʶ�㡿�л�������еĹ����ż���ṹ���л���ĺϳ� L7M3
���𰸽�����
(1)±���� CH4����� -CH0��ȩ��(��I�֣���3��)
(2)�������(2��) (3)1:2:4:4 (������˳����������)(2��)
(4) NaOH���Ҵ���Һ���ȣ�3�֣�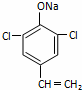 ��
��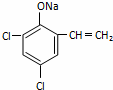 ��2�֣�
��2�֣�
(5) 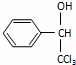 +CH3COOH
+CH3COOH
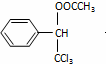 +H2O(2��) ������Ӧ��ȡ����Ӧ����1�֣�
+H2O(2��) ������Ӧ��ȡ����Ӧ����1�֣�
��������1��AΪ���ȼ��飬���й�����Clԭ�ӣ�����AΪ±�����������ܹ�����������ȡ����Ӧ�������ȼ��飻�л���BΪ����ȩ�����еĹ�����Ϊȩ����-CHO��
��2���������Ϊ�Σ����Ա������ܹ�����ˮ�����ˮ��ȡ����Һ���ܳ�ȥ�ĸ������DZ�����أ�
��3�����ݷ�Ӧ +
+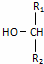

 +H2O��֪��
+H2O��֪�� �ܹ���G
�ܹ���G ��Ӧ����
��Ӧ����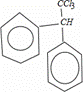 �����л�������к���4��λ�ò�ͬ��H������֮��Ϊ1��2��4��4�������Գƣ�����������շ�����֮��Ϊ1��2��4��4��
�����л�������к���4��λ�ò�ͬ��H������֮��Ϊ1��2��4��4�������Գƣ�����������շ�����֮��Ϊ1��2��4��4��
��4��������FeCl3��Һ��ɫ��֪L�����ǻ���������������ˮ��Ӧδ����ɫ��������˵�����ǻ����ڡ���λû��H�����ڡ���λ��ȡ��������L��NaOH���Ҵ���Һ����˵��L�ܷ�����ȥ��Ӧ���û�����-C2H4Cl����L��NaOH���Ҵ���Һ���ȣ������л���Ľṹ��ʽΪ ��
��  ��
��
��5����Ӧ��Ϊ �����ᷢ��������Ӧ����
�����ᷢ��������Ӧ���� ����Ӧ�Ļ�ѧ����ʽΪ��
����Ӧ�Ļ�ѧ����ʽΪ�� +CH3COOH
+CH3COOH
 +H2O
+H2O
��˼·�㲦�����⿼�����л�����ࡢ�л���ṹ�����ʡ��л��ϳɷ�����ơ�ͬ���칹�������֪ʶ����Ŀ�Ѷ��еȣ�ע�����ճ����л�����ɡ����༰���еĽṹ�����ʣ���ȷͬ���칹��ĸ�����㷽������������������ѧ�����Ӧ����ѧ֪ʶ��������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������һ�����ᣬ��������ʴ��������֪25��ʱ��
HF(aq) + OH��(aq)  F��(aq) + H2O(l) ��H=��67.7 kJ/mol
F��(aq) + H2O(l) ��H=��67.7 kJ/mol
H+(aq) + OH��(aq)  H2O(l) ��H=��57.3kJ/mol
H2O(l) ��H=��57.3kJ/mol
��10 mL 0.1mol/L��NaOH��Һ�У�����10 mL Ũ��Ϊc mol/L��HFϡ��Һ������˵������������ �� ��
A�����������Һ�¶����ߣ�HF�ĵ���̶ȼ�С�������ǻӷ���
B��ˮ������Ȼ�ѧ����ʽΪ��H2O(1) 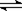 H+(aq)+OH��(aq)����H= +57.3kJ/mol
H+(aq)+OH��(aq)����H= +57.3kJ/mol
C����c > 0.1ʱ��һ�������ڣ�c(Na+) = c(F��)
D������Ϻ���Һ�У�c(Na+)>c(OH��) >c(F��)>c(H+)����cһ��С��0.1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
���л���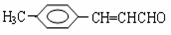 ����Ϊ
����Ϊ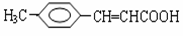 ��������������������ǣ� ��
��������������������ǣ� ��
A��O2 B������KMnO4 C��������Һ D����ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����й�ʵ��ԭ����ʵ�������ȷ����
A.��ˮʪ��pH��ֽ����ij��Һ��pHֵ
B.ʢ��NaOH��Һʱ.ʹ�ô���������ĥ��ƿ
C.��50 mL��ʽ�ζ��ܿ�ȷ��ȡ25.00 mLKMnO4��Һ
D.�ñ���ȡ��ˮ�е���ʱ������ı���Һ�ӷ�Һ©���¿ڷų�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
ij�о�С��Ϊ��̽��һ����������x(��������Ԫ��)����ɺ�����.��
�Ʋ����������ʵ��:

��ȡ10.80gX�ڶ��������м�������ȫ�ֽ⣬�õ�6.40g����1����ش��������⣺
(1)X�Ļ�ѧʽΪ �������������м���X����ȫ�ֽ�Ļ�ѧ��Ӧ����ʽΪ
��
(2)һ�������£�����������1�е�ij�ֳɷֿ��ܷ���������ԭ��Ӧ��д��һ�����ܵĻ�ѧ��Ӧ����ʽ �������ʵ�鷽����֤�÷�Ӧ�IJ��� ��
(3)��ɫ����1�н���Ԫ�ص�ԭ�ӽṹʾ��ͼΪ ������ĵ���ʽΪ ��
(4)��ɫ����2�ڿ����б�ɺ��ɫ������ԭ���� ��
(�û�ѧ��Ӧ����ʽ��ʾ)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
agCO2�к���b�����ӣ����ӵ�����Ϊ��������
| �� | A�� |
| B�� |
| C�� |
| D�� |
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��NA��ʾ�����ӵ�������ֵ��������������ȷ���ǣ�������
| �� | A�� | ��������ΪNA��NO2��CO2��������к��е���ԭ����Ϊ2NA |
| �� | B�� | ������1.00mol•L��1��NaCl��Һ1.00L���ɽ�����1.00Lˮ�� |
| �� | C�� | 1molAl3+���Ӻ��еĺ��������Ϊ3NA |
| �� | D�� | 1.0L1.0mo1•L ��1 ��NaOHˮ��Һ�к��е���ԭ����Ϊ2NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����������ȷ����
A��ֻ��һ��Ԫ�ص����ʣ�����Ϊ�����
B���ǽ���Ԫ�ض�������Ԫ�أ����������������ڻ����3
C��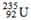 ������Ϊ143��ͨ����ѧ�仯����ʵ��235U��238U����ת��
������Ϊ143��ͨ����ѧ�仯����ʵ��235U��238U����ת��
D����ҵ��N2�Ʊ������Լ���NH3�����Ʊ�����Ĺ��̶����ڵ��Ĺ̶�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�������� ��ȷ����( )
��ȷ����( )
A.���ԭ�ӽṹģ�͵Ŀ�ѧ�Ұ�ʱ���Ⱥ������ǣ������١�¬ɪ������ķ��������
B.����������������ѧ���ʵ�����dz��õ��ֶΣ�ԭ�����չ��׳�����ȷ�������к�����Щ�ǽ���Ԫ��
C.�����ϴ��������̲��ڴ��У�����屻��Ϊ������Ԫ�ء�
D.������ˮӦ��������ɫ�Լ�ƿ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com