
用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
|
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
|
| B. | 欲配置1.00mol•L﹣1的NaCl溶液1.00L,可将溶于1.00L水中 |
|
| C. | 1molAl3+离子含有的核外电子数为3NA |
|
| D. | 1.0L1.0mo1•L ﹣1 的NaOH水溶液中含有的氧原子数为2NA |
| 阿伏加德罗常数.. | |
| 专题: | 阿伏加德罗常数和阿伏加德罗定律. |
| 分析: | A、根据NO2和CO2的分子结构来分析; B、欲配制溶液1.00L,应将氯化钠溶于水配成1.00L溶液; C、依据铝离子含有10个电子分析; D、根据溶液由溶质和溶剂构成来分析. |
| 解答: | 解:A、由于NO2和CO2的分子结构中均含2个氧原子,故当NO2和CO2的分子总数为NA时,含有的氧原子数为2NA,故A正确; B、欲配置1.00mol•L﹣1的NaCl溶液1.00L,应将58.5g的NaCl溶于水配成1.00L溶液,故B错误; C、铝离子含有10个电子,1mol Al3+包含的电子数为10NA个,故C错误; D、1.0L1.0mo1•L ﹣1 的NaOH水溶液中,含溶质NaOH1.0mol和溶剂H2O,故含有的氧原子数不是2NA,故D错误. 故选A. |
| 点评: | 本题考查了有关阿伏伽德罗常数的计算,注意分子结构和电子数的分析,难度中等. |


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.氯化钠溶液在电流作用下电离成Na+与Cl‑
B.溶于水后能电离出H+的化合物都是酸
C.氯化氢溶于水后能导电,但液态氯化氢不能导电
D.导电性强的溶液中自由移动离子数 目一定比导电性弱的溶液中自由移动离子数目多
目一定比导电性弱的溶液中自由移动离子数目多
查看答案和解析>>
科目:高中化学 来源: 题型:
在1 L溶液中含有Fe(NO3)3和H2SO4两种溶质,其浓度分别为0.2 mol•L-1和1.5
mol•L-1,现向该溶液中加入39.2 g铁粉使其充分反应。下列有关说法正确的是( )
A.反应后溶液中Fe3+物质的量为0.8 mol
B.反应后产生13.44 L H2(标准状况)
C.反应后溶液中Fe2+和Fe3+物质的量之和为0.9 mol
D.由于氧化性Fe3+>H+,故反应中先没有气体产生后产生气体
查看答案和解析>>
科目:高中化学 来源: 题型:
结晶玫瑰是具有强烈玫瑰香气的香料,可由下列反应路线合成(部分反应条件略去):
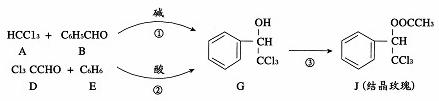
请回答下列问题.
(1)A的类别是__________,能与Cl2反应生成A的烷烃是__________;B中的官能团是__________。
(2)已知:B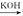 苯甲醇+苯甲酸钾,则经反应路线①得到的产物加水萃取、分液、能除去的副产物是______________。
苯甲醇+苯甲酸钾,则经反应路线①得到的产物加水萃取、分液、能除去的副产物是______________。
(3)已知: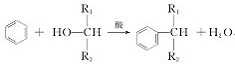 ,则经反应路线②得到一种副产物,其核磁共振氢谱有4组峰,各组吸收峰的面积之比为____________。
,则经反应路线②得到一种副产物,其核磁共振氢谱有4组峰,各组吸收峰的面积之比为____________。
(4 )G的同分异构体L遇FeCl3溶液显色,与足量饱和溴水反应未见白色沉淀产生,且能发生消去反应,发生该消去反应需要的条件为__________,消去反应所得有机物的结构简式为____________(只写一种)。
(5)反应③的化学方程式为____________________。该反应的反应类型为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某气体物质,经测定其蒸气密度折合成标准状况约为1.518 g/L.该化合物可能是下列的( )
|
| A. | HCl | B. | H2S | C. | CH4 | D. | C2H6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | 一定温度、压强下,气体体积由其分子的大小决定 |
|
| B. | 一定温度、压强下,气体体积由其物质的量的多少决定 |
|
| C. | 气体摩尔体积是指1mol任何气体所占的体积为22.4L |
|
| D. | 不同的气体,若体积不等,则它们所含的分子数一定不等 |
查看答案和解析>>
科目:高中化学 来源: 题型:
右图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制100mL 1.84mol•L﹣1的稀硫酸.可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平.
请回答下列问题:
(1)配制稀硫酸时,还缺少的仪器有 100mL容量瓶、玻璃棒 填写名称).
(2)经计算,配制100mL 1.84mol•L﹣1的稀硫酸需要用量筒量取上述浓硫酸的体积为 10.0 mL.
(3)在烧杯中稀释浓硫酸的实验操作为 在小烧杯中加适量水,将浓硫酸缓慢加入水中,边加边搅拌
,若在稀释过程中,少量浓硫酸不慎沾在手上,处理方法为 先用干抹布抹去,再用较多的水冲洗,再用3%~5%的NaHCO3溶液冲洗 .
(4)对所配制的稀硫酸进行测定,发现其浓度大于1.84mol•L﹣1,配制过程中下列各项操作可能引起该偏差的是 ACE (填写字母)
A.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
B.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
C.将硫酸稀释后立即转入容量瓶后,紧接着就进行以后的实验操作
D.转移溶液时,不慎有少量溶液洒到容量瓶外面
E.定容时,俯视容量瓶刻度线进行定容
F.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,又补充几滴水至刻度处.

查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、W为四种短周期主族元素。其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期。X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是
A.Y元素最高价氧化物对应水化物的化学式为H2YO4
B.原子半径由小到大的顺序为:W<X<Y<Z
C.X与W形成的化合物属于离子化合物
D.Y、Z两元素的气态氢化物中,Z的气态氢化物较稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.胶体粒子很小,可以透过半透膜
B.胶体与其它分散系的本质区别是胶体有丁达尔效应,而其它分散系却没有
C.直径介于1nm -100nm之间的微粒称为胶体
D.豆浆、雾、有色玻璃都是胶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com