
下列说法正确的是( )
A.胶体粒子很小,可以透过半透膜
B.胶体与其它分散系的本质区别是胶体有丁达尔效应,而其它分散系却没有
C.直径介于1nm -100nm之间的微粒称为胶体
D.豆浆、雾、有色玻璃都是胶体
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
|
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA |
|
| B. | 欲配置1.00mol•L﹣1的NaCl溶液1.00L,可将溶于1.00L水中 |
|
| C. | 1molAl3+离子含有的核外电子数为3NA |
|
| D. | 1.0L1.0mo1•L ﹣1 的NaOH水溶液中含有的氧原子数为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述 正确的是( )
正确的是( )
A.提出原子结构模型的科学家按时间先后依次是:道尔顿、卢瑟福、汤姆生、玻尔
B.借助仪器来分析化学物质的组成是常用的手段,原子吸收光谱常用来确定物质中含有哪些非金属元素
C.地球上大量的溴蕴藏在大海中,因此溴被称为“海洋元素”
D.新制氯水应保存在无色试剂瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
在标准状况 下,由CO和CO2组成的混合气体13.44 L,
下,由CO和CO2组成的混合气体13.44 L, 其质量为24g,此混合气体中C和O两种原子的物质的量之比是( )
其质量为24g,此混合气体中C和O两种原子的物质的量之比是( )
A.3∶7 B.3∶4 C.4∶7 D.1∶3
查看答案和解析>>
科目:高中化学 来源: 题型:
已知R2-的核内有x个中子,R的质量数为M,则m克R2-含有的电子的物质的量为( )
A.(M-x+2 )mol B.m(M+x-2
)mol B.m(M+x-2 )/M mol
)/M mol
C.m(M-x-2 )/M mol D. m(M-x+2
)/M mol D. m(M-x+2 )/M mol
)/M mol
查看答案和解析>>
科目:高中化学 来源: 题型:
有以下几种物质:①食盐晶体 ②乙醇 ③水银 ④蔗糖 ⑤冰醋酸(纯醋酸晶体)⑥KNO3溶液 ⑦熔融的氢氧化钠 ⑧液态氯化氢 填空回答(填序号):
(1)以上物质可以导电的是 ;
(2)以上物质中属于电解质的是 ;
(3)以上物质中属于非电解质的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
现用质量分数为98%、密度为1.84 g·cm-3的浓H2SO4来配制500 mL0.2 mol/L的稀H2SO4。可供选择的仪器有:①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒⑥容量瓶 ⑦托盘天平 。请回答下列问题:
(1) 上述仪器中,在配制稀H2SO4时用不到的有 (填代号)。
(2) 将计算、取得的浓H2SO4加适量蒸馏水稀释,冷却片刻,随后全部转移到 mL的容量瓶中,转移时应用玻璃棒 。转移完毕,用少量蒸馏水 ,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。然后缓缓地把蒸馏水直接注入容量瓶直到液面接近刻度 处。改用 加蒸馏水到瓶颈刻度的地方,振荡、摇匀后,装瓶、贴签。
(3) 在配制过程中,其他操作都准确,下列操作中,能引起误差偏高的有 (填代号)。
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中
③将浓H2SO4直接倒入烧杯,再向烧杯中注入蒸馏水稀释浓H2SO4
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤转移前,容量瓶中含有少量蒸馏水
⑥定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑦定容时,俯视标线
查看答案和解析>>
科目:高中化学 来源: 题型:
煤化工中常需研究不同温度下平衡常数、投料比及热值等问题.
已知:CO(g)+H2O(g) H2(g)+CO2(g)平衡常数随温度的变化如下表:
H2(g)+CO2(g)平衡常数随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
试回答下列问题:
在800℃发生上述反应,以表中的物质的量投入恒容反应器,其中向正反应方向移动的有 (选填A、B、C、D、E);
| n(CO) | n(H2O) | n(H2) | n(CO2) | |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 2 | 1 | 2 | 3 |
| D | 0.5 | 2 | 1 | 1 |
| E | 3 | 1 | 2 | 1 |
在1L密闭容器中通入10 molCO和10 mol水蒸气,在500℃下经过30s达
到平衡,则30s内CO的平均反应速率为
(3)已知在一定温度下,C(s)+CO2(g)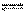 2CO(g)平衡常数K;K的表达式 ;
2CO(g)平衡常数K;K的表达式 ;
C(s)+H2O(g)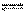 CO(g)+ H2(g)平衡常数K1;
CO(g)+ H2(g)平衡常数K1;
CO(g)+H2O(g)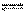 H2(g)+ CO2(g)平衡常数K2;
H2(g)+ CO2(g)平衡常数K2;
则K、K1、K2之间的关系是:
某温度、容积固定容器中,投入一定反应物,对可逆反应
C(s)+ CO2(g)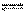 2CO(g)不能判断该反应达到化学平衡状态的是
2CO(g)不能判断该反应达到化学平衡状态的是
A.c(CO2)= c(CO) B.混合气体相对分子质量不变
C.容器中的压强不变 D.v正(CO)= 2v正(CO2) E.c(CO)保持不变
(5)如图1所示,在甲、乙两容器中都充入1mol C和1mol CO2,并使甲、乙
两容器初始容积相等.在相同温度下发生反应C(s)+CO2(g) 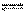 2CO(g),
2CO(g),
并维持反应过程中温度不变.已知甲容器中CO2的转化率随时间变化的
图象如图2所示,请在图2中画出乙容器中CO2的转化率随时间变化的图象.

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com