
����Ŀ������(H2C2O4)��һ�ֶ�Ԫ���ᡣ��������H2C2O4��Һ�еμ�NaOH��Һ�������Һ��lgX[X��ʾ![]() ��
��![]() ]��pH�ı仯��ϵ��ͼ��ʾ������˵������ȷ����
]��pH�ı仯��ϵ��ͼ��ʾ������˵������ȷ����

A. ֱ��I��X��ʾ����![]()
B. ֱ��I������б�ʾ�Ϊ1
C. c(HC2O4��)>c(C2O42��)>c(H2C2O4)��Ӧ1.22<pH<4.19
D. c(Na+)=c(HC2O4��)+2c(C2O42��)��ӦpH=7
���𰸡�C
��������
A������lgX=0ʱ��pH=-lgc(H��)=-lgK,�����жϣ�
B����pH=0������㣻
C������ƽ�ⳣ������ʽ�����ͼ��lgX=0ʱ�������pH��
D��Ӧ�õ���غ�����
A����Ԫ��������K1=c(H��)c(HC2O4��)/c(H2C2O4)>K2=c(H��)c(C2O42��)/c(HC2O4��)����lgX=0ʱ��pH=-lgc(H��)=-lgK,pH1=1.22<pH2=4.19������K1=10-1.22>K2=10-4.19������ ֱ��I��X��ʾ����c(HC2O4��)/c(H2C2O4)��ֱ�ߢ���X��ʾ����c(C2O42��)/c(HC2O4��)����A��ȷ��
B��pH=0ʱ��lgc(HC2O4��)/c(H2C2O4)=lgK1=-1.22��lgc(C2O42��)/c(HC2O4��)=lgK2=-4.19�����ԣ�ֱ��I��II��б�ʾ�Ϊ1����B��ȷ��
C����pH=a,c(H��)=10-a,c(C2O42��)/c(HC2O4��)=K2/c(H��)=10a-4.19����c(C2O42��)<c(HC2O4��)ʱ��10a-4.19<1����a-4.19<0����ã�a<4.19��K1��K2=c(H��)c(HC2O4��)/c(H2C2O4)��c(H��)c(C2O42��)/c(HC2O4��)=c2(H��)c(C2O42��)/c(H2C2O4)����c(C2O42��)/c(H2C2O4)=K1��K2/c2(H��)=102a-5.41����c(C2O42��)>c(H2C2O4)ʱ��102a-5.41>1��2a-5.41>0�����a>2.705������c(HC2O4��)>c(C2O42��)>c(H2C2O4)��Ӧ2.705<pH<4.19����C����
D������غ㣺 c(Na+)+c(H��)=c(HC2O4��)+2c(C2O42��)+c(OH��)����c(Na+)=c(HC2O4��)+2c(C2O42��)ʱ��c(H��)=c(OH��)����ӦpH=7����D��ȷ��
��ѡC��


 һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
һŵ��ҵ�����ҵ���ּ�����������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʢ��������ڴ����ᡡ�۴������ ����ֱ��ʹ������ɫ������ɫ����(����)
A. ���� B. ���� C. ���ڢ� D. �٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͨ��һ����Ӧ����ֱ����ɵ���
��N2��NO2�� ��NO2��NO ��NH3��NO ��NO��HNO3�� ��Cu��Cu(NO3)2 ��HNO3��NO2
A. �٢�B. ��C. �٢ܢ�D. �٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ʵ��ԭ����ʵ���������ȷ����(����)

A. ��ͼ1��ʾװ����ȡ�����İ���
B. ��ͼ2װ�ÿ����������Ȫ��ʵ��
C. ��ͼ3��ʾװ���ռ�SO2
D. ���ü���Ũ��ˮ�ư���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����ݻ��̶�Ϊa L���ܱ������г���1 mol X�����2 mol Y���壬������ӦX(g)��2Y(g) ![]() 2Z(g)���˷�Ӧ�ﵽƽ��״̬�ı�־��(����)
2Z(g)���˷�Ӧ�ﵽƽ��״̬�ı�־��(����)
A. �����������ܶȲ���ʱ��仯 B. �����ڸ����ʵ�Ũ�Ȳ���ʱ��仯
C. ������X��Y��Z��Ũ��֮��Ϊ1��2��2 D. ��λʱ��������0.1 mol X��ͬʱ����0.2 mol Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�ɢϵ�У���ɢ����ֱ����С���ǣ� ��
A.������������B.��������Һ
C.ʯ����D.�������Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������(F)�����ڼ����ļ������������粫�������Ķ����٣��ϳ�·�����£�
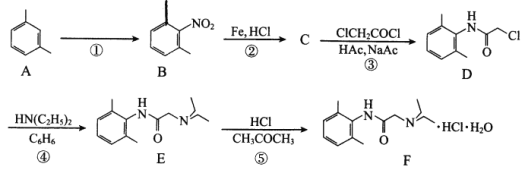
�ش��������⣺
��1��A�Ļ�ѧ����Ϊ_________��
��2����Ӧ�������Լ��������ֱ�Ϊ_________��_________��
��3��B��ͬ���칹������ܶ࣬��������������B��ͬ���칹�干��_________��(�����������칹)�����й����ŵ�������_________��
�����ڱ�������������Ϲ�������ȡ������
����̼��������Һ��Ӧ�ɷų�CO2���塣
��4��C�Ľṹ��ʽΪ_________��
��5���ڷ�Ӧ��~��������ȡ����Ӧ����_________��
��6��ClCH2COCl������NaOH��Һ���ȳ�ַ�Ӧ�Ļ�ѧ����ʽΪ_________��
��7��NH(C2H5)2�ں˴Ź�����������_________��壬�������Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ����Ǧ�����е�Ǧ������Na2CO3��NaHCO3��Һ����Ǧ�ࣨ��Ҫ�ɷ�PbSO4�����PbCO3��PbSO4(s) + CO32��(aq) ![]() PbCO3(s) + SO42��(aq) K = 2.2��105�� �������õ���PbCO3���պ���PbO��PbO�پ�һ��ת��ΪPb������˵����ȷ����
PbCO3(s) + SO42��(aq) K = 2.2��105�� �������õ���PbCO3���պ���PbO��PbO�پ�һ��ת��ΪPb������˵����ȷ����
A. PbSO4���ܽ��С��PbCO3
B. ����PbSO4��Na2CO3��NaHCO3��Һ��pH����
C. ���õ��������Ũ�ȵ�Na2CO3��NaHCO3��Һ�ֱ���PbSO4��Na2CO3��Һ�е�PbSO4ת���ʽϴ�
D. ���������漰һ�����ֽⷴӦ������������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ӹ����п�������1��8�ƶ�ϩ��![]() ���������й�����˵����ȷ���ǣ� ��
���������й�����˵����ȷ���ǣ� ��
A. ����ʽΪC10H14
B. ��������������ˮ������ijЩ�л��ܼ���ȡ1��8�ƶ�ϩ
C. �����Ը��������Һ����������ˮ�Ⱦ��ɷ���������Ӧ
D. ����һ��ͬ���칹��Ľṹ�п��ܺ��б���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com