
【题目】化合物G是一种医药中间体,由芳香化合物A制备G的一种合成路线如下:

回答下列问题:已知:①酯能被LiAlH4还原为醇
②
(1)A的化学名称_________________。
(2)C的结构简式_______________,由B生成C的反应类型_____________。
(3)由F生成G的反应方程式_____________________。
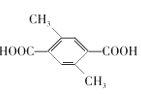
(4)芳香化合物X是C的同分异构体,1mol X与足量碳酸氢钠溶液反应生成88g CO2,其核磁共振氢谱显示有3种不同化学环境的氢,峰面积之比为3:1:1的有________种,写出1种符合要求的X的结构简式__________________。
(5)参照上述合成路线,写出用甲醇和苯甲醇为原料制备化合物 的合成路线__________。
的合成路线__________。
【答案】 (1)邻苯二甲酸 ![]() ; 取代反应
; 取代反应 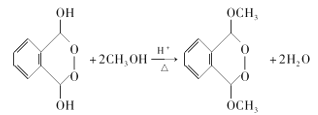 ;4
;4 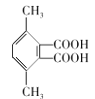 、
、 、
、 、
、 ;以上任写一种即可
;以上任写一种即可 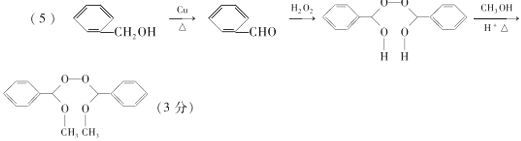
【解析】(1)根据机物B的结构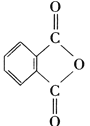 可知,A为邻苯二甲酸,脱去1分子水可得B;正确答案:邻苯二甲酸。
可知,A为邻苯二甲酸,脱去1分子水可得B;正确答案:邻苯二甲酸。
(2)根据信息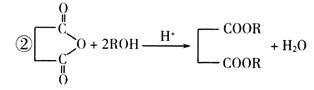 可知,有机物B与甲醇发生取代反应,生成有机物C,结构简式
可知,有机物B与甲醇发生取代反应,生成有机物C,结构简式![]() ;正确答案:
;正确答案:![]() ;取代反应。
;取代反应。
-CH2OH
(3)根据信息酯能被LiAlH4还原为醇,所以有机物D为![]() ;
;![]() 又被氧化为醛E,结构简式为
又被氧化为醛E,结构简式为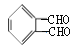 ;根据信息
;根据信息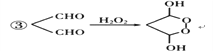 可知,有机物E在双氧水作用下变为有机物F,结构简式为
可知,有机物E在双氧水作用下变为有机物F,结构简式为 ;有机物F与甲醇在一定条件下发生取代反应生成有机物G,反应方程式:
;有机物F与甲醇在一定条件下发生取代反应生成有机物G,反应方程式: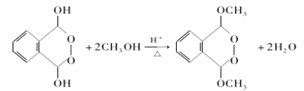 ;正确答案:
;正确答案: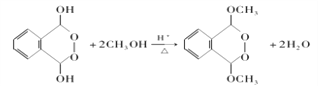 。
。
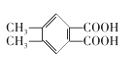
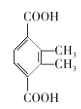
(4)有机物C为![]() ,芳香化合物X是C的同分异构体,1mol X与足量碳酸氢钠溶液反应生成88g CO2,含有2个羧基,其核磁共振氢谱显示有3种不同化学环境的氢,峰面积之比为3:1:1的4种,分别为:
,芳香化合物X是C的同分异构体,1mol X与足量碳酸氢钠溶液反应生成88g CO2,含有2个羧基,其核磁共振氢谱显示有3种不同化学环境的氢,峰面积之比为3:1:1的4种,分别为: 、
、 、
、 、
、 ;以上任写一种即可;正确答案:4;
;以上任写一种即可;正确答案:4; 、
、 、
、 、
、 ;以上任写一种即可。
;以上任写一种即可。
(5) 苯甲醇氧化为苯甲醛, 根据信息2可知:![]() 被过氧化氢氧化为
被过氧化氢氧化为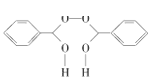 ;根据信息可知
;根据信息可知 与甲醇在酸性环境下,发生取代反应生成
与甲醇在酸性环境下,发生取代反应生成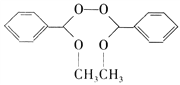 ;合成流程如下;
;合成流程如下;  ;正确答案:
;正确答案: 。
。


科目:高中化学 来源: 题型:
【题目】厨房垃圾发酵液可通过电渗析法处理,同时得到乳酸的原理如图所示(图中HA表示乳酸分子,A—表示乳酸根离子)。下列说法正确的是( )
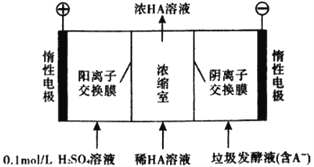
A. 通电后,阳极附近pH增大
B. 电子从负极经电解质溶液回到正极
C. 通电后,A—通过阴离子交换膜从阴极进入浓缩室
D. 当电路中通过2 mol电子的电量时,会有1 mol的O2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或表示方法正确的是( )
A.等质量的硫蒸气和硫磺分别完全燃烧,二者放出的热量一样多
B.氢气的燃烧热为285.8kJ/mol,则氢气燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=﹣285.8 kJ/mol
C.2H2(g)+O2(g)═2H2O(l)△H=﹣Q1 kJ/mol 2H2(g)+O2(g)═2H2O(g)△H=﹣Q2 kJ/mol,则Q1>Q2
D.已知中和热为57.3 kJ/mol,若将含0.5molH2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量等于57.3kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于放射性气体氡222 86Rn的说法正确的是 ( )
A. 质量数为222 B. 中子数为86
C. 质子数为136 D. 核电荷数为222
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】500mLKNO3和Cu(NO3)2的混合溶液中c(NO3﹣)=6.0molL﹣1 , 用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4L气体(标准状况),假定电解后溶液体积仍为500mL,下列说法正确的是( )
A.原混合溶液中c(K+)为2molL﹣1
B.上述电解过程中共转移2mol电子
C.电解得到铜的物质的量为0.5mol
D.电解后溶液中c(H+)为2molL﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒温恒容的密闭容器中,发生可逆反应2NO(g)+O2(g)![]() 2NO2(g),不能说明该反应已经达到平衡状态的是
2NO2(g),不能说明该反应已经达到平衡状态的是
A. 正反应生成NO2的速率和逆反应生成NO的速率相等
B. 反应容器中压强不随时间的延长而变化
C. 混合气体颜色深浅保持不变
D. 混合气体的密度不随时间延长而变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出基态镍原子的电子排布式______.与其同周期的基态原子的M 层电子全充满的元素位于周期表的_____区; 基态原子变成激发态原子产生的光谱叫_________光谱。
(2)丙酮( )分子中2号碳原子的杂化方式为____________;与CS2互为等电子体的阴离子是____(写一种);CO32-的立体构型是________。
)分子中2号碳原子的杂化方式为____________;与CS2互为等电子体的阴离子是____(写一种);CO32-的立体构型是________。
(3)含0.1mol[Cr(H2O)Cl]Cl2·H2O的水溶液与足量硝酸银溶液反应生成_____mol AgCl沉淀。H2O分子的键角比H2S分子的键角大,原因是_________。
(4)如图所示为GaAs的晶胞结构。

①一个镓原子周围所有距离最近且相等的砷原子形成的空间构型是______
②已知晶胞棱长a=5.64×10-10m.则该晶胞密度为ρ=_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E为原子序数依次增大的五种短周期元素,其中仅含有一种金属元素,A和D最外层电子数相同;B、C和E在周期表中相邻,且C、E同主族。B、C的最外层电子数之和等于D的原子核外电子数,A和C可形成两种常见的液态化合物。请回答下列问题:
(1)C、D、E三种原子对应的离子半径由大到小的顺序是________(填具体离子符号);由A、B、C三种元素按4∶2∶3组成的化合物所含的化学键类型属于_____。固体物质M由A和B以原子个数五比一组成的,所有原子的最外层都符合相应的稀有气体原子的最外层电子结构。该物质适当加热就分解成两种气体。则M 电子式为______,受热分解所得气体化学式是_______和_________。
(2)地壳中含量最高的金属元素的单质与D的最高价氧化物对应水化物的溶液反应,其离子方程式为____________________________。
(3)A、C两元素的单质与熔融K2CO3组成的燃料电池,其负极反应式为_______。
(4)可逆反应2EC2(气)+C2(气)![]() 2EC3(气)在两个密闭容器中进行,A容器中有一个可上下移动的活塞,B容器可保持恒容(如图所示),若在A、B中分别充入1 mol C2和2 mol EC2,使反应开始时的体积V(A)=V(B),在相同温度下反应,则达平衡所需时间:t(A)__________t(B)(填“>”、“<”、“=”或“无法确定”)。
2EC3(气)在两个密闭容器中进行,A容器中有一个可上下移动的活塞,B容器可保持恒容(如图所示),若在A、B中分别充入1 mol C2和2 mol EC2,使反应开始时的体积V(A)=V(B),在相同温度下反应,则达平衡所需时间:t(A)__________t(B)(填“>”、“<”、“=”或“无法确定”)。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com