
【题目】实验室制取乙酸乙酯的主要步骤如下:
①在甲试管(如图)中加入2mL浓硫酸、3mL乙醇和2mL乙酸的混合溶液.
②按下图连接好装置(装置气密性良好)并加入混合液,用小火均匀地加热3~5min。
③待试管乙收集到一定量产物后停止加热,撤出试管乙并用力振荡,然后静置待分层。
④分离出乙酸乙酯层、洗涤、干燥。
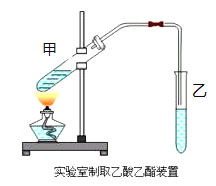
(1)写出制取乙酸乙酯的化学方程式:___________________________________。
(2)在反应未开始前,乙试管中所盛溶液为____________________。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】关于NaCl晶体的堆积方式的说法中正确的是 ( )
A. 可以看成是Na+按面心立方方式进行最密堆积,Cl-填在Na+形成的空隙中
B. 可以看成是Cl-按面心立方方式进行最密堆积,Na+填在Cl-形成的空隙中
C. 可以看成是Cl-按六方方式进行最密堆积,Na+填在Cl-形成的空隙中
D. 由于离子键有方向性和饱和性,NaCl晶体中的阴阳离子不服从紧密堆积原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了酯。在实验室也可以用如下图所示的装置制取乙酸乙酯,请回答下列问题。
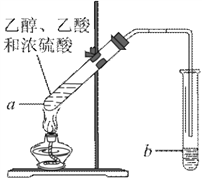
(1)乙酸分子中-COOH原子团的名称是_______。
(2)装置b中通蒸气的导管应置于饱和碳酸钠溶液的液面上而不能插入溶液中,目的是_________________。
(3)浓硫酸的作用是____________、____________。
(4)试管 a 中发生反应的化学方程式为_________________,反应类型是____________。
(5)反应时生成的乙酸乙酯密度比水________,可以闻到_______味。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.生铁和钢都属于合金
B.明矾可用作混凝剂去除水中的悬浮物
C.食盐水、稀豆浆、蔗糖水都能产生丁达尔效应
D.漂白液(有效成分为NaClO)可用于游泳池的消毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 A、B、C、D、E、F均为短周期主族元素,且原子序数依次增大,A是原子半径最小的元素,B的最高价氧化物的水化物可与其氢化物反应形成离子化合物甲;A与D可以按照原子个数比4:1形成化合物乙,且乙分子中含有18个电子,E与B同主族,C的阳离子与F的阴离子相差一个电子层,且可形成阳离子、阴离子个数比为2:1的离子化合物丙.
(1)B的气态氢化物的电子式为_____________,请用电子式表示A与C形成化合物的过程____________。
(2)E在周期表中的位置为______________________。
(3)下列说法正确的有_________。
①化合物乙分子中只含有极性共价键
②化合物甲和化合物丙都含有离子键和共价键
③B、E分别与A形成的简单化合物中,B的更稳定
④C、D、E、F原子半径由大到小的顺序为C>D>E>F
(4)写出由以上元素构成的10电子分子与18电子分子按物质的量之比1:1反应生成盐的化学方程式_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L的恒容密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
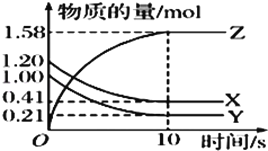
(1)该反应的化学方程式为_____。
(2)从反应开始到10s时,用Y表示的反应速率为________,X的转化率为_____。(均保留三位有效数字)
(3)10s时,该反应___达到了化学平衡状态。(填“是”或“否”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是一种具有香蕉气味的香精,实验室制备乙酸异戊酯的反应原理、装置示意图和有关数据如下:
【实验原理】

【装置与数据】


【查阅资料】分水器能将反应产生的水从反应体系中分离开来。乙酸乙酯可与无水CaCl2反应。
【实验步骤】
①酯化:在干燥的A中加入6.6异戊醇、9.0g冰醋酸、1.0mL浓硫酸,混匀后放入1~2粒沸石。按图组装好反应装置。检查装置气密性后,缓缓加热A,大约需要1h反应基本完成。
②洗涤:停止加热,冷却后将A中的反应液倒入分液漏斗中,用15mL冷水淋洗烧瓶内壁,洗涤液并入分液漏斗。充分振摇,接通大气静置,分层后分去水层。再用15mL冷水重复操作一次。然后酯层用20mL 5%碳酸氢钠溶液分两次洗涤。最后再用15mL饱和食盐水洗涤一次。
③干燥:将洗涤后的酯层倒入干燥的锥形瓶中,加入2g无水硫酸镁,配上塞子,充分振摇后,放置30min。
④蒸馏:将干燥好的粗酯蒸馏纯化,收集140~143 ℃馏分,得乙酸异戊酯5.2 g。
回答下列问题:
(1)仪器A的名称为 。球形冷凝管中冷凝水的进口是 (填“a”或“b”)。
(2)从化学平衡的角度分析分水器的作用是 。
(3)分液操作中,充分振荡静置分层后,酯层分离出来的方法是 。
(4)酯层用20mL 5%碳酸氢钠溶液洗涤的现象是 。
(5)干燥时加入的无水硫酸镁不能换成无水CaCl2,理由是 。
(6)本实验的产率为 。
(7)本实验中加入过量乙酸能提高醇的转化率,为何不加入过量的醇从而提高乙酸的转化率?其原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g)![]() 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别以下图和下表表示。

容器 | 甲 | 乙 | 丙 |
容积 | 1L | 1L | 2L |
温度/℃ | T1 | T2 | T2 |
反应物 起始量 | 1molA 2molB | 1molA 2molB | 4molA 8molB |
下列说法正确的是
A. 由图可知T1<T2,且该反应为吸热反应
B. 前10min内甲、乙、丙三个容器中反应的平均速率:v(A)乙<v(A)甲< v(A)丙
C. 平衡时A的转化率a:a乙<a甲<a丙
D. T1时该反应的平衡常数K=7.2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com