
实验室制得的乙炔中常混有H2S、PH3等杂质气体。如图是两学生设计的实验装置,用来测定CaC2样品的纯度,右边的反应装置相同而左边的气体发生装置则不同,分别如Ⅰ和Ⅱ所示。

(1)A瓶中的液体可以从酸性KMnO4溶液和FeCl3溶液中选择,应该选择________,它的作用是___________________________。
(2)装置Ⅰ的主要缺点是______________________________________。
(3)装置Ⅱ的主要缺点是_____________________;
若选用此装置来完成实验,则应采取的措施是___________________。
(4)若称取a g CaC2,反应完全后,测得B处溴水增重b g,则CaC2的纯度为________。
(1)FeCl3溶液 除去H2S、PH3等杂质气体
(2)部分乙炔会从长颈漏斗逸出,造成实验误差,且不易控制加水量
(3)反应产生的泡沫易堵塞导管 在装置的导管口加上一团棉花
(4) 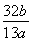 ×100%
×100%
【解析】A瓶中的液体是用来除去混在乙炔中的H2S、PH3,酸性KMnO4溶液会在除去H2S、PH3的同时也将C2H2氧化,故选用FeCl3溶液,装置Ⅰ和Ⅱ均可制乙炔,但装置Ⅰ的主要缺点为部分乙炔气体会从长颈漏斗口逸出,造成实验误差,且长颈漏斗也不易控制加水量。由于CaC2与水剧烈反应产生泡沫,故装置Ⅱ的缺点为泡沫易堵塞导管,可在装置的导管口加上一团棉花。实验时,B处溴水增加质量即为所吸收乙炔的质量,由题意则有:n(CaC2)=n(C2H2)=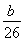 mol,m(CaC2)=
mol,m(CaC2)= mol×64 g/mol=
mol×64 g/mol= g,CaC2的纯度=
g,CaC2的纯度=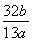 ×100%。
×100%。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014年高二人教版化学选修五 4-1 油脂练习卷(解析版) 题型:选择题
A、B两瓶液体,一瓶是植物油,一瓶是矿物油。现各取少量,放在两支洁净的试管里,加入NaOH溶液并加热,冷却后加水振荡静置,A出现泡沫,B无泡沫且分为两层。
由此可推出,A为________,B为________。
理由是___________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高二人教版化学选修五 1-3有机化合物的命名练习卷(解析版) 题型:选择题
“辛烷值”用来表示汽油的质量,汽油中异辛烷的爆震程度最小,将其辛烷值标定为100,如图是异辛烷的球棍模型,则异辛烷的系统命名为( )
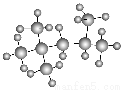
A.1,1,3,3-四甲基丁烷
B.2-甲基庚烷
C.2,4,4-三甲基戊烷
D.2,2,4-三甲基戊烷
查看答案和解析>>
科目:高中化学 来源:2014年高二人教版化学选修五 1-1有机化合物的分类练习卷(解析版) 题型:填空题
在下列化合物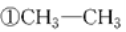
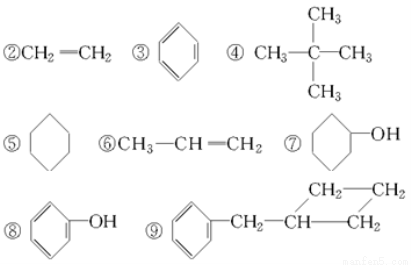 中
中
(1)属于环状化合物的有________,
(2)属于脂环化合物的有________,
(3)属于芳香化合物的有________,
(4)属于脂肪烃的有________。
查看答案和解析>>
科目:高中化学 来源:2014年高二人教化学选修五2-1-2脂肪烃炔烃脂肪烃来源及应用练习卷(解析版) 题型:选择题
含有一个三键的炔烃,氢化后的产物结构简式为:
 ,此炔烃可能的结构简式有( )
,此炔烃可能的结构简式有( )
A.1种 B.2种 C.3种 D.4种
查看答案和解析>>
科目:高中化学 来源:2014年高中化学创新训练上专题10常见非金属元素及其重要化合物练习卷(解析版) 题型:实验题
某化学兴趣小组的同学利用下图所示实验装置进行某些气体的制备、性质等实验(图中夹持装置有省略)。请按要求填空:
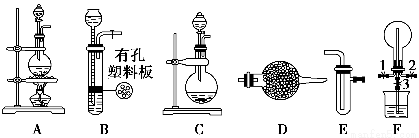
Ⅰ.探究氯气与氨气的反应
(1)为制取干燥氨气,可将装置C与________(填装置编号)连接;装置C中的烧瓶内固体宜选用________。
a.碱石灰 b.氯化钙 c.五氧化二磷 d.生石灰
(2)装置A、E、E连接可制取纯净、干燥的氯气,则两个E装置内的药品依次是________________。
(3)装置F可用于探究氯气与氨气(已知氯气与氨气可发生反应:3Cl2+2NH3=N2+6HCl)的反应。实验时打开弹簧夹1、3,关闭2,先向烧瓶中通入________,然后关闭1、3,打开2,向烧瓶中缓慢通入一定量的另一种气体。实验一段时间后烧瓶内出现浓厚的白烟并在容器内壁凝结,请设计一个实验方案鉴定该固体中的阳离子__________________________________________________________。
Ⅱ.探究某些物质的性质
(4)利用装置A、E,可设计实验比较Cl-和Br-的还原性强弱,能证明结论的实验现象是_______________________________________________________。
(5)若利用装置A、E进行乙烯与溴水反应的实验,写出反应的化学方程式_________________________________________________________________。
(6)将装置B、C分别与F相连后,进行H2S与SO2反应的实验。F的烧瓶中发生反应的化学方程式为______________________;F的烧杯所起的作用是_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上专题9常见金属元素及其重要化合物练习卷(解析版) 题型:选择题
下列推断正确的是 ( )。
事实结论
A常温下铁、铜均不溶于浓硫酸常温下铁、铜与浓硫酸均不反应
BHCl与Na2CO3溶液反应生成CO2可用饱和Na2CO3溶液除去CO2中的少量HCl
C氧化铜高温下生成红色物质,该物质可与稀硫酸反应氧化铜高温下可分解生成Cu2O
D稀、浓硝酸分别与铜反应,还原产物分别为NO和NO2稀硝酸氧化性比浓硝酸强
查看答案和解析>>
科目:高中化学 来源:2014年高中化学二轮创新训练上 专题6化学反应速率和化学平衡练习卷(解析版) 题型:填空题
25 ℃时,在体积为2 L的密闭容器中,气态A、B、C的物质的量n随时间t的变化如图1所示,已知达到平衡后,降低温度,A的转化率将增大。
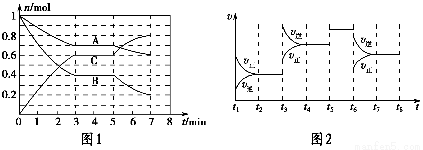
t2~t3 | t4~t5 | t5~t6 | t7~t8 |
K1 | K2 | K3 | K4 |
(1)根据图1数据,写出该反应的化学方程式:__________________。此反应的平衡常数表达式K=________,从反应开始到第一次平衡时的平均速率v(A)为________。
(2)在5~7 min内,若K值不变,则此处曲线变化的原因是________________。
(3)如图2表示此反应的反应速率v和时间t的关系图,各阶段的平衡常数如表所示。K1、K2、K3、K4之间的关系为________(用“>”、“<”或“=”连接)。A的转化率最大的一段时间是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com