

 4Al+3O2↑
4Al+3O2↑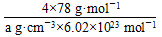
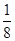 +6×
+6×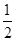 =4,F原子全部在该晶胞内部,故该晶胞含有F原子个数为8,其化学式为CaF2;取一个晶胞,其质量为
=4,F原子全部在该晶胞内部,故该晶胞含有F原子个数为8,其化学式为CaF2;取一个晶胞,其质量为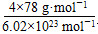 ,则其体积为质量除以密度,即
,则其体积为质量除以密度,即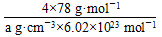 。
。

 备战中考寒假系列答案
备战中考寒假系列答案科目:高中化学 来源:不详 题型:单选题
| A.最外层只有1个电子的元素一定是金属元素 |
| B.最外层有2个电子的元素一定是金属元素 |
| C.原子核外各层电子数相等的元素一定是金属元素 |
| D.最外层电子数为7的原子,最高正价为+7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.第三、四周期同主族元素的原子序数相差8 |
| B.任何原子都是核外电子层数等于该元素在周期表中的周期数 |
| C.短周期中次外层电子数是最外层电子数2倍的元素一定是非金属元素 |
| D.短周期中族序数与周期数相同的元素是H、Be |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
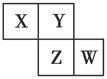
| A.原子半径:W>Z>Y>X |
| B.最高价氧化物对应水化物的酸性:Z>W>X |
| C.氢化物的稳定性:X>Y>Z |
| D.四种元素的单质中,Z单质的熔、沸点最高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.元素周期表中元素X位于元素Y的上一个周期 |
| B.元素X的含氧酸的酸性强于元素Y的含氧酸 |
| C.分别加热H2X、HY至500 ℃,只有HY发生分解 |
| D.元素X与Y同主族,相同温度时其单质与铜反应分别生成Cu2X和CuY |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:Y>Z>R>T |
| B.气态氢化物的稳定性:W<R<T |
| C.最高价氧化物对应的水化物碱性:X>Z |
| D.XR2、WR2两化合物中R的化合价相同 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.以共价键形成的单质中只存在非极性键,以共价键形成的化合物中只存在极性键 |
| B.NaCl和SiC晶体熔化时,克服粒子间作用力的类型相同 |
| C.PCl3和Na2O2中各原子或离子最外层都满足8电子稳定结构 |
| D.24Mg34S晶体中电子总数与中子总数之比为1∶1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com