
【题目】常用的电池是一个液体电解质将两个固体电极隔开。而钠-硫(Na/S8)电池正相反,它是由固体电解质将两个液体电极隔开(如图),一个由钠-β-氧化铝固体电解质做成的中心管,将内室的熔融钠(熔点98℃)和外室的熔融硫(熔点119℃)隔开,并允许Na+通过。下列有关说法不正确的是

A. a为电池的正极
B. 充电时b接电源的正极
C. 正极反应为:nS8+16ne-=8Sn2-
D. Na+可以穿过固体电解质从而传递电流
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A. 加水稀释0.01 mol·L-1的CH3COOH溶液,溶液中c(OH-)减小
B. 室温时,0.1 mol·L-1的某一元酸HA在水中有0.1%发生电离,则该溶液的pH=4
C. 氨水加水稀释后,溶液中![]() 的值增大
的值增大
D. 常温下,pH均为5的盐酸与氯化铵溶液中,水的电离程度相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叠氮酸钠(NaN3)是汽车安全气囊的产气剂,Fe2O3是主氧化剂,NaHCO3作冷却剂。当汽车发生剧烈碰撞时,分解产生大量气体使安全气囊迅速打开,从而起到安全保护作用[已知Ka(HN3)=1.8×10-5]。下列有关说法正确的是
A. NaHCO3的冷却原理是它发生分解,消耗体系的热量
B. Fe2O3和Na反应的氧化产物是Na2O2
C. 等物质的量的NaN3和HN3混合溶液显碱性
D. 若有6.5 gNaN3分解产生N2,则转移0.9 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为 MnO2 + 4HCl (浓)![]() MnCl2+ Cl2↑ +2H2O ,欲制得标准状况下4.48L氯气,
MnCl2+ Cl2↑ +2H2O ,欲制得标准状况下4.48L氯气,
(1)参加反应的HCl的质量是 __________ 克
(2)反应中实际被氧化的HCl的物质的量是__________ mol
(3)反应中转移的电子个数为 ______________ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧化钙晶体(CaO2·8H2O)常用作医药消毒剂,可以轻质碳酸钙为原料,按以下实验方法来制备。
![]()
下列有关说法正确的是
A. ①煮沸的主要目的是为了除去溶解的CO2
B. ②的反应中H2O2作氧化剂,氨水用来调节溶液的pH
C. ②中结晶的颗粒较小,过滤时可用玻璃棒轻轻搅动
D. ③醇洗的主要目的是为了减少晶体的损失
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2气体是安全、无毒的绿色消毒剂和保鲜剂,使用中不产生致癌物及二次污染物。某化学兴趣小组通过下图对其吸收、释放进行研究,请回答以下问题:
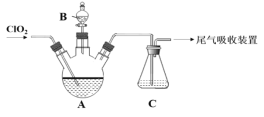
(1)用KClO3与Na2SO3在H2SO4酸化时制取ClO2,该反应的离子方程式为______。
(2)如图A中盛放有Na2CO3-H2O2混合溶液,常用于ClO2的吸收稳定剂。已知ClO2被稳定剂吸收生成NaClO2,若C中淀粉KI-H2SO4溶液变蓝,_____(填“能”或“不能”) 说明在仪器A中ClO2被完全吸收。
(3)已知ClO2的消毒能力是等物质的量Cl2的2.5倍,则ClO2在将含氰废液中的CN-氧化成CO2和N2的反应中,氧化剂和还原剂的物质的量之比为______。
(4)由B向A中滴加稀盐酸即可释放出ClO2,此时C的作用是_____。已知ClO2能被多种稳定剂所吸收,若将ClO2用于果蔬保鲜,图中吸收效果较好的稳定剂是___(填 “Ⅰ”或“Ⅱ”),原因是______。

(5)ClO2的“有效氯”可通过标定反应后溶液中的残氯[c(Cl-)]来测定。在分析化学中以K2CrO4为指示剂,用AgNO3标准溶液滴定溶液中的Cl-,当出现砖红色沉淀时,即指示达滴定终点。若保证溶液中c(Cl-)降为1.0×10-5 mol/L,则此时溶液中c(CrO42-)应不超过______mol/L。[Ksp(AgCl)=2.0×10-10,Ksp(Ag2CrO4)=2.0×10-12]。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.2 L由NaCl溶液、MgCl2溶液、CuCl2溶液组成的混合溶液中,部分离子的浓度如图所示。
(1)混合液中,NaCl的物质的量为_______mol,MgCl2的质量为_______g。
(2)该混合溶液中CuCl2的物质的量浓度为_____molL﹣1,将该混合溶液加水稀释至体积为1 L,稀释后溶液中Cu2+的物质的量浓度为_______molL﹣1。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A.常温常压下,22.4 L CCl4、CO2含有的分子数为1NA
B.常温常压下,1.06 g Na2CO3含有的Na+离子数为0.02NA
C.通常状况下,NA个CO2分子占有的体积约为22.4 L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油是一种重要的能源,通过石油分馏可得到重油,以重油为原料,可合成X:CH3COOCH=CH2。其中A是最简单的烯烃,B能发生银镜反应,D的相对分子质量比A小2。请回答下列有关问题:

(1)A中的官能团名称是___________________
(2)B→C的化学方程式_____________________________
(3)已知C与D发生加成反应生成X,其化学方程式为________________________
(4)下列说法正确的是_____
A.此处的“某工艺”指的是分馏 B.B在一定条件下能与氢气发生加成反应
C.X不溶于水,能使酸性高锰酸钾溶液褪色 D.可用溴的四氯化碳溶液鉴别A和D
(5)F是X的同分异构体,1molF能与4molAg(NH3)2OH反应,写出F可能的结构简式_____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com