
【题目】ClO2气体是安全、无毒的绿色消毒剂和保鲜剂,使用中不产生致癌物及二次污染物。某化学兴趣小组通过下图对其吸收、释放进行研究,请回答以下问题:
(1)用KClO3与Na2SO3在H2SO4酸化时制取ClO2,该反应的离子方程式为______。
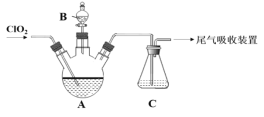
(2)如图A中盛放有Na2CO3-H2O2混合溶液,常用于ClO2的吸收稳定剂。已知ClO2被稳定剂吸收生成NaClO2,若C中淀粉KI-H2SO4溶液变蓝,_____(填“能”或“不能”) 说明在仪器A中ClO2被完全吸收。
(3)已知ClO2的消毒能力是等物质的量Cl2的2.5倍,则ClO2在将含氰废液中的CN-氧化成CO2和N2的反应中,氧化剂和还原剂的物质的量之比为______。
(4)由B向A中滴加稀盐酸即可释放出ClO2,此时C的作用是_____。已知ClO2能被多种稳定剂所吸收,若将ClO2用于果蔬保鲜,图中吸收效果较好的稳定剂是___(填 “Ⅰ”或“Ⅱ”),原因是______。

(5)ClO2的“有效氯”可通过标定反应后溶液中的残氯[c(Cl-)]来测定。在分析化学中以K2CrO4为指示剂,用AgNO3标准溶液滴定溶液中的Cl-,当出现砖红色沉淀时,即指示达滴定终点。若保证溶液中c(Cl-)降为1.0×10-5 mol/L,则此时溶液中c(CrO42-)应不超过______mol/L。[Ksp(AgCl)=2.0×10-10,Ksp(Ag2CrO4)=2.0×10-12]。
【答案】2ClO3-+SO32-+2H+= 2ClO2↑+SO42-+H2O 不能 1∶1 检验是否有ClO2生成 Ⅱ 缓慢释放出ClO2,且能长时间维持保鲜所需要的浓度 5.0×10-3
【解析】
(1) KClO3具有氧化性,Na2SO3具有还原性,二者在酸性条件下发生氧化还原反应,KClO3被还原为ClO2,SO32-被氧化为SO42-,根据电子守恒、电荷守恒及原子守恒,可得反应的离子方程式为2ClO3-+SO32-+2H+= 2ClO2↑+SO42-+H2O;
(2)H2O2不稳定,分解产生的O2也可以将KI氧化产生I2,I2遇淀粉溶液会变为蓝色,所以说明在仪器A中ClO2被完全吸收;
(3)ClO2在将含氰废液中的CN-氧化成CO2和N2,它被还原为Cl-,反应的离子方程式为2CN-+2ClO2=2CO2↑+N2↑+2Cl-,可见氧化剂和还原剂的物质的量之比为1:1;
(4)A中ClO2被稳定剂吸收转化为NaClO2,由B向A中滴加稀盐酸即可释放出ClO2,此时C的作用是检验是否有ClO2生成;若将ClO2用于果蔬保鲜,要求稳定剂缓慢释放出ClO2气体,且能长时间维持保鲜所需要的浓度,这样保鲜期才可以延长,根据图示可知稳定剂II相对效果更好;
(5)c(Ag+)c(Cl-)> Ksp(AgCl)=2.0×10-10,c(Ag+)<2.0×10-10÷1.0×10-5=2.0×10-5mol/L,c2(Ag+) c(CrO42-)>Ksp(Ag2CrO4)=2.0×10-12,c(CrO42-)<2.0×10-12÷(2.0×10-5)2=5.0×10-3mol/L,即此时溶液中c(CrO42-)应不超过5.0×10-3mol/L。


科目:高中化学 来源: 题型:
【题目】【题目】已知:①H2(g)+ ![]() O2(g)=2H2O(g) △H1=akJ/mol
O2(g)=2H2O(g) △H1=akJ/mol
②2H2(g)+O2(g)=2H2O(g) △H2=b kJ/mol
③H2(g)+ ![]() O2(g)=H2O(l) △H3=ckJ/mol;
O2(g)=H2O(l) △H3=ckJ/mol;
④2H2(g)+O2(g)=2H2O(l) △H4=dkJ/mol。
下列关系正确的是
A. a<c<0 B. b>d>0 C. 2a=b<0 D. 2c=d>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】SO2 是危害最为严重的大气污染物之一,SO2 的含量是衡量大气污染的一个重要指标。工业上常采用催化还原法或吸收法处理 SO2。催化还原 SO2 不仅可以消除 SO2 污染,而且可得到有价值的单质S。
(1)在复合组分催化剂作用下,CH4 可使 SO2 转化为 S,同时生成 CO2 和 H2O。已知 CH4 和 S的燃烧热分别为 890.3 kJ /mol 和 297.2 kJ /mol , CH4 和 SO2 反应的热化学方程式为__________。
(2)用 H2 还原 SO2 生成S 的反应分两步完成,如图 1 所示,该过程中相关物质的物质的量浓度随时间的 变化关系如图 2 所示:

①分析可知X 为______写化学式),0~t1 时间段的温度为_____,0~t1 时间段用SO2 表示的化学反应速率为_____。
②总反应的化学方程式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知苯乙烯的结构为![]() 。有关该物质的下列说法正确的是( )
。有关该物质的下列说法正确的是( )
A. 该物质在一定条件下和氢气完全加成,加成产物的一溴取代物 6 种
B. 该物质能使溴水和酸性高锰酸钾溶液褪色,褪色原理完全相同
C. 苯乙烯分子的所有原子不可能在同一平面上
D. 除去乙苯中混有的苯乙烯可以通入等量氢气反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常用的电池是一个液体电解质将两个固体电极隔开。而钠-硫(Na/S8)电池正相反,它是由固体电解质将两个液体电极隔开(如图),一个由钠-β-氧化铝固体电解质做成的中心管,将内室的熔融钠(熔点98℃)和外室的熔融硫(熔点119℃)隔开,并允许Na+通过。下列有关说法不正确的是

A. a为电池的正极
B. 充电时b接电源的正极
C. 正极反应为:nS8+16ne-=8Sn2-
D. Na+可以穿过固体电解质从而传递电流
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】结合图回答问题:
(1)学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容如图Ⅰ,现欲用此硫酸配制配制成浓度为0.50molL﹣1的稀硫酸100mL.①所需玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管外还需________。
②所取浓硫酸的体积为________ mL。
(2)写出上述装置中仪器的名称:②________;③________。
(3)若利用装置Ⅱ分离乙酸(沸点118℃)和乙酸乙酯(沸点77.1℃)的混合物,还缺少的仪器有________,将仪器补充完整后进行的实验操作的名称为________。
(4)实验室常用装置Ⅲ分离碘水中的碘, 进行该操作时,需在碘水中加一试剂,在选择试剂时,下列性质你认为哪些性质是必需的:________(填序号)。①常温下为液态 ②I2在其中溶解程度大 ③与水互不相容 ④密度要比水大。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列电离方程式书写正确的是( )
A.把CaCl2放入水中:CaCl2===Cu2++Cl2-
B.把NaHSO4放入水中:NaHSO4===Na++H++SO![]()
C.把Ba(OH)2放入水中:Ba(OH)2=== Ba 2++(OH)2-
D.把H2SO4放入水中:H2SO4=== H2++SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图中A~J均为有机化合物,根据图中的信息,回答下列问题。
已知:分子中含有两个碳碳双键,且两个双键之间有一个碳碳单键的烯烃与单烯烃可发生反应:
(1)环状化合物A的相对分子质量为82,其中含碳87.80%,含氢12.2%。B的一氯代物仅有一种,B的结构简式为_______________________。
(2)M是B的一种同分异构体,M能使溴的四氯化碳溶液褪色,分子中所有的碳原子共平面,则M的结构简式为__________________________________。
(3)由E和A反应生成F的化学方程式为___________________________________。
(4)D中含有的官能团是________,由H生成I的反应类型是______________
(5)已知:R-COOH+NaOH→R-COONa+H2O,G的分子式为C6H10O4,0.146gG需用20mL0.100mol·L-1 NaOH溶液完全中和,G的结构简式为______________________;
(6)![]() 为重要的化工原料,根据题中信息,设计以1,3-丁二烯为原料合成
为重要的化工原料,根据题中信息,设计以1,3-丁二烯为原料合成![]() 的合成路线_____________________________(以流程图形式表示,无机试剂任选)。
的合成路线_____________________________(以流程图形式表示,无机试剂任选)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com