
【题目】 MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如下图所示。下列叙述中不正确的是: ( ) 
A.ROH是一种强碱
B.在x点,MOH并没有完全电离
C.在x点,c(M+)=c(R+)
D.稀释前,c(ROH)=10c(MOH)
【答案】D
【解析】解:pH=13的ROH稀释100倍,pH变为11,所以ROH为强碱,故A正确,故A不符合题意;pH=12的MOH稀释100倍,pH变为11,所以MOH为弱碱,在x点,MOH未完全电离,故B正确,故B不符合题意;根据电荷守恒,c(M+)+c(H+)=c(OH-) 、c(R+)+c(H+)=c(OH-) ,在x点,两溶液中氢离子、氢氧根离子浓度均相等,所以c(M+)=c(R+),故C正确,故C不符合题意;MOH为弱碱、ROH为强碱,稀释前,c(ROH)<10c(MOH),故D错误,故D符合题意。
所以答案是D
有图分析ROH稀释倍数与OH-降低倍数一致,说明ROH完全电离,是强碱;而MOH稀释时电离的OH-降低倍数比碱降低倍数要小,说明MOH是部分电离,是弱电解质。A.ROH完全电离,是强碱B.MOH是部分电离,是弱电解质C.在x点,两溶液中氢离子、氢氧根离子浓度均相等D.MOH是部分电离,所以碱浓度大于OH-浓度
【考点精析】利用强电解质和弱电解质的概念和判断和弱电解质在水溶液中的电离平衡对题目进行判断即可得到答案,需要熟知强电解质:离子键、强极性键、完全电离;弱电解质:极性键、部分电离;当弱电解质分子离解成离子的速率等于结合成分子的速率时,弱电解质的电离就处于电离平衡状态;电离平衡是化学平衡的一种,同样具有化学平衡的特征.条件改变时平衡移动的规律符合勒沙特列原理.


科目:高中化学 来源: 题型:
【题目】俄罗斯科学家最近合成第114号元素的原子,该原子的质量数为289,存在时间达到30秒,这项成果具有重要意义。该原子的中子数与电子数之差是( )
A.61B.114C.175D.289
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将9.4克的铜铝合金,投入到足量的稀硫酸中充分反应后,共收集到标准状况下氢气6.72升,计算:
(1)参加反应的H2SO4的物质的量;
(2)合金中金属铜的质量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】埋在地下的输油铸铁管道,在下列各种情况下被腐蚀速度最慢的是( )
A.在含铁元素较多的酸性土壤中
B.在潮湿疏松透气的土壤中
C.在干燥致密不透气的土壤中
D.在含碳粒较多、潮湿透气的土壤中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示,装置Ⅰ为甲醇燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜。
(1)b处应通入(填“CH3OH”或“O2”),a处电极上发生的电极反应式是;
(2)电镀结束后,装置Ⅰ中溶液的pH(填写“变大”“变小”或“不变”,下同),装置Ⅱ中Cu2+的物质的量浓度;
(3)若铜电极质量减小6.4 g,则消耗标况下的O2的体积为。
(4)若将装置I中电解质溶液换成硫酸溶液,则在工作过程中H+ 移向电极(填“a”或“b”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,容器内某一反应aN![]() bM 的物质的量随反应时间变化的曲线如下图所示,下列表述中正确的是
bM 的物质的量随反应时间变化的曲线如下图所示,下列表述中正确的是
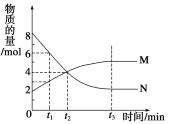
A. a∶b= 1∶2
B. t2时,逆反应速率大于正反应速率
C. t3时,正、逆反应速率相等,达到平衡
D. t1时,v(N)的反应速率是 2/ t1 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列空白。
(1)“辛烷值”用来表示汽油的质量,汽油中异辛烷的爆震程度最小,将其辛烷值标定为100,右图是异辛烷的球棍模型,则异辛烷的系统命名为。
(2)写出下列反应的化学方程式
① 2,5-二甲基-2,4-己二烯与足量氢气加成:
② 2-甲基-2-丁烯加聚反应
③ 甲苯在一定条件下生成三硝基甲苯:
(3)烯烃与溴化氢、水加成时,产物有主次之分,例如:
CH2=CHCH3 + HBr → CH3CHBrCH3 + CH3CH2CH2Br
(主要产物) (次要产物)
A是一种不对称烯烃,与HBr加成时,生成的主要产物为B,且B中仅含有4个碳原子、1个溴原子、1种氢原子。则B的结构简式为 , A的结构简式
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() (x)、
(x)、![]() (y)、
(y)、![]() (z) 互为同分异构体,下列说法不正确的是( )
(z) 互为同分异构体,下列说法不正确的是( )
A. Z的二氯代物只有三种
B. x、y、z中只有x的所有原子可能处于同一平面
C. x的同分异构体只有y和z两种
D. x、y可使溴的四氯化碳溶液因发生加成反应而褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com