
����Ŀ����ѧ��Ӧ���ʺ���������������������ء�
��1��ijѧ��Ϊ��̽��п�����ᷴӦ�����е����ʱ仯����400mLϡ�����м���������п�ۣ�����ˮ�������ռ���Ӧ�ų���������ʵ���¼���(�ۼ�ֵ)��
ʱ��(min) | 1 | 2 | 3 | 4 | 5 |
�������(mL)(��״��) | 100 | 240 | 464 | 576 | 620 |
����һʱ��η�Ӧ�������___min(��0~1��1~2��2~3��3~4��4~5)��ԭ����____��
����3~4����ʱ����������Ũ�ȱ仯����ʾ�ĸ÷�Ӧ����___(����Һ�������)��
��2����һѧ��Ϊ���Ʒ�Ӧ���ʷ�ֹ��Ӧ�������Բ�������������������������м���������������Һ�Լ�����Ӧ���ʣ�����Ϊ�����е�����________��
A.����ˮ
B.KCl��Һ
C.KNO3��Һ
D.CuSO4��Һ
��3��ij�¶�����4L�ܱ������У�X��Y��Z������̬���ʵ����ʵ�����ʱ��仯������ͼ��
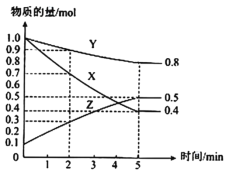
�ٸ÷�Ӧ�Ļ�ѧ����ʽ��___��
�ڸ÷�Ӧ�ﵽƽ��״̬�ı�־��___��
A.X��Y��Z�ķ�Ӧ�������
B.X��Y�ķ�Ӧ���ʱ�Ϊ3��1
C.����������ѹǿ���ֲ���
D.����1molY��ͬʱ����2molZ
��2min��X��ת����Ϊ___��
���𰸡�2~3min ��÷�Ӧ�Ƿ��ȷ�Ӧ����ʱ�¶ȸ�������Ũ�Ƚϴ����Է�Ӧ���ʽϿ� 0.025mol/(L��min) CD 3X(g)+Y(g)![]() 2Z(g) CD 30%
2Z(g) CD 30%
��������
(1)����ͬ�����£���Ӧ����Խ����ͬʱ�����ռ�������Խ�ࣻ�ɱ������ݿ�֪����Ӧ��������ʱ�����2��3 min����Ϊ��Ӧ�Ƿ��ȷ�Ӧ����ʱ�¶ȸ�������Ũ�Ƚϴ����Է�Ӧ���ʽϿ죻�ʴ�Ϊ��2~3min����÷�Ӧ�Ƿ��ȷ�Ӧ����ʱ�¶ȸ�������Ũ�Ƚϴ����Է�Ӧ���ʽϿ죻
��3��4����ʱ��Σ��ռ����������=(576-464)mL=112mL��n(H2)=![]() =0.005mol������������HCl��ϵʽ�����ĵ�n(HCl)=2n(H2)=2��0.005mol=0.01mol����v(HCl)=
=0.005mol������������HCl��ϵʽ�����ĵ�n(HCl)=2n(H2)=2��0.005mol=0.01mol����v(HCl)=![]() =0.025 mol/(Lmin)���ʴ�Ϊ��0.025mol/(L��min)��
=0.025 mol/(Lmin)���ʴ�Ϊ��0.025mol/(L��min)��
��2��A����������ˮ��������Ũ�ȼ�С����Ӧ���ʽ��ͣ���A���У�
B������KCl��Һ��������Ũ�Ƚ��ͣ���Ӧ���ʽ��ͣ���B���У�
C������KNO3��Һ���൱�ں������ᣬ�����Zn��Ӧ����NO��������������C�����У�
D������CuSO4��Һ��Zn��ͭ���ӷ�Ӧ����Cu��Zn��Cu��ϡ���ṹ��ԭ��ض��ӿ췴Ӧ���ʣ���D�����У��ʴ�Ϊ��CD��
��3���ٸ���ͼ֪�����ŷ�Ӧ���У�X��Y�����ʵ������ٶ�Z�����ʵ������ӣ���X��Y�Ƿ�Ӧ���Z���������Ӧ�ﵽƽ��ʱ����n(X)=(1.0-0.4)mol=0.6mol����n(Y)=(1.0-0.8)mol=0.2mol����n(Z)=(0.5-0.1)mol=0.4mol��ͬһ���淴Ӧ��ͬһ��ʱ���ڲμӷ�Ӧ�ĸ����ʵ����ʵ����仯��֮�ȵ��ڻ�ѧ������֮�ȣ�X��Y��Z�Ļ�ѧ������֮��=0.6mol��0.2mol��0.4mol=3��1��2����÷�Ӧ����ʽΪ3X(g)+Y(g)2Z(g)���ʴ�Ϊ��3X(g)+Y(g)![]() 2Z(g)��
2Z(g)��
��A���ò�ͬ���ʱ�ʾ���������棩��Ӧ����֮��ʼ�յ��ڻ�ѧ������֮�ȣ��ﵽƽ��ʱ�ò�ͬ���ʱ�ʾ�������淴Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ���A��ѡ��
B�����ŷ�Ӧ�Ľ��У�X��Y�ķ�Ӧ���ʱ�ʼ��Ϊ3��1��������Ϊƽ��״̬�ı�־����B��ѡ��
C���÷�Ӧǰ������ϵ��֮�Ͳ���ȣ�����δƽ��ʱ����������ʵ�����䣬�����ݻ��㶨������ѹǿ��䣬������������ѹǿ���ֲ���ʱ����Ӧ�ﵽƽ��״̬����Cѡ��
D������1molY��ͬʱ����2molZ������1molY�����淴Ӧ������ȣ���Ӧ�ﵽƽ��״̬����Dѡ��
�ʴ�Ϊ��CD��
��2min��Xת��1.0mol-0.7mol=0.3mol����X��ת����Ϊ![]() ��100%=30%��
��100%=30%��
�ʴ�Ϊ��30%��


 ��ڽ��ȫ������ϵ�д�
��ڽ��ȫ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������;�㷺�Ļ���ԭ�ϣ�������ˮ������ˮ�����������ʹ����ȡ�
��1����ҵ������ͭ�ķ����ܶࡣ
�ٷ���һ����Ũ�����ͭ��ȡ����ͭ���÷�Ӧ�Ļ�ѧ����ʽ��_______��
�ڷ���������ϡ���ᡢͭ����������ȡ����ͭ����������Ҫ��������ͼ��ʾ��
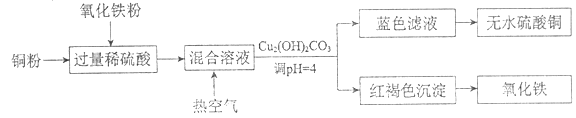
ϡ�������������Ӧ�����ӷ���ʽ��_________��ͭ��������Ӧ�õ������ʷ�Ӧ�����ӷ���ʽ��_________��������Һ��ͨ���ȿ����ķ�Ӧ�����ӷ���ʽ��_________��������ɫ��Һ�ͺ��ɫ������ʵ�������_________��
��2���������������������Ṥҵβ���еĶ�������ͬʱ�Ƶ�����李���Ҫ�Ĺ�����������ͼ��ʾ��
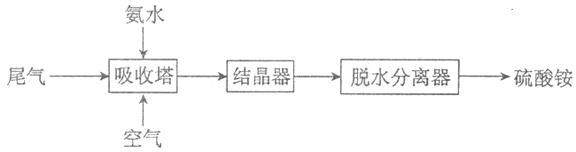
���������з�����Ӧ�Ļ�ѧ����ʽ��_________��
�ڼ���������е�NH4+�����ӷ���ʽ��_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����13�֣�����ͭ����(CuSO4��5H2O)��ͭ������Ҫ��������ԭ�ϣ��㷺Ӧ����ũҵ����ơ��������Ӽ���������ʯ�͡�ѡ���������ҵ��
���ÿ�ȸʯ[��Ҫ�ɷ�CuCO3��Cu(OH)2]�����ᣨ70%������ˮΪԭ����ȡ����ͭ���塣�乤���������£�
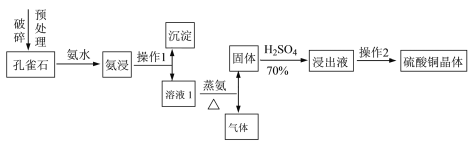
��1��Ԥ����ʱҪ�����������ȸʯ���������ֱ��<1 mm�������Ŀ����____________________��
��2����֪����ʱ�����ķ�ӦΪCuCO3��Cu(OH)2+8NH3��H2O![]() [Cu(NH3)4]2(OH)2CO3+8H2O������ʱ�õ��Ĺ���ʺ�ɫ����д������ʱ�ķ�Ӧ����ʽ��______________________��
[Cu(NH3)4]2(OH)2CO3+8H2O������ʱ�õ��Ĺ���ʺ�ɫ����д������ʱ�ķ�Ӧ����ʽ��______________________��
��3��������������������Ⱦ����Ҫ������������ͼװ���к��ʵ�Ϊ___________�����ţ��������վ������õ���Һ��;��_______________����дһ������

��4������2Ϊһϵ�еIJ�����ͨ������Ũ������ȴ�ᾧ��___________��ϴ�ӡ�___________�Ȳ����õ�����ͭ���塣
���ý���ͭ�����Ʊ�����ͭ����
��5���̲����ý���ͭ������Ũ���ᷴӦ�Ʊ�����ͭ����Ȼ�������ռ�࣬����ʵ�����������в����ã���ԭ����______________________����д��������
��6��ij��ȤС��������ϵ�֪��Cu+CuCl2![]() 2CuCl��4CuCl+O2+2H2O
2CuCl��4CuCl+O2+2H2O![]() 2[Cu(OH)2��CuCl2]��[Cu(OH)2��CuCl2]+H2SO4
2[Cu(OH)2��CuCl2]��[Cu(OH)2��CuCl2]+H2SO4![]() CuSO4+CuCl2+2H2O�����������ʵ�����Ʊ�����ͭ���壬װ����ͼ��
CuSO4+CuCl2+2H2O�����������ʵ�����Ʊ�����ͭ���壬װ����ͼ��
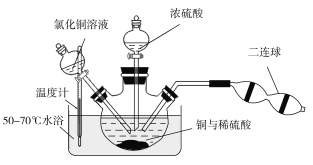
��ͭ��ϡ����Ļ�����м����Ȼ�ͭ��Һ�����ö���������������ͭ�ܽ⣬��������ƿ�г���״����Һʱ���μ�Ũ���ᡣ
��ʢװŨ�������������Ϊ___________��
��װ���м���CuCl2��������______________�������������ؽᾧ�ķ�����������ͭ�����ԭ��Ϊ______________________��
������ʼʱ����a gͭ�ۣ���b g�Ȼ�ͭ���ʵ��Ȼ�ͭ��Һ������Ƶ�c g CuSO4��5H2O�������������������ʲ����뷴Ӧ�Ҳ��ᾧ��ÿ����Ӧ�����еñȽ���ȫ����ԭͭ�۵Ĵ���Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��DΪԭ�������������������Ԫ�أ�A2-��B+������ͬ�ĵ��ӹ��ͣ� C��DΪͬ����Ԫ�أ�C��������������������������3����DԪ���������һ��δ�ɶԵ��ӡ��ش��������⣺
��1������Ԫ���е縺��������___________����Ԫ�ط��ţ�������Cԭ�ӵĺ�������Ų�ʽΪ__________��
��2������A������ͬ�������壬���зе�ߵ���____________�������ʽ����A��B���⻯�������ľ������ͷֱ�Ϊ___________��___________��
��3��C��D��Ӧ��������ɱ�Ϊ1��3�Ļ�����E��E�����幹��Ϊ____________������ԭ�ӵ��ӻ��������Ϊ________________��
��4������D��ʪ���Na2CO3��Ӧ���Ʊ�D2A���仯ѧ����ʽΪ______________��
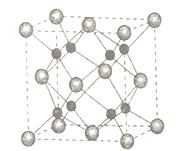
��5��A��B�ܹ��γɻ�����F���侧���ṹ��ͼ��ʾ����������a=0.566nm��F�Ļ�ѧʽΪ________��������Aԭ�ӵ���λ��Ϊ____________����ʽ���㾧��F���ܶȣ�g cm-3 ��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ݻ�������ܱ������д������·�Ӧ��2SO2(g)��O2(g) ![]() 2SO3(g) ��H����QkJ��mol��1(Q>0)��ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ����
2SO3(g) ��H����QkJ��mol��1(Q>0)��ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬���з�����ȷ����
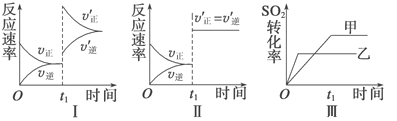
A. ͼ���о�����t0ʱ������O2��Ũ�ȶԷ�Ӧ���ʵ�Ӱ��
B. ͼ���о�����t0ʱ�̼��������Է�Ӧ���ʵ�Ӱ��
C. ͼ���о����Ǵ�����ƽ���Ӱ�죬�ҼĴ�Ч�ʱ��Ҹ�
D. ͼ���о������¶ȶԻ�ѧƽ���Ӱ�죬���ҵ��¶Ƚϵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ����ϡ������п��ȡ������ʵ���У����ּ�����������ͭ��Һ�ɼӿ��������������ʡ�
Ϊ�˽�һ���о�����ͭ�������������������ʵ�Ӱ�죬��ͬѧ���������һϵ��ʵ�顣�����������Ļ����Һ�ֱ���뵽6��ʢ�й���Zn���ķ�Ӧƿ�У��ռ����������壬��¼�����ͬ�������������ʱ�䡣����������Һ��������ڻ��ǰ����Һ�����֮�ͣ�
ʵ�� �����Һ | A | B | C | D | E | F |
4mol/LH2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
����CuSO4��Һ/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
��ش��������⣺
������ɴ�ʵ����ƣ����У�V3=___��V8=___��
�ڸ�ͬѧ���ó��Ľ���Ϊ������������CuSO4��Һʱ���������������ʻ�����ߡ����������CuSO4��Һ����һ����ʱ���������������ʷ������½���������������������½�����Ҫԭ��___��
��ʵ��A��ã��ռ�������H2���Ϊ112mL����״���£�ʱ�����ʱ��Ϊ10���ӣ���ѧ��Ӧ������(H2SO4)=___�����Է�Ӧǰ����Һ����仯����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1.5L���ܱ�������ͨ��2molX2��3molY2�Ļ�����壬��һ�������·�����Ӧ:X2(g)+3Y2(g) ![]() 2Z(g) +4W(?) ��H<0�ﵽƽ��ʱ��������ѹǿΪ��Ӧ��ʼʱ��0.8����ͬ�¶��²�������
2Z(g) +4W(?) ��H<0�ﵽƽ��ʱ��������ѹǿΪ��Ӧ��ʼʱ��0.8����ͬ�¶��²�������
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ��ֵΪ_______
��2��Ϊ���X2��ƽ��ת���ʣ����д�ʩ���е���___________
a.����ϵ����ͨ��һ������X2
b.����
c.�Ƴ�����Z
d.�ٳ���һ����Ar e.�����������
��3����Ӧ��ƽ���t1ʱ�̸ı�������������ʱ��仯��ͼ��ʾ����t1��Ӧ�����ı�Ϊ_______

a. ����
b. ����ϵ����ͨ��һ������W
c. ���߲���X2��Y2
d.�����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����298 Kʱ��1 mol C2H5OH����������ȫȼ�����ɶ�����̼��Һ̬ˮ�ų�����1366.8 kJ��
��1��д���÷�Ӧ���Ȼ�ѧ����ʽ��________________________________________��
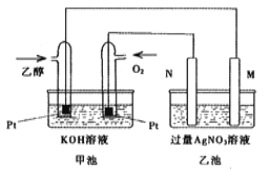
��2����ͼ���˷�Ӧ���Ϊԭ��أ��ҳ��е������缫һ����ʯī�缫��һ�������缫������ʱM��N�����缫�������������٣��ҳ����ܷ�Ӧ�Ļ�ѧ����ʽΪ��_________________��һ��ʱ�����ҳ���ijһ�缫��������4.32gʱ�������ϼ׳������������Ϊ����״����__________mL��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڻ�����2������ϩ��![]() ��������˵����ȷ����
��������˵����ȷ����
A. ����ʹϡ���������Һ��ɫ
B. ���Է����ӳɾۺϷ�Ӧ
C. ����������ԭ�ӹ�ƽ��
D. ������ˮ���ױ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com