
【题目】化合物YX2、ZX2中X、Y、Z都是前三周期元素,X与Y同周期,Y与Z同主族,Y元素的最外层p轨道上的电子数等于前一电子层电子总数;X原子最外层的p轨道中有一个轨道填充了2个电子。则
(1)X元素基态原子的电子排布式是__________________,Y原子的价层电子的电子排布图是_______________________。
(2)YX2的分子构型是____________。
(3)YX2分子中,Y原子的杂化类型是__________,一个YX2分子中含________个π键。
科目:高中化学 来源: 题型:
【题目】下列过程中,涉及化学变化的是
A. 四氣化碳萃取碘水中的碘 B. 生石灰被用作干燥剂后失效
C. 过滤除去粗盐中的不溶性杂质 D. 蒸馏法将海水淡化为饮用水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纯净的过氧化钙(CaO2)是白色粉末,难溶于水,不溶于乙醇、乙醚,常温下较为稳定,是一种新型水产养殖增氧剂,常用于鲜活水产品的运输.已知:在实验室可用钙盐制取CaO28H2O,再经脱水制得CaO2 . 其制备过程如下: 
(1)“溶解”过程需要的玻璃仪器有;“沉淀”时需控制反应温度在0℃左右,比较简单易行的方法是;为检验“水洗”是否合格,可取少量洗涤液于试管中,再滴加(填试剂),无明显现象说明“水洗”合格.
(2)“沉淀”时发生反应的离子方程式为;该制法的副产品为(填化学式);若称取11.1g无水CaCl2 , 理论上应该量取质量分数30%、密度1.1g/cm3的H2O2溶液mL.
(3)测定产品中CaO2的含量的实验步骤是: 第一步,准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2mol/L的H2SO4溶液,充分反应;
第二步,向上述锥形瓶中加入几滴淀粉溶液;
第三步,逐滴加入浓度为c mol/L的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL.【已知:I2+2S2O32﹣→2I﹣+S4O62﹣(无色)】
①第三步中说明反应恰好完全的现象是 .
②CaO2的质量分数为(用字母表示);
③某同学第一步和第二步的操作都很规范,第三步滴速太慢,这样测得的CaO2的质量分数可能(填“偏高”、“偏低”、“无影响”、“不能确定”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中甲曲线表示在最适温度下,某种酶促反应速率与反应物浓度之间的关系。其余两条曲线分别表示该酶促反应的反应速率受温度和pH的影响情况。回答下列问题:

(1)甲曲线中,若在A点适当提高温度,反应速率将会_____________________;在B点适当增加酶的浓度,反应速率将会__________________。
(2)丙曲线中,H点代表该酶的_____________________。
(3)若想要短期保存该酶,应选择曲线中的________点所对应的温度。
(4)探究温度对酶活性的影响时,通常选择_________________________(填“淀粉酶”或“过氧化氢酶”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)CH![]() 、CH3、CH
、CH3、CH![]() 都是重要的有机反应中间体,它们的电子式分别是________、________、________;其中CH
都是重要的有机反应中间体,它们的电子式分别是________、________、________;其中CH![]() 中四个原子是共平面的,三个键角相等,则键角应是________。
中四个原子是共平面的,三个键角相等,则键角应是________。
(2)叠氮化合物在化学工业上有重要应用。N![]() 叫做叠氮离子,请写出3种由三个原子构成的含有与N
叫做叠氮离子,请写出3种由三个原子构成的含有与N![]() 的电子数相同的粒子的化学式__________、__________、__________。
的电子数相同的粒子的化学式__________、__________、__________。
(3)N≡N键的键能为946 kJ/mol,N—N键的键能为193 kJ/mol,说明N2中的________键比________键稳定(填“σ”或“π”)
(4)CaC2中C![]() 与O
与O![]() 互为等电子体,O
互为等电子体,O![]() 的电子式可表示为________________;1 mol O
的电子式可表示为________________;1 mol O![]() 中含有的π键数目为________。
中含有的π键数目为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】制备氯化物时,常用两种方法:①用金属与氯气直接化合制得;②用金属与盐酸反应制得。用以上两种方法都可制得的氯化物是( )
A. MgCl2 B. FeCl3 C. FeCl2 D. CuCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置设计正确、且能达到目的是( ) 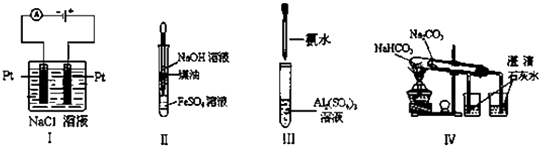
A.实验Ⅰ:制备金属钠
B.实验Ⅱ:制取氢氧化亚铁并观察其颜色
C.实验Ⅲ:制取少量的氢氧化铝
D.实验Ⅳ:比较两种物质的热稳定性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com