
【题目】已知饱和氯化铵溶液与亚硝酸钠晶体混合加热可制备氮气。利用如下装置制取氮气,并用氮气制备Ca3N2,Ca3N2遇水发生水解反应。下列说法错误的是
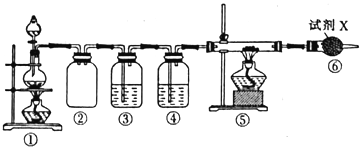
A. ①中发生的化学反应为NaNO2+NH4Cl![]() NaCl+N2↑+2H2O
NaCl+N2↑+2H2O
B. ④、⑥中依次盛装的试剂可以是浓H2SO4、碱石灰
C. ③中盛放的试剂是NaOH 溶液
D. 实验结束,取⑤中的少量产物于试管中,加适量蒸馏水,可以使试管口湿润的红色石蕊试纸变蓝
【答案】C
【解析】A、根据题干可知,装置①为制备氮气的装置,饱和氯化铵溶液与亚硝酸钠晶体混合生成氮气、氯化钠和水,所以反应方程式为NaNO2+NH4Cl![]() NaCl+N2↑+2H2O,故A正确。B、Ca3N2遇水发生水解,所以产生的氮气需要干燥才能进入玻璃管中反应,装置④应为干燥装置,可选用浓硫酸作干燥剂;装置⑥中也应装有干燥剂,防止空气中的水蒸气进入,装置⑥中可盛放碱石灰,故B正确。C、装置中含有氧气,可利用装置③除去装置中的氧气,NaOH溶液不能除氧气,可改成酸性氯化亚铁溶液,故C错误;D、实验结束后,装置⑤中有生成的Ca3N2,Ca3N2遇水发生水解反应生成NH3和Ca(OH)2,NH3可以使湿润的红色石蕊试纸变蓝,故D正确。故选C。
NaCl+N2↑+2H2O,故A正确。B、Ca3N2遇水发生水解,所以产生的氮气需要干燥才能进入玻璃管中反应,装置④应为干燥装置,可选用浓硫酸作干燥剂;装置⑥中也应装有干燥剂,防止空气中的水蒸气进入,装置⑥中可盛放碱石灰,故B正确。C、装置中含有氧气,可利用装置③除去装置中的氧气,NaOH溶液不能除氧气,可改成酸性氯化亚铁溶液,故C错误;D、实验结束后,装置⑤中有生成的Ca3N2,Ca3N2遇水发生水解反应生成NH3和Ca(OH)2,NH3可以使湿润的红色石蕊试纸变蓝,故D正确。故选C。


科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁是四种短周期元素,乙原子中K层与M层电子数相等;甲原子的核外电子数比乙原子核外电子数少1;丙原子的最外层电子数是次外层电子数的2倍;丁原子核电荷数比丙原子核电荷数多2。请回答:
(1)甲的单质与水反应的离子方程式为__________________。
(2)乙元素在周期表中的位置为__________________。
(3)丙元素的最高价氧化物的电子式为__________________。
(4)甲与丁两种元素可组成的具有强氧化性的物质是__________(填化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠是一种重要的化工原料,请回答下列问题:
I.高铁酸钾(K2FeO4)溶液呈紫红色,向其中加入过量亚硝酸钠后,溶液紫红色逐渐褪去,并出现红褐色沉淀,请写出该反应的离子方程式__________。
II.实验室模拟下图所示流程制备亚硝酸钠:

已知:①氧化过程中,控制反应温度在35~60℃条件下主要发生反应:
C6H12O6+12HNO3=3HOOC-COOH+9NO2↑+3NO↑+9H2O
②氢氧化钠溶液吸收NO和NO2发生反应:
NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO3+NaNO2+H2O

(1)木屑的主要成分是纤维素,结合已知信息①,你认为向木屑中加稀硫酸的作用是______,氧化过程中反应温度不宜高于60℃,原因是______________。
(2)不做任何处理,按此过程进行,氢氧化钠溶液吸收后的溶液中除了OH-外还有两种阴离子,其中一种是NO2-,NO2-与另一种阴离子的物质的量之比为________。
(3)装置B用于制备NaNO2,盛装的试剂除NaOH(aq)外,还可以是______(填字母)。
a.NaCl(aq) b.Na2CO3(aq) c.NaNO3(aq)
III.测定产品纯度:
【实验步骤】①准确称量ag产品配成200mL溶液;②从步骤①配制的溶液中移取20.00mL加入锥形瓶中;③用cmol/L酸性KMnO4溶液滴定至终点;④重复以上操作3次,消耗酸性KMnO4溶液的平均体积为VmL
(1)锥形瓶中发生反应的离子方程式为_____________。达到滴定终点的现象是_________。
(2)产品中NaNO2的纯度为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中( )
A. 水的电离程度始终增大
B. ![]() 先增大再减小
先增大再减小
C. c(CH3COOH)与c(CH3COO-)之和始终保持不变
D. 当加入氨水的体积为10 mL时,c (NH4+)=c(CH3COO-)
【答案】D
【解析】试题分析:A、CH3COOH属于弱酸,抑制水的电离,加入NH3·H2O,消耗CH3COOH,水的电离程度增大,但氨水过量后,对水电离抑制,故错误;B、当向CH3COOH溶液中滴加相同浓度的NH3·H2O,开始时溶液为CH3COOH和CH3COONH4的混合物,由CH3COONH4的水解常数Kh=[c(H+)×c(NH3·H2O)]/c(NH4+),随着氨水的加入,c(H+)逐渐减小,Kh不变,因此c(NH4+)/c(NH3·H2O)变小,当氨水至溶液显碱性时,氨水的电离常数Kb=[c(OH-)×c(NH4+)]/c(NH3·H2O),随着氨水的加入,c(OH-)逐渐增大,Kb不变,c(NH4+)/c(NH3·H2O)变小,因此此比值始终变小;C、根据物料守恒,n(CH3COOH)+n(CH3COO-)=0.001mol,由于溶液体积逐渐增大,因此c(CH3COOH)和c(CH3COO-)之和逐渐减小,故错误;D、当加入氨水的体积为10mL,醋酸和NH3·H2O物质的量相等,由于二者电离常数相等,因此溶液显中性,c(H+)=c(OH-),根据电荷守恒,c(NH4+)=c(CH3COO-),故正确。
考点:考查电离平衡常数、水解平衡常数、离子浓度大小比较等知识。
【题型】单选题
【结束】
13
【题目】常温下,下列有关离子浓度及pH大小的比较,正确的是( )
A. NH4+浓度相同的下列溶液:①(NH4)2Fe(SO4)2 ②(NH4)2CO3 ③(NH4)2SO4,溶液浓度由大到小的顺序是:③>②>①
B. 由pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,其离子浓度不可能是:c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
C. pH=13的Ba(OH)2溶液与pH=1的HCl溶液等体积混合后,混合溶液的pH>7
D. pH=12的Ba(OH)2溶液与pH=14的NaOH溶液等体积混合,混合溶液的pH范围是13<pH<14
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图表示细胞四种有机物的组成。依据生物功能,分析回答下列问题:
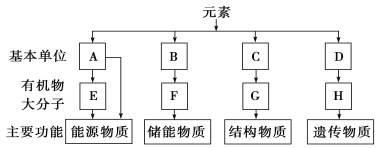
(1)A是指________;E在动物细胞内是指________,在植物细胞内主要是指________。
(2)F是指________;它是由B(脂肪酸和甘油)形成的,除此之外,脂质还包括________ 和________。
(3)C是指________,通式是________;C形成G过程的反应叫________。
(4)D是指________,H是指________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】40℃时,在氨—水体系中不断通入CO2,各种离子的变化趋势如下图所示。下列说法不正确的是( )
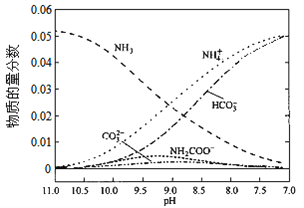
A. 在pH=9.0时,c(NH4+)>c(HCO3-)>c(NH2COO-)>c(CO32-)
B. 不同pH的溶液中存在关系:c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-)
C. 在溶液中pH不断降低的过程中,有含NH2COOˉ的中间产物生成
D. 随着CO2的通入,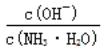 不断增大
不断增大
【答案】D
【解析】从图中在pH=9的点,做一条垂线就可以大致判断其浓度,所以有c(NH4+)>c(HCO3-)>c(NH2COO-)>c(CO32-),选项A正确。c(NH4+)+c(H+)=2c(CO32-)+c(HCO3-)+c(NH2COO-)+c(OH-)是溶液的电荷守恒,所以是任何pH下都成立的。选项B正确。随着pH的降低,NH2COOˉ的浓度增大,说明生成了含有NH2COOˉ的化合物,后期NH2COOˉ的浓度又减小,说明该化合物又被反应,说明含有NH2COOˉ的化合物是中间产物,选项C正确。根据一水合氨的电离平衡常数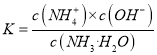 ,得到
,得到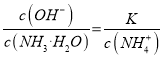 ,因为通入二氧化碳实际就是加入碳酸,加入酸c(NH4+)一定增大,所以
,因为通入二氧化碳实际就是加入碳酸,加入酸c(NH4+)一定增大,所以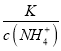 减小,即
减小,即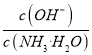 减小,选项D错误。
减小,选项D错误。
【题型】单选题
【结束】
17
【题目】下列物质中:A.KI(s) B.C2H5OH(l) C.Cl2(g) D.CH3COOH(l)E.BaSO4(s) F.NaHSO4(aq) G.石墨(s) H.蔗糖(s) I.NaOH(l) J.硫酸 K.盐酸
(1)属于非电解质的是____________(填序号,下同),属于强电解质的是____________,属于弱电解质的是____________。
(2)能直接导电的是________________,电解质中能溶于水,且水溶液能导电是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中通入两种气体并使其发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
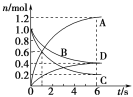
A. 该反应的化学方程式为3B+4D![]() 6A+2C
6A+2C
B. 0~1 s内,v(A)=v(C)
C. 0~6 s内,B的平均反应速率为0.05 mol·L-1·s-1
D. 0~6 s内,各物质的反应速率相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com