
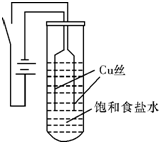
| ���� | �Ȼ�ͭ | ������ͭ | ��������ͭ �����ȶ��� | �Ȼ���ͭ |
| ��ɫ | �������ɫ��Ũ��Һ����ɫ��ϡ��Һ����ɫ | ��ɫ | �Ȼ�ɫ | ��ɫ |
| A�� | ���������������������ƶ� | B�� | ��ʼʱ����Cu �ŵ�����Cu2+ | ||
| C�� | ������ӦΪ2H2O+2e-=H2��+2OH- | D�� | ����ҺpH����CuCl��ת��ΪCuOH |
���� ���ʱ��ͭ��������������ͭʧ��������Cu+������Һ��Cu+��Cl-����CuCl��ɫ��������ʱ��Һ�е�c��OH-����С�����Խ�������˲�������CuOH������������ͬ�¶���CuCl���ܽ�ȴ���CuOH�����30s�����˳�����ת������CuCl��ΪCuOH������ɫ������ɳȻ�ɫ���ǣ���ʱ�ⶨ��Һ��pHԼΪ10����Һ��ʾ���ԣ�����CuOH���ȶ������һ��ʱ���ᷢ���ֽ����ɺ�ɫ��Cu2O������һ��ʱ����Թܵײ��ۼ�������ɫ��������Һ��������ȻΪNaCl��������Һ��Ϊ��ɫ��
A�����ʱ�������Һ���������������ƶ���
B����Ϊ����CuCl������������Cuʧ����������ͭ���ӣ�
C��������ˮ�õ��ӷ�����ԭ��Ӧ��
D����ͬ�¶���CuCl���ܽ�ȴ���CuOH���ܽ�ȴ��������ת��Ϊ�ܽ��С�����ʣ�
��� �⣺���ʱ��ͭ��������������ͭʧ��������Cu+������Һ��Cu+��Cl-����CuCl��ɫ��������ʱ��Һ�е�c��OH-����С�����Խ�������˲�������CuOH������������ͬ�¶���CuCl���ܽ�ȴ���CuOH�����30s�����˳�����ת������CuCl��ΪCuOH������ɫ������ɳȻ�ɫ���ǣ���ʱ�ⶨ��Һ��pHԼΪ10����Һ��ʾ���ԣ�����CuOH���ȶ������һ��ʱ���ᷢ���ֽ����ɺ�ɫ��Cu2O������һ��ʱ����Թܵײ��ۼ�������ɫ��������Һ��������ȻΪNaCl��NaOH��������Һ��Ϊ��ɫ��
A���������е������Һ���������������������ƶ�����A��ȷ��
B���������Ϸ���֪��������Cuʧ����������ͭ���ӣ���B����
C��������ˮ�õ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ2H2O+2e-=H2��+2OH-����C��ȷ��
D����ͬ�¶���CuCl���ܽ�ȴ���CuOH���ܽ�ȴ��������ת��Ϊ�ܽ��С�����ʣ���������ҺpH����CuCl��ת��ΪCuOH�������Ȼ�ɫ��������D��ȷ��
��ѡB��
���� ���⿼����ԭ����Ϊ��Ƶ���㣬��ȷ�������з����ķ�Ӧ�������ɷ��ǽⱾ��ؼ������ؿ���ѧ����ȡ��Ϣ����ȷ���Ⲣ���������������Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
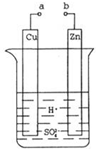 ԭ����ǻ�ѧ�������һ���ش��ף�ij��ȤС��Ϊ�о�ԭ���ԭ���������ͼװ�ã�
ԭ����ǻ�ѧ�������һ���ش��ף�ij��ȤС��Ϊ�о�ԭ���ԭ���������ͼװ�ã��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������� | B�� | ��������� | C�� | �Ҵ�������� | D�� | H��D��T |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
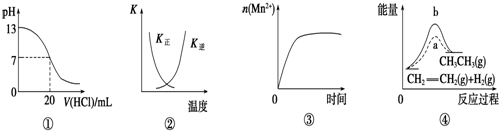
| A�� | ͼ�ٱ�ʾ25��ʱ����0.1 mol/L����ζ�20 mL 0.1 mol/L NaOH��Һ����Һ��pH�����������ı仯 | |
| B�� | ͼ�������߱�ʾ��Ӧ2SO2��g��+O2��g��?2SO3��g����H��0�����淴Ӧ��ƽ�ⳣ��K���¶ȵı仯 | |
| C�� | ͼ�۱�ʾ10 mL 0.01 mol/L KMnO4������Һ�������0.1 mol/L H2C2O4��Һ���ʱ��n��Mn2+����ʱ��ı仯 | |
| D�� | ͼ����a��b���߷ֱ��ʾ��Ӧ��CH2�TCH2��g��+H2��g����CH3CH3��g����H��0ʹ�ú�δʹ�ô���ʱ����Ӧ�����е��������仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶Y��Z�����Ӱ뾶Z-��M2+ | |
| B�� | MX2��ˮ������Ӧʱ��MX2ֻ�������� | |
| C�� | X��Y�γɵĻ����������ǿ�ᷴӦ������ǿ�Ӧ | |
| D�� | MX2��MZ2���ֻ������У��������������Ӹ����Ⱦ�Ϊ1��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
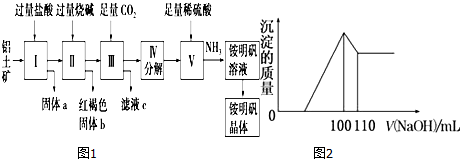
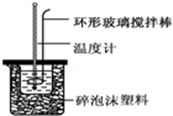 ʵ������50mL 0.50mol•L-1���ᡢ50mL 0.55mol•L-1 NaOH��Һ����ͼ��ʾװ�ã����вⶨ�к��ȵ�ʵ�飬�õ����е����ݣ�����������⣺
ʵ������50mL 0.50mol•L-1���ᡢ50mL 0.55mol•L-1 NaOH��Һ����ͼ��ʾװ�ã����вⶨ�к��ȵ�ʵ�飬�õ����е����ݣ�����������⣺| ʵ����� | ��ʼ�¶�t1/�� | ��ֹ�¶�t2/�� | |
| ���� | NaOH��Һ | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
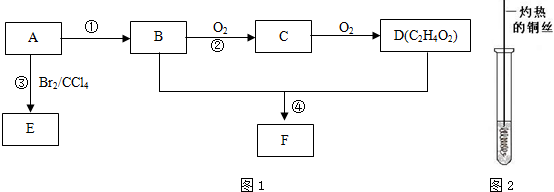
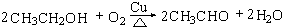 ��
��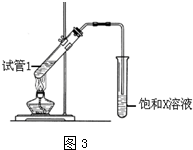 ��4��D��̼��������Һ��Ӧ�����ӷ���ʽΪCH3COOH+HCO3-��CH3COO-+H2O+CO2����
��4��D��̼��������Һ��Ӧ�����ӷ���ʽΪCH3COOH+HCO3-��CH3COO-+H2O+CO2�����鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com