
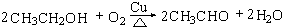 .
. (4)D与碳酸氢钠溶液反应的离子方程式为CH3COOH+HCO3-→CH3COO-+H2O+CO2↑.
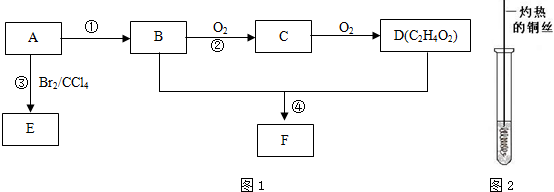
(4)D与碳酸氢钠溶液反应的离子方程式为CH3COOH+HCO3-→CH3COO-+H2O+CO2↑.分析 某气态烃A在标准状况下的密度为1.25g/L,其摩尔质量=1.25g/L×22.4L/mol=28g/mol,其产量可以用来衡量一个国家的石油化工发展水平,则A为CH2=CH2;
A和溴发生加成反应生成E为CH2BrCH2Br,
B氧化生成C、C氧化生成D,B和D都是生活中常见的有机物,结合D的分子式可知,B为CH3CH2OH,C为CH3CHO,D为CH3COOH,故反应①是乙烯与水发生加成反应生成CH3CH2OH,CH3CH2OH和CH3COOH在浓硫酸作用下发生酯化反应生成F为CH3COOCH2CH3,
再结合题目分析解答.
解答 解:某气态烃A在标准状况下的密度为1.25g/L,其摩尔质量=1.25g/L×22.4L/mol=28g/mol,其产量可以用来衡量一个国家的石油化工发展水平,则A为CH2=CH2;
A和溴发生加成反应生成E为CH2BrCH2Br,
B氧化生成C、C氧化生成D,B和D都是生活中常见的有机物,结合D的分子式可知,B为CH3CH2OH,C为CH3CHO,D为CH3COOH,故反应①是乙烯与水发生加成反应生成CH3CH2OH,CH3CH2OH和CH3COOH在浓硫酸作用下发生酯化反应生成F为CH3COOCH2CH3,
(1)A是乙烯,其结构简式为CH2=CH2,D是乙酸,其官能团名称是羧基,
故答案为:CH2=CH2;羧基;
(2)反应①的反应类型是加成反应,反应③为乙烯和溴的加成反应,该反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br,
故答案为:加成;CH2=CH2+Br2→CH2BrCH2Br;
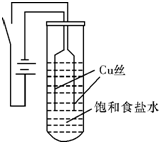
(3)反应②在Cu做催化剂的条件下进行,该实验的步骤是将红亮的铜丝置于酒精灯上加热,待铜丝变为黑色时,迅速将其插入到装有B的试管中(如图2所示),重复操作2-3次,观察到的现象是:铜丝由黑色变红色,产生刺激性气味,反应方程式为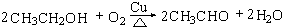 ,
,
故答案为:铜丝由黑色变红色,产生刺激性气味;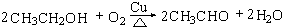 ;
;
(4)D是乙酸,乙酸和碳酸氢钠反应生成乙酸钠、二氧化碳和水,离子方程式为CH3COOH+HCO3-→CH3COO-+H2O+CO2↑,
故答案为:CH3COOH+HCO3-→CH3COO-+H2O+CO2↑;
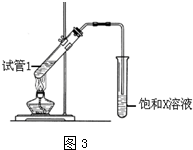
(5)乙酸乙酯的制取中,用浓硫酸作催化剂和吸水剂,用饱和的碳酸钠溶液分离乙酸乙酯,试管Ⅰ中在加热前应加碎瓷片,防止液体暴沸;导管末端为伸入小试管液面下的原因是防止倒吸;该反应的化学方程式为CH3COOH+HOCH2CH3$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;分离产物F的方法是分液,
故答案为:Na2CO3;催化剂、吸水剂;碎瓷片;防倒吸;CH3COOH+HOCH2CH3$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O;分液.
点评 本题考查有机物推断及物质制备,为高频考点,明确物质官能团及其性质关系、物质制备方法、实验操作等知识点是解本题关键,注意乙酸乙酯制备中实验操作规范性及饱和碳酸钠溶液的用途,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 物质 | 氯化铜 | 氧化亚铜 | 氢氧化亚铜 (不稳定) | 氯化亚铜 |
| 颜色 | 固体呈棕色,浓溶液呈绿色,稀溶液呈蓝色 | 红色 | 橙黄色 | 白色 |
| A. | 电解过程中氯离子向阳极移动 | B. | 电解开始时阳极Cu 放电生成Cu2+ | ||
| C. | 阴极反应为2H2O+2e-=H2↑+2OH- | D. | 随溶液pH升高CuCl逐渐转化为CuOH |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 实验结论 氧化性从强到弱的顺序:氯、溴、碘 |
| ①氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色 | |
| ②NaBr溶液+氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色 | |
| ③KI溶液+氯水+1mL CCl4,振荡,静置,观察四氯化碳层颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室制备Cl2,可用排饱和食盐水集气法收集 | |
| B. | 浓盐酸与KMnO4制氯气的离子方程式是:MnO4-+8H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+4H2O | |
| C. | 漂白粉溶液在空气中失效变化的离子方程式是:ClO-+CO2+H2O=HClO+HCO3- | |
| D. | H2O2具有很强的氧化性,在化学反应中只能作氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KW随浓度的改变而改变 | |
| B. | 一般情况下,一元弱酸HA的Ka 越大,表明该酸的酸性越弱 | |
| C. | 对已达到化学平衡的反应,改变压强,平衡常数(K)一定改变 | |
| D. | Ksp只与难溶电解质的性质和温度有关,而与溶液中的离子浓度无关 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
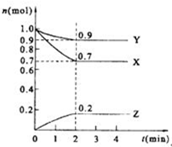 某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示.
某温度时,在2L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
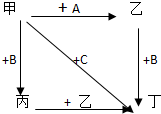 图中,乙是一种非金属单质,通常为黄绿色气体,A为一种黑色粉状固体,B是一种常见的金属单质,C是一种红褐色物质,它们之间存在如图关系:
图中,乙是一种非金属单质,通常为黄绿色气体,A为一种黑色粉状固体,B是一种常见的金属单质,C是一种红褐色物质,它们之间存在如图关系:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com