
����Ŀ���ȱ�����Ҫ���л�������Ʒ����Ⱦ�ϡ�ҽҩ���л��ϳɵ��м��壬��ҵ�ϳ�������϶������ȡ����Ӧԭ����ʵ��װ��ͼ������װ�ö�����ȥ�����£�![]()

��֪���ȱ�Ϊ��ɫҺ�壬�е�132.2�森
�ش��������⣺
��1��A��Ӧ��������ʵ���ҷ���ȡ�������пղ�����B��������___________,����������ˮӦ��______������a������b���� ��ͨ�롣
��2���Ѹ��������ͨ��װ�и��ﱽ�ķ�Ӧ��C�У������൱�ڱ���1%����м��������������ά�ַ�Ӧ�¶���40��60��Ϊ�ˣ��¶ȹ������ɶ��ȱ���
����C���ȵķ�����_________������ţ�
a���ƾ��Ƽ��� b����ԡ���� c��ˮԡ����
��D���ڵ�����ɷ���HCl��________��________��
��3��C��Ӧ����Ӧ��ɺ�ҵ��Ҫ����ˮϴ����ϴ��ʳ�θ����������ϴ֮ǰҪˮϴ��Ŀ����ϴȥ�������ͬʱ���ټ����������Լ�ɱ���д����10%�������Ƽ�ϴʱ���ܷ����Ļ�ѧ��Ӧ����ʽ��_____________________��_________________����д�������ɣ�
��4������װ��ͼ��A��C��Ӧ��֮�䣬��Ҫ����һ��U�ιܣ�������������________________��
��5����ҵ�����б�����ʧ������£�
��Ŀ | ���ȱ� | β�� | ��ȷ������ | ��ʧ���� |
����ʧ����kg/t�� | 13 | 24.9 | 51.3 | 89.2 |
��lt�����Ƶó�ƷΪ________________t��ֻҪ����ʽ����
���𰸡�ƽ����ѹ a c ������ ���� FeCl3+3NaOH=Fe��OH��3��+3NaCl HCl+NaOH=NaCl+H2O �����������Ȼ��� ![]()
��������
��1��������B����Һ���£�װ����ѹǿ����ʱ����������ƽ����ѹ����ȡ����ԭ��ͨ������ˮ��ʹ�����ܳ�������ˮ�������ȴ��������ˮ��a�����룬��b���������ʴ�Ϊƽ����ѹ��a��
��2������Ӧ��C���ȿ��Ʒ�Ӧ�¶���40-60����Ӧ����ˮԡ���ȣ���ѡc��
�����ӷ�����Ӧ��������HCl������δ��Ӧ��������D���������к���HCl�����������������ʴ�Ϊ��������������
��3�������Ȼ������������Ʒ�Ӧ�����ɵ�HCl�����������Ʒ�Ӧ���ܽ������Ҳ�����������Ʒ�Ӧ����Ӧ����ʽΪ��FeCl3+3NaOH=Fe��OH��3��+3NaCl��HCl+NaOH=NaCl+H2O��Cl2+2NaOH=NaCl+NaClO+H2O���ʴ�ΪFeCl3+3NaOH=Fe��OH��3��+3NaCl��HCl+NaOH=NaCl+H2O��
��4��A��C��Ӧ��֮����Ҫ����U�ܣ��������ɵ������������������������Ȼ��Ƶȣ��ʴ�Ϊ�����������Ȼ��ƣ�
��5����������ʧ��Ϊ89.2kg/t����1t���вμӷ�Ӧ�ı�������Ϊ��1t-0.0892t�����ɱ����ȱ�����֮��Ϊ78:112.5��֪�����ȱ�����Ϊ![]() t��
t��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������̿�(��Ҫ�ɷ�ΪMnO2��SiO2��Al2O3)�ͻ�����(FeS2��SiO2)Ϊԭ��ұ�������̵Ĺ���������ͼ��ʾ��

��֪��ؽ�������[c(Mn��)��0.1mol��L��1]�γ��������������pH���£�
�������� | Fe3�� | Mn2�� | Al3�� |
��ʼ������pH | 2.7 | 8.3 | 3.2 |
������ȫ��pH | 3.7 | 9.8 | 5.0 |
�ش��������⣺
���Ӳ����м����MnCO3��������____________________________���ù����������ҺpH�ķ�Χ��___________________________������pH���ù��ߣ�������_________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�� ���º�ѹ�£����ݻ��ɱ�������У���Ӧ2NO2 (g)![]() N2O4 (g)�ﵽƽ�������������ͨ��һ����NO2���ִﵽƽ��ʱ��N2O4���������
N2O4 (g)�ﵽƽ�������������ͨ��һ����NO2���ִﵽƽ��ʱ��N2O4���������
A����С B������ C������ D�����ж�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)ij�л���A�Ľṹ��ʽ����ͼ���밴Ҫ��д����Ӧ����Ľṹ��ʽ
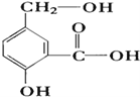
��A��NaOH��Һ��Ӧ ____________________________��
��A��NaHCO3��Һ��Ӧ _________________________________��
��A��Na��Ӧ _______________________��
(2)���������һ�����ϣ�����������ķ����ϳɣ�![]()
��д��A��B��C��D�Ľṹ��ʽ��
A ____________B_____________C_____________D_______________
��D�кܶ�ͬ���칹�壬���к����Ȼ���ͬ���칹���У������ϵ�һ�ȴ�����2�ֵĽṹ��ʽΪ________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��20mL 0.1mol��L��1������Һ�в��ϵ���0.1mol��L��1NaOH(aq)����ҺpH�仯��ͼ��ʾ���˹�������Һ������Ũ�ȵĹ�ϵ�������( )
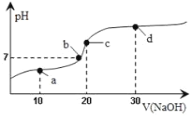
A.a�㣺c(CH3COO��)��c(Na+)��c(H+)��c(OH��)
B.b�㣺c(Na+) = c(CH3COO��)��c(H+) = c(OH��)
C.c�㣺c(H+) = c(CH3COO��) + c(OH��)
D.d�㣺c(Na +)��c(OH��) ��c(CH3COO��)��c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��CH3COOH��H2SO3����ѧ��ѧ�г��������ᣬ��ش��������⣺
��1�������£�����������֤��CH3COOHΪ������_________��
a�� CH3COONa ��Һ��pH����7��
b����ͬ�����ͬŨ�ȵ�����ʹ�����Һ���ֱ�������п�۷�Ӧ���ų���ͬ�����������
c����ͬ�������ͬpH������ʹ��ᣬ�����к�NaOH�����ʵ����ࣻ
d��0.01mol/L��CH3COOH��Һ��PH > 2
��2�������£���0.1 mol��L��1 CH3COOH��Һ�м�����ˮϡ�ͣ�ϡ�ͺ����и����������_________��
a.![]() b.
b.![]() c.c(OH-)
c.c(OH-)
��3����Ũ�Ⱦ�Ϊ0.1mol/LCH3COOH��CH3COONa��Һ�������ϣ���û��Һ��c(CH3COO��)>c(Na+)�������й�ϵʽ����ȷ������_____��
A��c(H+) > c(OH��) B��c(H+) < c(OH��)
C��c(CH3COOH) > c(CH3COO��) D��c(CH3COOH) + c(CH3COO��)=0.1mol/L
��4��������������ʵ���Ũ�ȵĴ��������������Һ��ϣ���Һ��_______������������������������������������ԭ���� _______________�������ӷ���ʽ��ʾ��������pH��3�Ĵ����pH��11������������Һ�������Ϻ���Һ��__________��������������������������������������Һ��c(Na��) ___________c(CH3COO��) ������ ���� ���������������� ����
��5��25��ʱ��H2SO3�ĵ��볣��Ka1=1��10-2mol/L��Ka2=6��10-3mol/L������¶���NaHSO3��ˮ��ƽ�ⳣ��Kh=__________mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����ȼ�ϵ�ؾƾ������ԭ����ͼ��ʾ������˵������ȷ���ǣ� ��

A.�����Ϸ����ķ�Ӧ�ǣ�O2��4e-��2H2O===4OH-
B.�����Ϸ����ķ�Ӧ�ǣ�CH3CH2OH��4e-��H2O ===CH3COOH��4H+
C.���ʱ���������Һ�е�H+���ƶ�
D.����0.4 mol����ת�ƣ������ı�״����4.48 LO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ӧ�ù㷺�Ľ�������������(��Ҫ�ɷ�ΪAl2O3����SiO2��Fe2O3������)Ϊԭ���Ʊ�����һ�ֹ����������£�

ע��SiO2����������ʱת��Ϊ�������Ƴ�����
��1����������ʱ����ƫ�����Ƶ����ӷ���ʽΪ_____________________��
��2������������������Һ�м���NaHCO3��Һ����Һ��pH_________ (��������������������������С��)��
��3����������ǵ������Al2O3������������������ʯī�����ģ�ԭ����___________��
��4����������ǵ��Na2CO3��Һ��ԭ����ͼ��ʾ�������ĵ缫��ӦʽΪ_____________________����������������A�Ļ�ѧʽΪ____________��

��5��������1000��ʱ����N2��Ӧ�Ʊ�AlN������������������NH4Cl���岢��ֻ�ϣ�������AlN���Ʊ�������Ҫԭ����_____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ѧʽΪC5H7Cl���л����ṹ�������ǣ� ��
A.ֻ��1��![]() ����ֱ���л���
����ֱ���л���
B.��2��![]() ����ֱ���л���
����ֱ���л���
C.��1��![]() ���Ļ�״�л���
���Ļ�״�л���
D.��1����C![]() C������ֱ���л���
C������ֱ���л���
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com