
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列各组性质比较中,正确的是 ( )
①酸性:HClO4>HBrO4>HIO4 ②碱性:Ba(OH)2>Mg(OH)2>Be(OH)2
③氧化性:F>C>O ④还原性:Cl<S<Si
⑤气态氢化物稳定性:HF>HCl>H2S
A.①②③ B.②③④ C.①②④⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
铜、锌和硫酸构成的原电池中,当导线中有1 mol电子通过时,理论上两极的变化是( )
①锌片溶解32.5 g ②锌片增重32.5 g ③铜片上析出1 g H2 ④铜片上析出1 mol H2
A.①③ B.①④ C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
在研究化学反应中的能量变化时,我们通常做下面的实验:
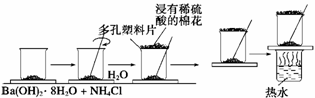
在一个小烧杯里,加入20 g已研磨成粉末的Ba(OH)2·8H2O,将小烧杯放在事先已滴有3~4滴水的玻璃片上,然后向烧杯中加入约10 g NH4Cl晶体,根据实验步骤,填写下表,并回答问题。
| 实验步骤 | 实验现象及结论 |
| 将晶体混合,立即快速搅拌 | 有刺激性气味能使湿润的紫色石蕊试纸变蓝的___①__产生 |
| 用手摸烧杯下部 | 感觉烧杯变凉说明此反应是_ ② 反应 |
| 用手拿起烧杯 | 烧杯下面的带有几滴水的玻璃片粘到了烧杯底部 |
| 将粘有玻璃片的烧杯放在盛有热水的烧杯上 | 玻璃片脱离上面烧杯底部 |
| 反应后移走多孔塑料片观察反应物 | 混合物成糊状,证明有_③___生成 |
(1)写出题目中①②③填入的内容
① ② ③
(2)实验中要立即用玻璃棒迅速搅拌的原因是: __________________。(2分)
(3)在上述实验过程中,为什么用浸有稀硫酸的湿棉花置于多孔塑料板上?(2分)
___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示是学生课外活动小组设计的制取氨气并进行氨气溶于水的喷泉实验等实验的装置示意图。

请回答下列问题:
(1)学生甲用图A所示装置制备氨气,写出该法制取氨气的化学方程式_________________________________________________________________;
制出的氨气应使用________法来收集,要得到干燥的氨气可选用________做干燥剂。
(2)学生乙用图B所示装置也制出了氨气,他选用的制取试剂可能是________和_ _______。
_______。
(3)学生丙用图C所示装置进行喷泉实验,烧瓶内已充满干燥的氨气,引发水向上喷的操作是_________ ___________________________________________
___________________________________________
_____________________________________ ____________________________。
____________________________。
(4)学生丁将装置C误认为装置D,但经同学讨论后,认为也可引发喷泉。请说明用该装置引发喷泉的方法________________________________________
_________________________________________________________________。
(5)学生戊用装置E吸收一段时间氨后,再通入空气,同时将经过加热的铂丝插入E装置的锥形瓶内,看到了具有催化作用的铂丝保持红热,同时瓶内生成了红棕色的气体。写出在此过程中可能发生反应的化学方程式___________
_________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下面有关铜的化合物的性质叙述中正确的是( )。
A.CuSO4变成Cu SO4·5H2O是物理变化
SO4·5H2O是物理变化
B.一定条件下,新制的Cu(OH)2悬浊液能与乙醛反应但不能与乙酸反应C.CuO是黑色固体,与水反应可生成Cu(OH)2
D.Cu2O遇硝酸可能会被氧化成Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
埋藏在地下的青铜器锈蚀过程可以表示为:Cu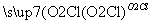
 CuCl
CuCl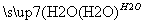 Cu2O―→X,X由两种物质X1和X2组成,且都由四种元素构成,定性实验表明:X1热分解的产物能使澄清石灰水变浑浊,而X2热分解的产物不能使澄清石灰水变浑浊,但两者均有水珠产生。为了定量测定X1和X2组成,某兴趣小组用如图实验装置对X1和X2分别做热分解实验(夹持装置已省去),实验结束后,硬质玻璃管内均残留黑色固体,分别称重,装置B和C中的质量均增加。
Cu2O―→X,X由两种物质X1和X2组成,且都由四种元素构成,定性实验表明:X1热分解的产物能使澄清石灰水变浑浊,而X2热分解的产物不能使澄清石灰水变浑浊,但两者均有水珠产生。为了定量测定X1和X2组成,某兴趣小组用如图实验装置对X1和X2分别做热分解实验(夹持装置已省去),实验结束后,硬质玻璃管内均残留黑色固体,分别称重,装置B和C中的质量均增加。

试回答下列问题:
(1)青铜器出土后防止青铜器继续锈蚀的关键是________________。
(2)利用上述装置进行热分解实验时,对判断A装置中反应是否完全进行带来困难,为解决此问题,要对B装置进行改装。B应改为内装有________(填试剂名称)的洗气瓶,判断反应完全的现象为__________________。
用经改装的装置,某同学进行正确操作,最终得出的测定结果仍有误差,原因是________________________________________________(回答一点即可)。
(3)在实验装置和实验操作正确的前提下,重做X1的热分解实验,测得装置B和C中质量增重之比Δm(B)∶Δm(C)=9∶22,________(填“能”或“否”)求出X1的化学式,若能求出X1的化学式,则化学式为______________(若不能求出X1的化学式,此空不填)。
(4)若测得X2中铜元素的质量分数为59.5%(铜元素的相对原子质量为63.5),则X2的化学式为______________________________________________。
X2热分解的化学方程式为_______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
向200mL Na2CO3和Na2SO4混合溶液中加入足量的BaCl2溶液,得到29.02g白色沉淀,用过量稀硝酸处理后剩余沉淀9.32g,并有气体产生。求:
(1)剩余沉淀的物质的量为___________ ;
(2)产生的气体在标准状况下的体积为___________ ;
(3)原混合溶液中Na+物质的量浓度为__________ _,Na2SO4的质量为___________ 。
计算过程:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com