
����Ŀ����������ȼ�ϵ��ԭ���о������°��ĺϳɣ���ع���ʱMV2+/MV+�ڵ缫��ø֮�䴫�ݵ��ӣ�ʾ��ͼ������ʾ������˵���������

A. ������й�ҵ�ϳɰ����÷��������ºͣ�ͬʱ�����ṩ����
B. �����������⻯ø�����·�����ӦH2+2MV2+![]() 2H++2MV+
2H++2MV+
C. ���������̵�øΪ������N2������ԭ��Ӧ����NH3
D. ��ع���ʱ����ͨ������Ĥ�ɸ��������������ƶ�
���𰸡�B
��������
������ȼ�ϵ�ص�ʾ��ͼ��֪�����ҵ缫Ϊȼ�ϵ�صĸ�����MV+�ڸ���ʧ���ӷ���������Ӧ����MV2+���缫��ӦʽΪMV+��e��= MV2+���ŵ����ɵ�MV2+���⻯ø����������H2��Ӧ����H+��MV+����Ӧ�ķ���ʽΪH2+2MV2+=2H++2MV+�����ҵ缫Ϊȼ�ϵ�ص�������MV2+�������õ��ӷ�����ԭ��Ӧ����MV+���缫��ӦʽΪMV2++e��= MV+���ŵ����ɵ�MV+��N2�ڹ̵�ø�������·�Ӧ����NH3��MV2+����Ӧ�ķ���ʽΪN2+6H++6MV+=6MV2++NH3����ع���ʱ��������ͨ������Ĥ�ɸ����������ƶ���
A�������й�ҵ�ϳɰ����÷���ѡ��ø�������������ºͣ�ͬʱ����MV+��MV2+���ת������ѧ��ת��Ϊ���ܣ��ʿ��ṩ���ܣ���A��ȷ��
B�����Ϊ��������MV+�ڸ���ʧ���ӷ���������Ӧ����MV2+���缫��ӦʽΪMV+��e��= MV2+���ŵ����ɵ�MV2+���⻯ø����������H2��Ӧ����H+��MV+����Ӧ�ķ���ʽΪH2+2MV2+=2H++2MV+����B����
C�����Ϊ��������MV2+�������õ��ӷ�����ԭ��Ӧ����MV+���缫��ӦʽΪMV2++e��= MV+���ŵ����ɵ�MV+��N2�ڹ̵�ø�������·�Ӧ����NH3��MV2+����C��ȷ��
D���ع���ʱ�������ӣ������ӣ�ͨ������Ĥ�ɸ����������ƶ�����D��ȷ��
��ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��V L Fe2(SO4)3��Һ�к���ag SO42-��ȡ����Һ0.5V L����ˮϡ����2V L����ϡ�ͺ���Һ��Fe3+�����ʵ���Ũ��Ϊ�� ��
A.![]() mol��L��1B.
mol��L��1B.![]() mol��L��1C.
mol��L��1C.![]() mol��L��1D.
mol��L��1D.![]() mol��L��1
mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ȤС���ڶ���������þ��[����MgCO3��Mg(OH)2��CaCO3��Al2O3��Fe2O3��SiO2]��Mg�����Ļ����ϣ������������Ʊ���ˮ���Ȼ�þ(MgCl2��6H2O)��

�����Ϣ���£�
��700��ֻ����MgCO3��Mg(OH)2�ķֽⷴӦ��
��NH4Cl��Һ������ϵ�е�MgO��Ӧ���ҷ�Ӧ�̶Ȳ���
�����������ǽ����ӹ�Һ���������������������ƺ��ʵ���������
��ش�
(1) ����˵����ȷ����________��
A�������������Ʒ�������������������������ձ�����ƿ
B������������ٽ�ƽ�������ƶ������MgO���ܽ���
C��������Խ���Һ�����C�ȹ��ˣ�������
D�����������Һ��������ɲ��ó�ѹ���ˣ�Ҳ�ɲ��ü�ѹ����
(2) �������Ҫ����ʵ�װ�ã�ʵ�����������պ�ָʾ��һ��(��������Һ���հ���)��
��ѡ��������������������˳������(��д������������ĸ�������Ǽгֺ���Ƥ������)����Դ��________��

��Ϊ��ָʾ����������ɣ���һ����������Һ�м�ָʾ�����������˵����������ֹͣʱ������________��
(3) ��ҺF�������ữ���������ᾧ�����ˡ�ϴ�Ӻ͵��¸���õ���Ʒ��ȡ������Ʒ����ˮ������Һ�ʼ��ԡ�
�ٺ��е�������________��
�ڴӲ����Ϸ����������ʵ�ԭ����________��
(4) ��ͬѧ����������沽����е�NH4Cl��Һ��������B��Ȼ����ӣ��Ʊ�MgCl2��Һ����֪���������γ��������������pH��Χ��
�������� | pH | |
��ʼ���� | ��ȫ���� | |
Al3+ | 3.0 | 4.7 |
Fe3+ | 1.1 | 2.8 |
Ca2+ | 11.3 | �� |
Mg2+ | 8.4 | 10.9 |
����������IJ�������(�����в�����ѡȡ�����Ⱥ�����г���ĸ���������ظ�ʹ��)������B��a����___������___������___������___������___������___����MgCl2��Һ����Ʒ��
a���������ܽ� b����pH��3.0 c����pH��5.0 d����pH��8.5
e����pH��11.0 f������ g��ϴ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����±�ΪԪ�����ڱ���һ���֣�����X��Y��Z��WΪ������Ԫ�أ�WԪ�صĺ˵����ΪXԪ�ص�2��������˵����ȷ���ǣ� ��
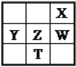
A. X��W��ZԪ�ص�ԭ�Ӱ뾶�����ǵ���̬�⻯������ȶ��Ծ����ε���
B. Y��Z��WԪ������Ȼ���о�����������̬���ڣ����ǵ�����������ˮ������������ε���
C. YX2�����ۻ���Һ̬WX3��������˷����Ӽ�������
D. ����Ԫ�������ɣ������Ʋ�TԪ�صĵ��ʾ��а뵼�����ԣ�T2X3���������Ժͻ�ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�������£���1.00molN2(g)��3.00molH2(g)�����һ��10.0L�ܱ������У��ڲ�ͬ�¶��´ﵽƽ��ʱNH3(g)��ƽ��Ũ����ͼ��ʾ�������¶�ΪT1ʱƽ���������а������������Ϊ25.0%��

��1���÷�Ӧ��T1�¶���5.0min�ﵽƽ�⣬���ʱ����N2�Ļ�ѧ��Ӧ����Ϊ_____________��
��2��T1�¶��¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K1=______________��
��3��T1�¶�ʱ�������������c(N2)=0.5mol/L��c(H2)=0.5mol/L��c(NH3)=0.5mol/L������������£��÷�Ӧ�Ƿ���ƽ��״̬__________(���ǻ��)����ʱ��Ӧ������v��_______v��(�������=)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±�ΪԪ�����ڱ���һ���֣��û�ѧ����ش��������⣺
���� ���ڡ� | ��A | ��A | ��A | ��A | ��A | ��A | ��A |
1 | �� | ||||||
2 | �� | �� | �� | ||||
3 | �� | �� | �� | �� | �� | �� |
��1�����ԭ�ӽṹʾ��ͼΪ________________________________��
��2���ں͢���̬�⻯���ȶ��ԵĴ�С˳��___________(�ѧʽ)��
��3���ۢ�����ۺ������������ǿ����__________(�ѧʽ)��
��4���۵���̬�⻯����۵�����������Ӧ��ˮ���ﷴӦ���ɵ�����________(�ѧʽ)��������________(�������ۻ��������������ӻ�������)��
��5���٢ܢ�����Ԫ�ص�ԭ�����γ�ԭ����Ŀ��Ϊ1��1��1�Ĺ��ۻ�������ĵ���ʽΪ________��
��6�����ȽϢܺ͢�����Ԫ�صķǽ�����ǿ����������Ϊ��֤��֤����________(����ĸ)��
A���Ƚ�������Ԫ�ص��ʵķе�
B���Ƚ�������Ԫ�ص������������ϵ�����
C���Ƚ�������Ԫ�ص�����������Ӧˮ����������
D���Ƚ�������Ԫ�ص��������Ӧ��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ����٤����������ֵ������˵����ȷ����
A. 0.1 mol H2��0.1 mol I2���ܱ������г�ַ�Ӧ���������������0.2 NA
B. ���ܱ������г���2 mol NO2һ��ʱ��������еķ�����Ϊ2 NA
C. 1 L 0.1 mol/L H3PO4��Һ�к�H����ĿΪ0.3 NA
D. 1 L 0.1 mol/L NH4Cl��Һ�к���NH4����ĿΪ0.1 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�����ƺ��ռ��ԭ�����£�����������Ȼ������ƣ�2NaCl(����) ![]() 2Na��Cl2��������ⱥ��ʳ��ˮ���ռ2NaCl��2H2O
2Na��Cl2��������ⱥ��ʳ��ˮ���ռ2NaCl��2H2O ![]() 2NaOH��H2����Cl2���������й�˵����ȷ���ǣ�������
2NaOH��H2����Cl2���������й�˵����ȷ���ǣ�������
A.�ڷ�Ӧ�������У��Ȼ��ƾ����������������ǻ�ԭ��
B.�ڷ�Ӧ���������ǻ�ԭ����ڷ�Ӧ���������ǻ�ԭ����
C.����״�������ɵ���������壬��Ӧ��������ת�Ƶ����������
D.�����ĵ��������Ȼ��ƣ���Ӧ�ٺ͢���ת�Ƶ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ά���ཱུ֬ҩ�������ؿ�������X��һ�������·�Ӧ�Ƶ�:

�����й�������ȷ����( )
A. 1mol����������������Na��Ӧ������22.4L��H2
B. ����X����������̼ԭ�ӿ���λ��ͬһƽ����
C. 1mol����X�������뺬2mol Br2����ˮ��Ӧ
D. �ñ���NaHCO3��Һ���Լ�������X�Ϳ�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com