
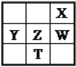
����Ŀ�����±�ΪԪ�����ڱ���һ���֣�����X��Y��Z��WΪ������Ԫ�أ�WԪ�صĺ˵����ΪXԪ�ص�2��������˵����ȷ���ǣ� ��
A. X��W��ZԪ�ص�ԭ�Ӱ뾶�����ǵ���̬�⻯������ȶ��Ծ����ε���
B. Y��Z��WԪ������Ȼ���о�����������̬���ڣ����ǵ�����������ˮ������������ε���
C. YX2�����ۻ���Һ̬WX3��������˷����Ӽ�������
D. ����Ԫ�������ɣ������Ʋ�TԪ�صĵ��ʾ��а뵼�����ԣ�T2X3���������Ժͻ�ԭ��
���𰸡�D
��������
�ӱ���λ�ù�ϵ�ɿ�����XΪ��2����Ԫ�أ�YΪ��3����Ԫ�أ�����ΪX��Wͬ������WԪ�صĺ˵����ΪX��2��������XΪ��Ԫ�ء�WΪ����Ԫ�أ��ٸ���Ԫ�������ڱ��е�λ�ù�ϵ����֪��YΪ��Ԫ�ء�ZΪ��Ԫ�ء�TΪ��Ԫ�ء�A��O��S��P��ԭ�Ӱ뾶��С��ϵΪ��P��S��O������Ԫ�ص���̬�⻯������ȶ���Ϊ��H2O��H2S��PH3��A����ȷ��B���ڻ�ɽ�ڸ�����ؿǵ��Ҳ��������������̬����B����ȷ��C��SiO2����Ϊԭ�Ӿ��壬�ۻ�ʱ��˷��������������Ϊ���ۼ���C����ȷ��D������Ԫ�����ڱ���λ�ڽ���Ԫ����ǽ����Ľ����߸��������а뵼������ԣ�As2O3����Ϊ+3�ۣ������м��̬�����Ծ��������Ժͻ�ԭ�ԣ�D��ȷ����ѡD��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��t ��ʱ�������������ܱ������з�����Ӧ��X(g)��3Y(g)![]() 2Z(g)��������ڲ�ͬʱ�̵�Ũ�����±���
2Z(g)��������ڲ�ͬʱ�̵�Ũ�����±���
���� | X | Y | Z |
��ʼŨ��/(mol��L��1) | 0.1 | 0.2 | 0 |
2 minĩŨ��/(mol��L��1) | 0.08 | a | b |
ƽ��Ũ��/(mol��L��1) | 0.05 | 0.05 | 0.1 |
����˵����ȷ����(����)
A. ƽ��ʱ��X��ת����Ϊ20%
B. 2 minʱY�����ʵ���Ϊ0.14
C. ����ƽ������ϵѹǿ��v(��)����v(��)��С
D. 2 min�ڣ���Y�ı仯����ʾ��ƽ����Ӧ����v(Y)��0.03 mol��L�D1��min�D1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з�Ӧ��mA (g) +nB (g)![]() pc (g) ���ﵽƽ������ߜض�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C����������Ҳ��С����
pc (g) ���ﵽƽ������ߜض�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C����������Ҳ��С����
��1���÷�Ӧ���淴ӦΪ____�ȷ�Ӧ����m+n____p (����>���� ��=�� ����<������
��2����ѹʱ��A����������______.(����������������С����������������ͬ��
��3��������B (������䣩����A��ת����_____��B��ת����_________��
��4�������ߜضȣ���ƽ��ʱB��C��Ũ��֮�Ƚ�__________��
��5�������������ƽ��ʱ��������������ʵ���______________��
��6����B����ɫ���ʣ�A��C����ɫ�������C (������䣩ʱ�������ɫ______����ά��������ѹǿ���䣬��������ʱ���������ɫ______(������������ ����dz������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������Ļ�����������ʵ�飺

��1������X��������___________��
��2������A��___________��
��3����������NaOH ��Һʱ������Ӧ�����ӷ���ʽΪ______________���������ᷢ����Ӧ�����ӷ���ʽΪ_______________��
��4����ҺB �������ӳ�OH-���_________����ҺD�д��ڵĽ�������Ϊ___________ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����2L�ܱ������У�����3A(g)��B(g) ![]() 2C(g)�ķ�Ӧ�����������A��B����4mol�� A��ƽ����Ӧ����Ϊ0.12mol��L��1��s��1����10s��������B�����ʵ�����
2C(g)�ķ�Ӧ�����������A��B����4mol�� A��ƽ����Ӧ����Ϊ0.12mol��L��1��s��1����10s��������B�����ʵ�����
A. 1.6 mol B. 2.8 mol C. 3.2 mol D. 3.6 mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������滮��ʵʩ�������Ϻ��Ļ���������λ�ڹ滮����һ������������Ǩ�����������ܵ��ó��������غ�ɫ���������š��������һ������Ⱦ����ܺ��У� ��
A. FeO�۳� B. P2O5�۳� C. Fe2O3�۳� D. SiO2�۳�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���̷��Ǻ���һ�����ᾧˮ�������������ڹ�ũҵ�����о�����Ҫ����;��ij��ͬѧ������ʵ��̽�������ʡ��ش��������⣺
(1)���Թ��м��������̷���Ʒ����ˮ�ܽ⣬���Ƴ�FeSO4��Һ������Һ�������������м����Ŀ����_____��
(2)����ͬѧȡ2 mLFeSO4��Һ�����뼸����ˮ���ټ���1��KSCN��Һ����Һ��죬˵��Cl2�ɽ�Fe2+������FeSO4��Һ����ˮ��Ӧ�����ӷ���ʽΪ______��
(3)����ͬѧ��Ϊ�����ʵ�鲻���Ͻ�������ͬѧ��2 mLFeSO4��Һ���ȼ���0.5 mL ú�ͣ�����Һ�������μ��뼸����ˮ��1��KSCN��Һ����Һ��죬ú�͵�������_________��
(4)����ͬѧ��ʢ��H2O2��Һ���Թ��м��뼸���ữ��FeSO4��Һ����Һ����ػ�ɫ��������Ӧ�����ӷ���ʽΪ________________
(5)Ϊ�ⶨ�̷��нᾧˮ��������ʯӢ�����ܣ������˿���K1��K2������Ϊװ��A�����أ���Ϊm1 g������Ʒװ��ʯӢ�������У��ٴν�װ��A���أ���Ϊ m2 g������ͼ���Ӻ�װ�ý���ʵ�顣
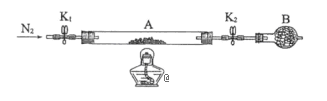
������B��������______��
�ڽ�����ʵ�����������ȷ����_____�����ţ����ظ������������裬ֱ��A���أ���Ϊm3 g��
a����ȼ�ƾ��ƣ����� b��Ϩ��ƾ��� c���ر�K1��K2
d����K1��K2������ͨ��N2 e������A f����ȴ������
�۸���ʵ���¼�������̷���ѧʽ�нᾧˮ��Ŀx=_________����ʽ��ʾ������ʵ��ʱ��a��d�����������ʹx_______���ƫ��ƫС������Ӱ�족����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ϩֱ��ˮ�Ϸ����Ҵ�����ȾС��Ӧ���ڹ�ҵ�ϳɣ������й�˵���������(����)
A. �÷�Ӧ���ڼӳɷ�Ӧ
B. ��ϩ��ʹ����KMnO4��Һ��ɫ
C. �����к���������ϩ������H2��ȥ
D. �����ʵ�������ϩ���Ҵ����ȼ�գ���������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������(�Է�ĩ״����)�Ͱ�������������ͬ�������塣��֪��
��Sn (s����)��2HCl (aq)��SnCl2 (aq)��H2 (g)��DH1
��Sn (s����)��2HCl (aq)��SnCl2 (aq)��H2 (g)��DH2
��Sn (s����)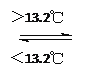 Sn (s����)��DH3����2.1 kJ/mol
Sn (s����)��DH3����2.1 kJ/mol
����˵����ȷ����( )
A. DH1��DH2
B. ���ڳ������Ի���״̬����
C. ����ת��Ϊ�����ķ�Ӧ�Ƿ��ȷ�Ӧ
D. ���������ڴ��ڵ���13.2 ���Ļ����У������лٻ�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com