
【题目】下列指定反应的离子方程式书写正确的是
A. 电解饱和氯化镁溶液:2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
B. Fe(OH)3溶于氢碘酸:Fe(OH)3+ 3H+=Fe3++3H2O
C. NaAlO2溶液中 AlO2-的水解:AlO2-+2H2O=Al(OH)3+ OH-
D. 向KAl(SO4)2溶液中加过量的Ba(OH)2溶液:Al3++2SO42- +2Ba2++4 OH-= AlO2-+2BaSO4↓+2H2O
 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:
【题目】下列物质的性质与用途具有对应关系的是
A. 明矾易溶于水,可用作净水剂
B. 二氧化硅熔点高,可用作光导纤维
C. 二氧化硫有氧化性,可用于漂白纸张
D. 过氧化钠可与二氧化碳反应生成氧气,可用作呼吸供氧剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)根据要求回答下列问题:
①CaBr2 ②H2O ③NH4Cl ④H2O2 ⑤Na2O2 ⑥Ca(OH)2 ⑦HClO ⑧I2 ⑨He
(1)含有共价键的离子化合物是(用序号回答) ,含有共价键的共价化合物是(用序号回答) 。
(2)当其熔化时,不破坏化学键的是(用序号回答) 。
(二)写出下列物质或微粒的电子式:
H2O: Na2O: CO2:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质:钠、Br2、CO2、SO3、NH3、H2S、硫酸、醋酸、Ba(OH)2、NH3·H2O、氯化钠、硫酸钡、乙醇、盐酸、蔗糖、胆矾,属于电解质、非电解质、强电解质的分别有
A. 9种、7种、6种 B.9种、5种、6种
C. 7种、5种、4种 D.8种、5种、5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在 1.01×105Pa、150℃条件下,某烃完全燃烧,反应前后压强不发生变化,该烃可能是( )
A. C2H4 B. C3H8 C. C2H6 D. C2H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用浓盐酸的质量分数为36.5%,密度为1.20 g/cm3。现用该浓盐酸配制100 mL 3.00 mol/L的盐酸。可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平。
请回答下列问题:
(1)配制稀盐酸时,上述仪器中不需要使用的有_________(选填序号),还缺少的仪器有_________(仪器名称)。
(2)经计算,配制100 mL 3.00 mol/L的稀盐酸需要用量筒量取上述浓盐酸的体积为_________mL(保留一位小数),量取浓盐酸时应选用_________(选填①10 mL、②50 mL、③100 mL的序号)规格的量筒。
(3)用配制所得100mL该稀盐酸与过量的铁屑充分反应,可制得氢气_________L(标准状况)。将生成的FeCl2配制成500 mL溶液,所得溶液中FeC12的物质的量浓度为_________mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡。下列说法正确的是
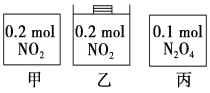
A.平衡时各容器内c(NO2)的大小顺序为乙>甲>丙
B.平衡时N2O4的百分含量:乙>甲=丙
C.平衡时甲中NO2与丙中N2O4的转化率相同
D.平衡时混合物的平均相对分子质量:甲>乙>丙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com