
【题目】一定温度下,在体积为2L的密闭容器中通入气体M和N并发生反应,物质的量随时间的变化关系如图。下列说法正确的是( )
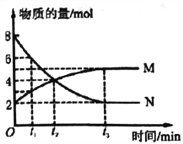
A. M、N之间转化的反应方程式为M =2N
B. t2时刻,反应达到平衡,正、逆反应速率达到相等
C. t3时刻,M的反应速率为![]() mol·L-1·min-l
mol·L-1·min-l
D. t1时刻,在容器内气体M和N的物质的量浓度之比为1:2
 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】已知:C(s)+ 1/2O2(g)CO(g) ΔH1 =—110.5 kJ/mol
CO(g)+ 1/2O2(g)CO2(g) ΔH2 = —283.0 kJ/mol
则反应C(s)+O2(g)CO2(g)的反应热为
A. 172.5 kJ/mol B. —172.5 kJ/mol C. 393.5 kJ/mol D. —393.5 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水煤气(CO 和H2)是合成甲醇的重要原料,它可用水蒸气通过炽热的炭层制得:C(s)+H2O(g)![]() CO(g)+H2(g) △H=+131.3kJ/mol
CO(g)+H2(g) △H=+131.3kJ/mol
⑴该反应的平衡常数的表达式为:_________________;升高温度,K值将 ;容器中气体的平均相对分子质量将 。(填“增大”、“减小”或“不变”)。
⑵上述反应达到平衡后,将体系中的C(s)部分移走,平衡将 (填序号)。
A.向左移 B.向右移 C.不移动
⑶下列事实能说明该反应在一定条件下已达到平衡状态的有 (填序号)。
A.单位体积内每消耗1molCO的同时生成1molH2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
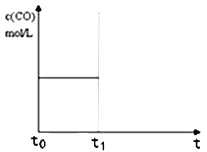
⑷上述反应在t0时刻达到平衡(如图),若在t1时刻改变某一条件,请在图中继续画出t1时刻后c(CO)随时间的变化曲线:
①缩小容器体积(用实线表示)。
②降低温度(用虚线表示)。
⑸某温度下,将4.0mol H2O(g)和足量的炭充入2L的密闭容器中,发生如下反应,C(s)+H2O(g)![]() CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是 ( )
A.已知2SO2(g)+O2![]() 2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
2SO3(g)为放热反应,则SO2的能量一定高于SO3的能量
B.已知C(石墨,s)=C(金刚石,s) △H﹥0,则金刚石比石墨稳定
C.已知H+(aq)+OH–(aq)=H2O(1) △H = -57.3kJ·mol-1,则任何酸碱中和的反应热均为57.3 kJ
D.已知2C(s)+2O2(g)=2CO2(g) △H1,2C(s)+O2(g)=2CO(g) △H2;则△H1﹤△H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示物质或微粒的化学用语或模型正确的是
A. 中子数为8的碳原子: ![]() B. S2-的结构示意图:
B. S2-的结构示意图: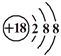
C. 二氧化碳电子式:![]() D. 氮气的结构式:N-N
D. 氮气的结构式:N-N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无机化合物X含有2种元素,是农业生产的一种杀虫剂,具有以下一系列变化:
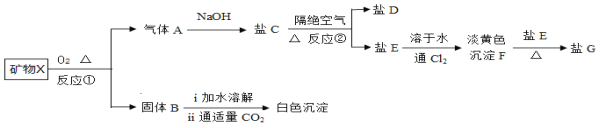
已知:1、气体A是形成酸雨的主要物质之一;
2、固体B是一种重要的建筑材料;
3、8.4gX在O2中充分灼烧得到2.8g固体B;
4、盐G的结构和Na2O2类似
请回答以下问题:
(1)写出CO2的电子式 ;X的化学式是 ;
(2)写出NaOH溶液中通入过量气体A的离子反应方程式 ;
(3)写出②的化学反应方程式 ;
(4)盐C在空气中易变质,请设计实验检验盐C是否变质 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X的单质是一种理想能源,X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。请回答下列问题:
(1)Y在元素周期表中的位置为__________。
(2)上述元素中,非金属气态氢化物还原性最强的是_________(写化学式);Y和Z形成的含有共价键的化合物的电子式为_________。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有_________。(写出其中两种物质的化学式)
(4)ZX与水剧烈反应产生X的单质,其化学方程式为_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】香料G 的一种合成工艺如下图所示。

核磁共振氢谱显示A有两种峰,且峰面积之比为1:1。
已知:CH3CH2CH=CH2![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2

请回答下列问题:
(1)A的结构简式为_________,M中官能团的名称为________。
(2)有学生建议,将M→N的转化用KMnO4(H+)代替O2,老师认为不合理,原因是:_______。
(3)写出下列转化的化学方程式,并标出反应类型:
D→E:______________,反应类型:________。
(4)F是M的同系物,比M多一个碳原子,F的同分异构体有多种,满足下列条件的F的同分异构体有_____种(不考虑立体异构),并写出核磁共振氢谱显示峰面积之比为1:2:2:2:3的结构简式__________。
① 能发生银镜反应 ② 能与溴的四氯化碳溶液加成 ③ 苯环上有2个对位取代基
(5)以丙烯和NBS试剂为原料制备甘油(丙三醇),请设计合成路线(其他无机原料任选)。请用以下方式表示:![]() ______________
______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com