

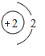 ��NaԪ�ص�ԭ�Ӱ뾶��ʴ�Ϊ��
��NaԪ�ص�ԭ�Ӱ뾶��ʴ�Ϊ��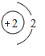 ��Na��
��Na�� 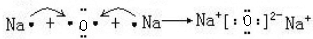 ���ʴ�Ϊ��
���ʴ�Ϊ��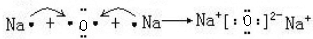 ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A���Ҵ���������ȡ��ȩ��2CH3CH2OH+O2
| |||
B������Ũ���ᡢŨ����Ļ��Һ�������������� +HNO3 +HNO3
 NO2+H2O NO2+H2O | |||
C��������Ҵ�������Ӧ��������������CH3CH2OH+CH3COOH
| |||
| D����ϩʹ������Ȼ�̼��Һ��ɫ��CH2�TCH2+Br2-��CH2Br-CH2Br |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� |
| �� |
| �� |
| �� |
| �� |
| H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| c(H+)?c(A-) |
| c(HA) |
| ���ữѧʽ | HCOOH | CH3COOH | C6H5OH | H2CO3 |
| ���볣�� | 1.8��10-4 | 1.8��10-5 | 1.3��10-10 | K1=4.3��10-7 K2=5.6��10-11 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��x+y��z |
| B��ƽ��������Ӧ�����ƶ� |
| C��Bת���ʼ�С |
| D������������½� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A���ṹʽΪ |
| B������ƽ����� |
| C�������������� |
| D������ͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�������ԣ�MnO
| ||||
B�������ԣ�S2O
| ||||
| C����ԭ�ԣ�I-��S2-��Fe2+��Mn2+��SO42- | ||||
D����ԭ�ԣ�Fe2+��I-��S2-��SO
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ͼ�ǡ�β����ת������������β�����ж�����ת��Ϊ���������ʾ��ͼ�����в�ͬ��Բ�������ͬԭ�ӣ�����˵��������ǣ�������
��ͼ�ǡ�β����ת������������β�����ж�����ת��Ϊ���������ʾ��ͼ�����в�ͬ��Բ�������ͬԭ�ӣ�����˵��������ǣ�������| A��ͼ��������ȫ���ǻ����� |
| B��ԭ���ڻ�ѧ�仯���Dz��ɷֵ� |
| C���˷�Ӧ�е������� |
| D���μӷ�Ӧ�����ַ��ӵĸ�����Ϊ1��1 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com