
【题目】党的十九大报告指出:要持续实施大气污染防治行动,打赢蓝天保卫战。当前空气质量检测的主要项目除了 PM2.5外,还有 CO、SO2、氮氧化物(NO和 NO2)、O3等气体。
完成下列填空:
(1)S2- 的核外电子排布式为__________, N原子核外电子有______种不同运动状态。
(2)C、O、S、N 四种元素中原子半径最小的是________(写元素符号);写出一个比较O与N非金属性强弱的事实: _____________________________________________。
(3)汽车尾气中含有NO和CO气体,用以下反应除去:2CO(g) +2NO(g) ![]() N2(g) +2CO2 (g) + Q
N2(g) +2CO2 (g) + Q
①该反应的平衡常数表达式为________________________;
②若增大压强,平衡常数__________(填“增大”、 “减小”或“不变”);
③若升高温度,逆反应速率先增大后减小,则 Q ______0(填“>”、 “<”或“=”)。
(4)某温度时,将 0.1mol CO和 0.1mol NO充入2L的密闭容器中,5s后测得生成 0.28g N2,则该时间内v(NO) = _______________。
【答案】 1s22s22p63s23p6 7 O NO中氮元素的化合价为+2,氧元素为-2(合理即可) 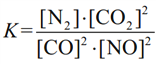 不变 > 0.002mol/(L·s)
不变 > 0.002mol/(L·s)
【解析】(1)S为16号元素,S2- 核外有18个电子,其核外电子排布式为:1s22s22p63s23p6;原子核外没有两个运动状态完全相同的电子,有几个电子就有几种运动状态,氮原子核外有7个电子,所以有7种不同运动状态。
故答案为:1s22s22p63s23p6;7;
(2)原子电子层数越大,半径越大;电子层数相同时,核电荷数越多半径越小。则C、O、S、N 四种元素中原子半径最小的为O元素;几种非金属元素同处于一种物质中,可用化合价判断其非金属性强弱,NO中氮元素的化合价为+2,氧元素为-2,说明O元素非金属性强于N元素;非金属单质与H2化合越容易,非金属性越强,O2与H2反应,比N2与H2反应容易,说明O元素的非金属性强于N元素。
故答案为:O;NO中氮元素的化合价为+2,氧元素为-2(或O2与H2反应,比N2与H2反应容易);
(3)①平衡常数K=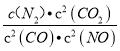 ;
;
②平衡常数只与温度有关,温度不变,平衡常数不变。
③升高温度,吸热反应速率和放热反应速率瞬间都增大,但吸热反应速率增得更多,所以吸热反应开始逐渐减小,放热反应开始逐渐增大,直到两个反应速率相等,达到新的平衡状态。本题中逆反应速率先增大后减小,则逆反应为放热反应,正反应为吸热反应,故△H>O。
故答案为:K= ;不变;>;
;不变;>;
(4)5s后生成 0.28g N2,即生成了0.01molN2,物质的量变化量之比等于系数之比,所以5s内NO变化了0.02mol。v(NO)= ![]() = 0.002mol/(L·s);
= 0.002mol/(L·s);
故答案为:0.002mol/(L·s);


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】每年6月5日为世界环境日.下列有关环保建议不能采纳的是( )
A.开发利用太阳能
B.提倡垃圾分类处理
C.改进汽车尾气净化技术
D.将工业废水直接排放
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个体重50kg的健康人,体内约含有2g铁,这2g铁在人体内不是以单质的形式存在,而是以Fe2+和Fe3+的形式存在.正二价铁离子易被吸收,给贫血者补充铁时,应给予含Fe2+的亚铁盐,如硫酸亚铁.服用维生素C,可使食物中Fe3+还原成Fe2+ , 有利于人体吸收.
(1)在人体中进行Fe2+ ![]() Fe3+的转化时,①中的Fe2+作剂,②中的Fe3+作剂.
Fe3+的转化时,①中的Fe2+作剂,②中的Fe3+作剂.
(2)“服用维生素C,可使食物中的Fe3+还原成Fe2+”这句话指出,维生素C在这一反应中作剂.
(3)市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸(HCl)的作用下转化成亚铁盐,此反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】C1O2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得C1O2:![]() ,下列说法中正确的是( )
,下列说法中正确的是( )
A. 在反应中H2C2O4既不是氧化剂也不是还原剂
B. 1 mol KClO3参加反应,在标准状况下能得到22.4 L气体
C. 1 mol KClO3参加反应有2 mol电子转移
D. KClO3在反应中是氧化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.第一电离能由大到小的顺序为N>O>C
B.由于C ![]() 和O
和O ![]() 为等电子体,所以可以判断O
为等电子体,所以可以判断O ![]() 的电子式为
的电子式为 ![]()
C.NO ![]() 中N采用sp2杂化,故NO
中N采用sp2杂化,故NO ![]() 的空间构型为三角锥形
的空间构型为三角锥形
D.液态HF通常也可以写成(HF)n的形式,是因为液态HF分子间存在氢键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数的值。俗名为“臭碱”的硫化钠广泛应用于冶金染料、皮革、电镀等工业。硫化钠的一种制备方法是Na2SO4+2C![]() Na2S+2CO2↑。下列有关说法正确的是
Na2S+2CO2↑。下列有关说法正确的是
A. 1mol/LNa2SO4溶液中含氧原子的数目一定大于4NA
B. 1L0.1mol/LNa2S溶液中含阴离子的数目小于0.1NA
C. 生成1mol氧化产物时转移电子数为4NA
D. 通常状况下11.2LCO2中含质子的数目为11NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于化学科学的说法,正确的是:
A.化学是在质子变化的层次上研究物质的一门基础学科
B.化学学科的特征是从宏观和微观两个角度认识物质
C.化学学科研究物质性质但不能创造出新物质
D.化学学科表征物质的方法与物理学科完全相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.SO2的水溶液能导电,所以SO2是电解质
B.酸式盐的水溶液呈酸性
C.醋酸溶液中醋酸的电离程度随温度的升高而增大
D.FeCl3的溶液加热蒸干可得到FeCl3的晶体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com