
【题目】每年6月5日为世界环境日.下列有关环保建议不能采纳的是( )
A.开发利用太阳能
B.提倡垃圾分类处理
C.改进汽车尾气净化技术
D.将工业废水直接排放
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分。
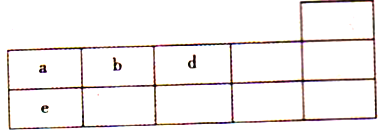
(1)a原子结构示意图为___________,d的一种氢化物为常见溶剂,其电子式为__________。
(2)e的最高价氧化物对应水化物的钠盐液中通入少量a的最高价氧化物会发生反应,写出相应的离子方程式:____________________________________。
(3)X、Y为同周期元素,它们简单离子的电子层与d离子的电子层结构相同,Y离子半径在同周期元素简单离子半径中最小,X、Y两种元素最高价氧化物对应的水化物之间可以相互反应生成盐和水,写出该反应的化学方程式:____________________________,X在周期表中的位置为________________。
(4)与Y同周期的W元素,其原子半径是同周期主族元素中最小的。工业上制取Y和W的无水化合物方法如下:Y的氧化物与a、W的单质在高温条件下反应,每消耗6kg a的单质,过程中转移1×103mol电子,写出相应反应的化学方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的( )
A.钠与水的反应:2Na+2H2O═2Na++2OH﹣+H2↑
B.硅酸钠溶液中通入过量CO2:SiO ![]() +2CO2+2H2O═H2SiO3↓+2HCO3﹣
+2CO2+2H2O═H2SiO3↓+2HCO3﹣
C.氯气与水反应:Cl2+H2O═2H++Cl﹣+ClO﹣
D.明矾溶液中加入过量的Ba(OH)2溶液:Al3++4OH﹣═AlO2﹣+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作均要用玻璃棒,其中玻璃棒作用相同的是( )
① 过滤 ② 蒸发 ③ 溶解 ④ 向容量瓶中转移液体
A.①和②B.①和③C.③和④D.①和④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表部分短周期元素信息,判断以下叙述正确的是( )

A. 氢化物的沸点为H2T<H2R B. 单质与稀盐酸反应的剧烈程度L<Q
C. M与T形成的化合物具有两性 D. L2+与R2﹣的核外电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
主族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
二 | ① | ② | ||||||
三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
四 | ⑨ | ⑩ |
(1)在③~⑦元素中,原子半径最大的是 ,其离子的原子结构示意图为
(2)元素的最高价氧化物对应的水化物中酸性最强的 ,碱性最强的是 ,呈两性的氢氧化物是 ;
(3)按要求写出下列两种物质的电子式:①的氢化物 ;⑨的最高价氧化物的对应的水化物 ;
(4)在⑦与⑩的单质中,化学性质较活泼的是 ,可用什么化学反应说明该事实(写出反应的化学方程式): 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量Mg、Zn、Al的混合物与足量稀H2SO4反应,生成H2 2.8L(标准状况),则原混合物的质量不可能是( )
A.2g B.4g C.6g D.8g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】党的十九大报告指出:要持续实施大气污染防治行动,打赢蓝天保卫战。当前空气质量检测的主要项目除了 PM2.5外,还有 CO、SO2、氮氧化物(NO和 NO2)、O3等气体。
完成下列填空:
(1)S2- 的核外电子排布式为__________, N原子核外电子有______种不同运动状态。
(2)C、O、S、N 四种元素中原子半径最小的是________(写元素符号);写出一个比较O与N非金属性强弱的事实: _____________________________________________。
(3)汽车尾气中含有NO和CO气体,用以下反应除去:2CO(g) +2NO(g) ![]() N2(g) +2CO2 (g) + Q
N2(g) +2CO2 (g) + Q
①该反应的平衡常数表达式为________________________;
②若增大压强,平衡常数__________(填“增大”、 “减小”或“不变”);
③若升高温度,逆反应速率先增大后减小,则 Q ______0(填“>”、 “<”或“=”)。
(4)某温度时,将 0.1mol CO和 0.1mol NO充入2L的密闭容器中,5s后测得生成 0.28g N2,则该时间内v(NO) = _______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com