
【题目】中草药秦皮中含有的七叶树内酯(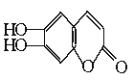 碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用。若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
碳氢原子未画出,每个折点表示一个碳原子),具有抗菌作用。若1mol 七叶树内酯,分别与 浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )
A. 3mol Br22mol NaOH B. 3mol Br24mol NaOH
C. 2mol Br23mol NaOH D. 4mol Br24mol NaOH
科目:高中化学 来源: 题型:
【题目】下列物质之间的相互关系错误的是( )
A. O2和O3互为同素异形体
B. 12C和14C互为同位素
C. CH3CH2OH和CH3OCH3互为同分异构体
D. CH3COOCH3和HCOOCH2CH3为同一种物质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.下列物质:①1H、2H、3H ;②H2O、D2O、T2O;③O2、O3;④12C、14C
(1)互为同位素的是______(填序号,下同);
(2)互为同素异形体的是_____;
(3)氢的三种原子1H、2H、3H与氯的两种原子35Cl、37Cl相互结合为氯化氢,可得分子中相对分子质量不同的有___种;
Ⅱ.用化学用语回答下列问题:
(1)写出NaOH的电子式____;
(2)用电子式表示二氧化碳分子的形成过程____;
下列物质:①N2②H2O2③NH3④Na2O ⑤NH4Cl
(3)含有极性键和非极性键的是_______(填序号,下同);
(4)含有极性键的离子化合物是_________;
(5)氟化氢水溶液中存在的氢键有________种;
(6)分子(CN)2分子中每个原子最外层均满足8电子稳定结构,其结构式为_____。
Ⅲ.正交硫和单斜硫是硫元素的两种常见单质,其晶状结构如左下图所示;构成晶体的微粒均是S8分子,其分子结构如右下图所示。回答下列问题:

已知正交硫的熔点为112.8℃,沸点为444.6℃,硬度较小。晶状的正交硫的微粒间存在在相互作用力有:______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与![]() ===
===![]() 相比较,水的作用不相同的是( )
相比较,水的作用不相同的是( )
A. ![]() ===
===![]() ↑
↑
B. ![]() ===
===![]()
C. ![]() ===
===![]()
D. ![]() ===
===![]() ↑
↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质性质与用途具有对应关系的是( )
A.NaHCO3受热易分解,可用于制胃酸中和剂
B.SiO2熔点高、硬度大,可用于制光导纤维
C.Al2O3是两性氧化物,可用作耐高温材料
D.硅胶多孔能吸水,可用作食品干燥剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原子序数大于4的主族元素Xm+、Yn-的离子核外电子层结构相同,则关于X、Y两元素的叙述正确的是
A. X的原子序数小于Y的原子序数 B. X、Y的核电荷数之差是(m-n)
C. X和Y处于同一周期 D. Y元素与X元素的族序数之差是8-(m+n)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】陶瓷是火与土的结晶,其形成、性质与化学有着密切的关系,下列说法错误的是( )
A.瓷器青色,来自氧化铁B.陶瓷由粘土经高温烧结而成
C.陶瓷主要化学成分是硅酸盐D.陶瓷化学性质稳定,具有抗氧化等优点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列框图所示的物质转化关系中,甲是日常生活中常见的金属,乙、丙、丁是常见的气体单质。气体B与气体C相遇产生大量的白烟,D是日常生活中常见的盐(部分反应物和生成物及溶剂水已略去)。

请回答下列问题:
(1)用电子式表示D的形成过程_________________;
(2)C的电子式为______________________;
(3)写出A溶液和丁反应生成D的离子方程式_________________________________;
(4)写出A和E反应的化学方程式_____________________________________。.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G是短周期元素,周期表中B与C相邻,C与E同主族;A中L层是K层的2倍,B的电子数比C的电子数少1个;F元素的原子在周期表中半径最小;常见化合物D2C2与水反应生成C的气体单质,且溶液使酚酞溶液变红。G是第三周期原子半径最小的主族元素。
(1)B在元素周期表中的位置_____;D的最高价氧化物的水化物的电子式____,用电子式表示FGC的形成过程为_______;
(2)B与F元素可形成18电子分子的电子式为_____。
(3)A、B、C的氢化物稳定性顺序为_______(用分子式表示);G的阴离子的还原性_____(大于或小于)E的阴离子。
(4)F2C和F2E中,沸点较高的是____(填化学式),其主要原因是_____。
(5)锡(Sn)是古代五金之一,在第五周期第ⅣA,锡能和浓硫酸反应生成Sn(SO4)2和刺激性气味气体,反应的化学方程式为_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com