
| A. | ClO-做还原剂 | |
| B. | 制备1molK2FeO4时转移3mol 电子 | |
| C. | 高铁酸钾中铁的化合价为+7 | |
| D. | Fe(OH)3在反应中被还原,发生还原反应 |
分析 2Fe(OH)3+3KClO+4KOH═2K2FeO4+3KCl+5H2O中,Fe元素的化合价由+3价升高为+6价,Cl元素的化合价+1价降低为-1价,以此来解答.
解答 解:A.Cl元素的化合价降低,则制备高铁酸钾用ClO-做氧化剂,故A错误;
B.制备高铁酸钾时1 mol Fe(OH)3失去3 mol 电子,故B正确;
C.K为+1价,O为-2价,由化合物中正负化合价的倒数和为0可知,高铁酸钾中铁的化合价为+6,故C错误;
D.Fe元素的化合价由+3价升高为+6价,所以Fe(OH)3在反应中被氧化,发生氧化反应,故D错误;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,注重化学与生活的联系,考查点较多,题目难度不大.


科目:高中化学 来源: 题型:选择题
| 选项 | 剩余固体 | 剩余固体的物质的量之比 |
| A | Pb3O4,PbO | 1:1 |
| B | PbO2,Pb3O4 | 1:1 |
| C | PbO2,Pb3O4,PbO | 1:2:1 |
| D | PbO2,Pb3O4,PbO | 1:1:2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
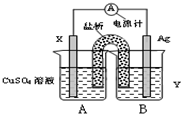 化学科学的重要责任在于认识自然界里存在的各种各样的、奇妙的化学反应,探索纷繁的化学反应的本质和规律.通过化学反应原理模块的学习,我们可以比较深刻地理解化学科学的精髓,提高化学学科素养.请根据所学化学反应原理,解决以下问题.
化学科学的重要责任在于认识自然界里存在的各种各样的、奇妙的化学反应,探索纷繁的化学反应的本质和规律.通过化学反应原理模块的学习,我们可以比较深刻地理解化学科学的精髓,提高化学学科素养.请根据所学化学反应原理,解决以下问题.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、Ba2+、Br-、CO32- | B. | K+、Na+、SO42-、MnO4- | ||
| C. | Na+、H+、NO3-、HCO3- | D. | Cl-、NO3-、Fe2+、H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液的质量增大 | B. | 溶质的溶解度增大 | ||
| C. | 溶液的浓度不变 | D. | 固体的质量一定不变 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高一上期中化学试卷(解析版) 题型:计算题
乙烯(C2H4)和乙烷(C2H6)的混合气体共amol,与bmolO2共存于一密闭容器中,点燃后充分反应,乙烯和乙烷全部消耗完,得到CO和CO2的混合气体和45gH2O,试求:
(1)当a=1时,乙烯和乙烷的物质的量之比n(C2H4):n(C2H6)= 。
(2)当a=1,且反应后CO和CO2的混合气体的物质的量为反应前O2的2/3时,b= ,得到的CO和CO2的物质的量之比n(CO)∶n(CO2)= 。
(3)a的取值范围是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com