
| A. | NH4+、Ba2+、Br-、CO32- | B. | K+、Na+、SO42-、MnO4- | ||
| C. | Na+、H+、NO3-、HCO3- | D. | Cl-、NO3-、Fe2+、H+ |
分析 A.钡离子与碳酸根离子反应生成碳酸钡沉淀;
B.四种离子之间不发生反应;
C.氢离子与碳酸氢根离子反应;
D.硝酸根离子在酸性条件下具有氧化性,能够氧化亚铁离子.
解答 解:A.Ba2+、CO32-之间反应生成碳酸钡沉淀,在溶液中不能大量共存,故A错误;
B.K+、Na+、SO42-、MnO4-之间不反应,在溶液中能够大量共存,故B正确;
C.H+、HCO3-之间发生反应,在溶液中不能大量共存,故C错误;
D.NO3-、Fe2+、H+之间发生氧化还原反应,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的正误判断,为中等难度的试题,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间;能发生络合反应的离子之间(如 Fe3+和 SCN-)等;试题侧重对学生基础知识的训练和检验,有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力.


科目:高中化学 来源: 题型:选择题
| A. | NaHC03水溶液显碱性,溶液中阳离子电荷总数小于阴离子电荷总数 | |
| B. | SiO2不跟碱反应,但可与氢氟酸反应 | |
| C. | NO2难液化,易溶于水并跟水反应 | |
| D. | Fe3O4能与浓盐酸反应生成FeCl2和FeCl3 |
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三月考二化学试卷(解析版) 题型:实验题
高铁酸钾广泛应用于净水、电池工业等领域。工业上以钛白粉生产的副产品FeSO4制备高铁酸钾的生产流程如下:

查资料得知K2FeO4的一些性质:
①在碱性环境中稳定,在中性和酸性条件下不稳定。
②在水中溶解度很大,难溶于无水乙醇等有机溶剂。
回答下列问题:
(1)写出氧化I中,生成Fe3+的离子反应方程式:
(2)氧化II中,试剂A为 (填“H2O2”或“HNO3”或“NaC1O”),反应的离子方程式为_____________________。
(3)操作I中包括冷却结晶,过滤洗涤、干燥几个步骤,洗涤干燥的目的是脱碱脱水,进行洗涤操作时应该用 洗涤。
(4)净水时高铁酸钾能逐渐与水反应生成絮状的Fe(OH)3,请补充并配平该反应方程式的系数及产物:
______K2FeO4 + H2O  Fe(OH)3(胶体)+ KOH + 。
Fe(OH)3(胶体)+ KOH + 。
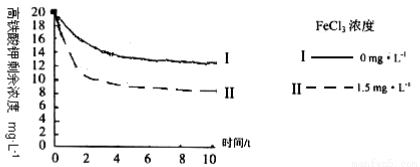
将一定量的K2FeO4投入一定浓度的FeC13溶液中,测得剩余K2FeO4浓度如下图所示,推测产生曲线I和曲线II差异的原因是: 。
(5)制得的粗K2FeO4产品中常混有少量KCl。取5.0 g粗产品溶于足量稀硝酸,充分反应后,加入足量的硝酸银,过滤得到沉淀,洗涤、干燥,称量得到1.435 g固体,K2FeO4的质量分数为___________。(可能用到的相对原子质量:O 16 Cl 35.5 K 39 Fe 56 Ag 108)
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上制取Y的单质常用还原剂还原Y的氧化物 | |
| B. | Z的最高价氧化物能与水反应生成相应的酸 | |
| C. | 室温下,X的最高价氧化物的水溶液的pH>7 | |
| D. | Y单质在一定条件下可以与氧化铁发生置换反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是C;
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是C;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ClO-做还原剂 | |
| B. | 制备1molK2FeO4时转移3mol 电子 | |
| C. | 高铁酸钾中铁的化合价为+7 | |
| D. | Fe(OH)3在反应中被还原,发生还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物理量 实验序号 | V(溶液)/mL | NH4Cl质量/g | 温度/℃ | pH | … |
| 1 | 250 | m | T1 | X | … |
| 2 | 250 | m | T2 | Y | … |

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验编号 | T/K | A的初始浓度/mol•L-1 | B的初始浓度/mol•L-1 | 催化剂的比表面积/m2•g-1 |
| Ⅰ | 200 | 0.40 | 0.60 | 82 |
| Ⅱ | T | 0.40 | 0.60 | 124 |
| Ⅲ | 220 | c1 | c2 | S |
| A. | T=200 | B. | S=100 | C. | c1=0.40 | D. | c2=0.60 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省高二上10月月考化学试卷(解析版) 题型:选择题
可通过实验来验证淀粉水解可生成还原性糖,其实验包括下列一些操作过程,这些操作过程正确的顺序是
①取少量淀粉加水制成溶液②加热煮沸③加入碱液中和并呈碱性
④加入新制Cu(OH)2悬浊液⑤加入几滴稀硫酸⑥再加热
A.①②⑤⑥④③ B.①⑤②④⑥③
C.①⑤②③④⑥ D.①⑥④⑤③②
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com