
【题目】下列属于物理变化的是 ( )
A.煤的干馏B.石油的裂化C.石油的裂解D.石油的分馏
科目:高中化学 来源: 题型:
【题目】可逆反应N2+3H2![]() 2NH3是一个放热反应。有甲、乙两个完全相同的容器,向甲容器中加入1molN2和3molH2,在一定条件下,达平衡时放出的热量为Q1;在相同条件下,向乙容器加入2molNH3,达平衡时,吸收的热量为Q2.已知Q2=4Q1,则甲容器中H2的转化率为
2NH3是一个放热反应。有甲、乙两个完全相同的容器,向甲容器中加入1molN2和3molH2,在一定条件下,达平衡时放出的热量为Q1;在相同条件下,向乙容器加入2molNH3,达平衡时,吸收的热量为Q2.已知Q2=4Q1,则甲容器中H2的转化率为
A. 80% B. 25% C. 75% D. 20%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将钠、铝混合物,放入足量的水中,反应停止后,还有不溶物,则此时溶液中溶质为
A.NaOHB.NaAlO2C.NaOH和NaAlO2D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列可以大量共存的离子组是( )
A. 无色透明溶液中:NH4+、Cu2+、Cl﹣、NO3﹣
B. 碱性溶液中:K+、Na+、SO42﹣、Cl﹣
C. 酸性溶液中:K+、Na+、HCO3﹣、Ca2+
D. 酸性溶液中:Na+、Fe2+、SO42﹣、ClO﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】32 g某气体的分子数目与22 g 二氧化碳的分子数目相同,则该气体的摩尔质量为 ( )
A. 32 g B. 32 g·mol-1 C. 64 g·mol-1 D. 64 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是六种短周期主族元素,它们的原子序数依次增大,其中C是地壳中含量最多的元素,A、F两元素的原子核中质子数之和比C、D两元素原子核中质子数之和少2,F元素的最外层电子数是次外层电子数的0.75倍.又知B元素的最外层电子数是内层电子数的2倍,E元素的最外层电子数等于其电子层数.
请回答:
(1)由E、F二种元素组成的化合物跟由A、C、D三种元素组成的化合物的水溶液充分反应的化学方程式为____________。
(2)单质B与A2C在一定条件下发生反应,工业上用于制水煤气、利用水煤气合成二甲醚的三步反应如下:
①2H2(g)+CO(g) ![]() CH3OH(g) ΔH=-90.8 kJ·mol-1
CH3OH(g) ΔH=-90.8 kJ·mol-1
②2CH3OH(g) ![]() CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
③CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH=-41.3 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.3 kJ·mol-1
请写出由水煤气合成二甲醚的总反应的热化学方程式:__________ 。
(3)用B元素的单质与E元素的单质可以制成电极浸入由A、C、D三种元素组成的化合物的溶液中构成电池,则电池负极的电极反应式_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验证明铜与浓硫酸能发生反应,并检验生成气体的性质,如图所示,在试管里加入2mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把放出的气体依次通入品红溶液和石蕊溶液中. 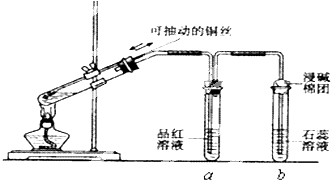
请回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式: .
(2)试管a、b分别检验生成气体的性质,写出观察到的现象及其作用.试管a中的现象是 , 作用是 . 试管b中的现象是 , 作用是 .
(3)装置中浸碱面团的作用是 .
(4)如图将铜丝改为可抽动的铜丝符合化学实验“绿色化”的原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列依据热化学方程式得出的结论正确的是( )
A. 常温常压下,1 g H2在足量Cl2中燃烧生成HCl,放出92.3 kJ的热量,则热化学方程式可表示为H2(g)+Cl2(g)2HCl(g) ΔH=+184.6 kJ·mol-1
B. 甲烷的标准燃烧热为ΔH=-890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为CH4(g)+2O2(g)CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
C. 已知NaOH(aq)+HCl(aq)NaCl(aq)+H2O(l) ΔH=-57.4 kJ·mol-1,则含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量
D. 相同条件下,2 mol氢原子所具有的能量小于1 mol氢分子所具有的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度不变的条件下,在恒容的容器中进行下列反应:N2O4(g)═2NO2(g),若N2O4的浓度由0.1molL﹣1降到0.07molL﹣1需要15s,那么N2O4的浓度由0.07molL﹣1降到0.05molL﹣1所需的反应时间( )
A.等于5s
B.等于10s
C.小于10s
D.大于10s
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com