
【题目】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。进行此实验所用仪器如图:
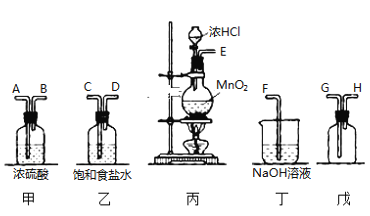
(1)连接上述仪器的正确顺序是 ________________________ 。
(2)气体发生装置中进行反应的离子方程式是_________________________;当0.5molMnO2反应时,生成的Cl2在标准状况下的体积约为 ________L。
(3)在装置中:乙中饱和食盐水的作用是___________________________,甲中浓硫酸的作用是_________________________。
(4)化学实验中检验是否有Cl2产生常用湿润的淀粉-KI试纸,如果有Cl2产生,可观察到的现象是____________________________,写出反应的化学方程式______________________________________。
(5)若用盛有过量烧碱溶液的小烧杯吸收标准状况下VL氯气,充分反应后,溶液中含等物质的量的次氯酸钠和氯酸钠,则反应消耗的NaOH的物质的量为____________mol。
【答案】丙乙甲戊丁 4H+ + 2Cl- + MnO2![]() Mn2+ + Cl2↑+2H2O 11.2 除去Cl2中的HCl 干燥氯气(或除去氯气中的水蒸气) 试纸变蓝 Cl2 + 2KI = 2KCl + I2
Mn2+ + Cl2↑+2H2O 11.2 除去Cl2中的HCl 干燥氯气(或除去氯气中的水蒸气) 试纸变蓝 Cl2 + 2KI = 2KCl + I2 ![]()
【解析】
本题为氯气的制备和性质检验,装置丙为发生装置,依据浓盐酸的挥发性可知制取的氯气中含有氯化氢和水蒸气,依次通过洗气瓶乙和甲除去氯化氢和水蒸气,装置戊可收集干燥的氯气,又氯气有毒需要进行尾气处理,装置丁为吸收过量氯气装置,结合氯气的性质进行分析。
(1)实验装置的连接顺序为:发生装置→除杂装置→收集装置→尾气处理装置;因为收集的是气体,所以除杂装置中长导管进气,短导管出气;因为饱和食盐水中有水,浓硫酸有吸水性,所以先连接饱和食盐水装置后连接浓硫酸装置;收集装置中,因为氯气的浓度大于空气的,所以长导管进气短导管出气,最后氯气用氢氧化钠吸收,故连接上述仪器的正确顺序是;丙乙甲戊丁;
(2)气体发生装置中浓盐酸与二氧化锰在加热条件下制备氯气,其离子方程式为:4H+ + 2Cl- + MnO2![]() Mn2+ + Cl2↑+2H2O,根据方程式可知,当0.5molMnO2反应时,生成的Cl2的物质的量为0.5mol,则在标准状况下,其体积为0.5mol×22.4L/mol=11.2L,故答案为:4H+ + 2Cl- + MnO2
Mn2+ + Cl2↑+2H2O,根据方程式可知,当0.5molMnO2反应时,生成的Cl2的物质的量为0.5mol,则在标准状况下,其体积为0.5mol×22.4L/mol=11.2L,故答案为:4H+ + 2Cl- + MnO2![]() Mn2+ + Cl2↑+2H2O;11.2L;
Mn2+ + Cl2↑+2H2O;11.2L;
(3)生成的氯气中含有水蒸气和挥发出的氯化氢,因此乙中饱和食盐水的作用是除去Cl2中的HCl;甲中浓硫酸的作用是干燥氯气(或除去氯气中的水蒸气),故答案为:除去Cl2中的HCl;干燥氯气(或除去氯气中的水蒸气);
(4)氯气具有强氧化性,能把碘化钾氧化单质碘,碘遇淀粉显蓝色。则如果有氯气产生,可观察到的现象是试纸变蓝,反应的化学方程式为:Cl2 + 2KI = 2KCl + I2,故答案为:试纸变蓝;Cl2 + 2KI = 2KCl + I2;
(5)根据题意易知,氢氧化钠吸收氯气生成等物质的量的次氯酸钠和氯酸钠,依据氧化还原反应规律可知,还有氯化钠和水生成,其反应的化学方程式为:4Cl2+8NaOH=6NaCl+NaClO+NaClO3+4H2O,则4Cl2![]() 8NaOH,则吸收标准状况下VL氯气,消耗的NaOH的物质的量为
8NaOH,则吸收标准状况下VL氯气,消耗的NaOH的物质的量为![]() ×2=
×2=![]() mol,故答案为:
mol,故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】用纯净的CaCO3与100 mL稀盐酸反应制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况下的体积),下列分析正确的是( )

A.OE段表示的平均速率最快
B.EF段,用盐酸表示该反应的平均反应速率为0.4 mol·L-1·min-1
C.OE、EF、FG三段中,该反应用二氧化碳表示的平均反应速率之比为2∶6∶7
D.F点收集到的CO2的量最多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于古籍中的记载说法不正确的是
A. 《本草纲目》“烧酒”条目下写道自元时始创其法,用浓酒和糟入甑,蒸令气上其清如水,味极浓烈,盖酒露也”。这里所用的“法”是指蒸馏
B. 《吕氏春秋·别类编》中“金(即铜)柔锡柔,合两柔则刚” 体现了合金硬度方面的特性
C. 《本草经集注》中关于鉴别硝石(KNO3)和朴硝(Na2SO4)的记载:“以火烧之,紫青烟起,乃真硝石也”,该方法应用了显色反应
D. 《抱朴子·金丹篇》中记载:“丹砂(HgS)烧之成水银,积变又成丹砂”,该过程发生了分解、化合、氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:

4种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是__.
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示.

①写出基态Cu原子的核外电子排布式__;金属铜采用下列__(填字母代号)堆积方式.

②写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来)__.
③水分子间存在氢键,请你列举两点事实说明氢键对水的性质的影响__.
④SO42﹣的空间构型是________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水AlCl3易升华,可用作有机合成的催化剂等。工业上以铝土矿(Al2O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下:

(1) 氯化炉中Al2O3、Cl2和C反应的化学方程式为____________________。
(2)用Na2SO3溶液可除去冷却器排出的尾气中的Cl2,此反应的离子方程式为__________。
(3)升华器中主要含有AlCl3和FeCl3,需加入少量Al,其作用是________。
(4)为测定制得的无水AlCl3产品(含杂质FeCl3)的纯度,称取16.25 g无水AlCl3样品,溶于过量的NaOH溶液中,过滤出沉淀物,沉淀物经洗涤、灼烧、冷却、称重,得其质量为0.32 g。
① 写出上述除杂过程中涉及的离子方程式___________、____________。
② AlCl3产品的纯度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列的说法,正确的是()
A.0.1mol Fe在0.lmol Cl2中充分燃烧,转移电子数为0.2NA
B.12mol/L的浓硫酸50ml与足量的Cu加热反应,得到SO2为0.3NA
C.1 mol Cl2与足量NaOH溶液反应得到电子数为2NA
D.1 mol Na2O2与足量水反应转移电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是金属镁和卤素单质(X2)反应的能量变化示意图.下列说法正确的是( )
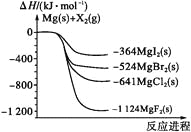
A. 由MgCl2制取Mg是放热过程
B. 热稳定性:MgI2>MgBr2>MgCl2>MgF2
C. 常温下氧化性:F2<Cl2<Br2<I2
D. 由图可知此温度下MgBr2(s)与Cl2(g)反应的热化学方程式为:MgBr2(s) + Cl2(g) ═ MgCl2(s) + Br2(g) △H = -117kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下所示4个装置图,以下说法中正确的是

A. ①装置可用于比较NaHCO3和Na2CO3的稳定性 B. 用酒精萃取溴水中的溴可选择②装置
C. 如③装置进行实验可看到酸性KMnO4溶液褪色 D. ④装置可用于实验室制取并收集少量SO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知甲为恒压容器、乙为恒容容器。相同条件下充入等物质的量NO2气体,且起始时体积相同。发生反应:2NO2(g)![]() N2O4(g) △H<0。一段时间后均达到平衡状态。下列说法中正确的是
N2O4(g) △H<0。一段时间后均达到平衡状态。下列说法中正确的是
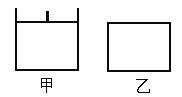
A. 平衡时NO2体积分数:甲<乙
B. 达到平衡所需时间,甲与乙相等
C. 该反应的平衡常数表达式K=c(N2O4)/c(NO2)
D. 若两容器内气体的压强保持不变,均说明反应已达到平衡状态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com