
| A. | 2-甲基-2-丁烯 | B. | 2,3-二甲基-1-丙烯 | ||
| C. | 3-甲基-1-丁烯 | D. | 2-甲基-1,3-丁二烯 |
分析 有机物分子中的不饱和键断裂,不饱和原子与其他原子或原子团相结合,生成新的化合物的反应是加成反应,采用逆推法,减去相邻碳原子上的氢原子,重新形成不饱和键,即可的原来的不饱和烃,再根据有机物的命名原则进行命名.
解答 解:(CH3)2CHCH2CH3,结构为 .5号碳原子与1号碳原子化学环境相同.
.5号碳原子与1号碳原子化学环境相同.
A.若2、3号碳原子各去掉1个H原子,形成的烯烃为2-甲基-2-丁烯,故A不选;
B.若1(或5号)、2号碳原子各去掉1个H原子,形成的烯烃为2-甲基-1-丁烯;若3、4号碳原子各去掉2个H原子,形成的炔烃为3-甲基-1-丁炔,无法得到2,3-二甲基-1-丙烯,故B选;
C.若3、4号碳原子各去掉1个H原子,形成的烯烃为3-甲基-1-丁烯,故C不选;
D.若1、2号碳原子各去掉1个H原子,同时3、4号碳原子各去掉1个H原子,形成的二烯烃为2-甲基-1,3-丁二烯,故D不选;
故选B.
点评 本题主要考查了加成反应与有机物的命名,难度不大,可以根据所学知识进行.加成反应的条件是有机物中必须含有不饱和键(如碳碳双键、碳碳三键等),逆推法是有机常用的推断方法.


科目:高中化学 来源: 题型:多选题
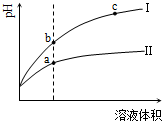
| A. | Ⅱ为盐酸稀释时的pH变化曲线 | |
| B. | a点Kw的数值比c点Kw的数值大 | |
| C. | b点酸的总浓度小于a点酸的总浓度 | |
| D. | b点溶液的导电性比c点溶液的导电性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
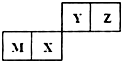
| A. | M与Z形成的化合物中只存在离子键 | |
| B. | X的最简单气态氢化物的热稳定性比Z的强 | |
| C. | 原子半径Z>Y | |
| D. | M的最高价氧化物对应水化物能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2,3-二甲基-4-乙基戊烷 | B. | 2-甲基3,4-二乙基戊烷 | ||
| C. | 2,4-二甲基-3-乙基己烷 | D. | 2,5-二甲基-3-乙基己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 )与P(
)与P( ),下列有关它们的说法中正确的是( )
),下列有关它们的说法中正确的是( )| A. | 二者的核磁共振氢谱中均只出现两种峰且峰面积之比为3:1 | |
| B. | 二者在NaOH醇溶液中均可发生消去反应 | |
| C. | 一定条件下,二者在NaOH溶液中均可发生取代反应 | |
| D. | Q的一氯代物只有1种,P的一溴代物有2种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:W>Z>Y>X>M | |
| B. | XZ2、X2M2、W2Z2均为共价化合物 | |
| C. | 由Z、M两种元素形成化合物的分子式一定为M2Z | |
| D. | 由 Y、Z、M 三种元素形成的化合物可以既有离子键,又有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.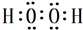 ,试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式Cu+2H++H2O2=Cu2++2H2O.
,试写出Cu、稀硫酸与X反应制备硫酸铜的离子方程式Cu+2H++H2O2=Cu2++2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标况下,22.4 L SO3中含有NA个SO3分子 | |
| B. | 1 mol/L NaCl溶液含有NA个Na+ | |
| C. | 1 mol Fe和足量稀硝酸反应产生22.4LNO | |
| D. | 16 g CH4中含有4 NA个C-H键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气态氢化物的稳定性:X>Y | |
| B. | 最高价氧化物对应的水化物的酸性:Y>X>W | |
| C. | Q可分别与X、Y、Z、W形成化学键类型相同的化合物 | |
| D. | Y的简单离子半径小于Z的简单离子半径 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com