
【题目】X、Y、Z、W代表四种短周期元素,有关它们的部分结构及性质如下表所示。
元素 | 部分结构信息 | 部分性质信息 |
X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2、X2O4等; |
Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氢化物 |
Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
按要求回答下列问题(注意不能用字母X、Y、Z、W作答):
(1)X的气态氢化物分子的电子式是______________;
(2)Z元素在周期表中的位置是__________________;
(3)X、Y、Z三元素的最高价氧化物对应水化物的酸性,由强到弱的顺序是(用化学式表示)_________________;
(4)实验室用X的氢化物的水溶液制取W的氢氧化物的方法是:(用离子方程式表示)_______________________________;
(5)写出Z的单质与二氧化硫的混合气体通入水中的离子反应方程式: __________________。
【答案】 ![]() 第三周期ⅦA族 HClO4>HNO3>H2CO3 Al3++3NH3·H2O===Al(OH)3↓+3NH
第三周期ⅦA族 HClO4>HNO3>H2CO3 Al3++3NH3·H2O===Al(OH)3↓+3NH![]() Cl2 + SO2 + 2H2O== 4H+ +2Cl- + SO42-
Cl2 + SO2 + 2H2O== 4H+ +2Cl- + SO42-
【解析】X的单质由双原子分子构成,分子中有14个电子,因此X的原子序数是14÷2=7,X是N;Y原子的次外层电子数等于最外层电子数的一半,且Y能形成多种气态氢化物,所以Y是C;Z原子的最外层电子数多于4,Z元素的最高正化合价与最低负化合价代数和等于6,说明是第第ⅦA族,即为Cl;W原子的最外层电子数等于2n-3(n为原子核外电子层数),化学反应中W原子易失去最外层电子形成Wn+,W是Al。则
(1)X的气态氢化物是氨气,属于共价化合物,氨气分子的电子式是![]() ;(2)Cl元素在周期表中的位置是第三周期ⅦA族;(3)X、Y、Z三元素的非金属性强弱顺序是Cl>N>C,非金属性越强,最高价氧化物水化物的酸性越强,则最高价氧化物对应水化物的酸性,由强到弱的顺序是HClO4>HNO3>H2CO3;(4)实验室用X的氢化物的水溶液制取W的氢氧化物氢氧化铝的方法是Al3++3NH3·H2O=Al(OH)3↓+3NH4+;(5)Z的单质氯气具有强氧化性,与二氧化硫的混合气体通入水中的离子反应方程式为Cl2 +SO2+2H2O=4H++2Cl-+SO42-。
;(2)Cl元素在周期表中的位置是第三周期ⅦA族;(3)X、Y、Z三元素的非金属性强弱顺序是Cl>N>C,非金属性越强,最高价氧化物水化物的酸性越强,则最高价氧化物对应水化物的酸性,由强到弱的顺序是HClO4>HNO3>H2CO3;(4)实验室用X的氢化物的水溶液制取W的氢氧化物氢氧化铝的方法是Al3++3NH3·H2O=Al(OH)3↓+3NH4+;(5)Z的单质氯气具有强氧化性,与二氧化硫的混合气体通入水中的离子反应方程式为Cl2 +SO2+2H2O=4H++2Cl-+SO42-。


科目:高中化学 来源: 题型:
【题目】化学与我们人类生活息息相关,下列说法不正确的是
A. 开发氢能、太阳能、风能、生物质能等是实现“低碳生活”的有效途径
B. 工业上,电解熔融MgCl2制金属镁
C. 研发使用高效催化剂,可提高反应中原料的转化率
D. “冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对十二烷基苯磺酸钠![]() 是常用洗涤剂的主要成分。
是常用洗涤剂的主要成分。
其结构可用图形![]() 来表示,端为链烃基,O端为极性基。根据这一结构特点,试分析和回答下列问题:
来表示,端为链烃基,O端为极性基。根据这一结构特点,试分析和回答下列问题:
(1)十二烷基苯磺酸钠分子在其水溶液表面分布的结构示意图应是下列各图中的____图(填写序号),理由是____________________________________。
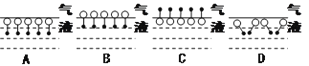
(2)进入介质(水)内部的十二烷基苯磺酸钠分子,可能会以下列结构形式中的____存在(填写序号),理由是____________________________________。
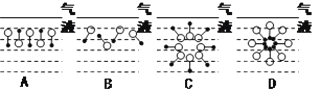
(3)工业合成对十二烷基苯磺酸钠的一种路线如下图所示:
![]()
![]()
请回答下列问题:
①产品中的亲油基是_______。
②由十二烷基苯制取对十二烷基苯磺酸的化学方程式为_________,反应类型为__________。
③在洗涤剂中添加酶制剂能促进污垢中的蛋白质(如奶渍、肉汤)等水解为可溶性的物质而被除去。使用加酶洗衣粉的水溶液中浸泡10~30min,水温在40~50℃最佳。加酶洗衣粉不宜在高温下、潮湿环境中贮存,也不宜久存。请解释原因_________________________________。
④过去使用的合成洗涤剂中常加入三聚磷酸钠(Na5P3O10)做助剂,它可使硬度大的洗涤水软化,对微细的无机粒子或油脂具有分散、乳化、胶溶作用,防止污渍再次沉积到衣物上;它还能维持水溶液的弱碱性,提高洗涤剂的去污能力和洗涤效果。但是,20世纪90年代以来,世界各国先后提出必须生产和使用无磷洗涤剂。请解释原因______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素W、X、Y、Z的原子序数依次增大,Y和Z位于同一主族。m、n、p均为由这些元素组成的二元化合物,甲、乙、丙为其中三种元素对应的单质,丙为淡黄色固体,易溶在XZ2中,n是一种二元弱酸。上述物质的转化关系如图所示(反应条件省略)。下列说法正确的是

A.原子半径:W<X<Y
B.W与X组成的化合物中只有极性键
C.Y与Z组成的化合物一定有漂白性
D.非金属性:Y>Z>X
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修5:有机化学基础】
D是一种催眠药,F是一种香料,它们的合成路线如下:

(1)A的化学名称是______,C中含氧官能团的名称为______。
(2)F的结构简式为______,A和E生成F的反应类型为______。
(3)A生成B的化学方程式为_______________。
(4)B与乙炔钠合成C的反应类型(酸化前)是_________;写出由C合成D的第二个反应的化学方程式___________________________________。
(5)同时满足下列条件的E的同分异构体有_____种(不含立体异构)。
①遇FeCl3溶液发生显色反应; ②能发生银镜反应
(6)以乙炔和甲醛为起始原料,选用必要的无机试剂合成1,3-丁二烯,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(化学组成为FeC2O4·2H2O)是一种淡黄色晶体粉末,是生产锂电池的原材料。已知FeC2O4·2H2O在300 ℃左右完全分解生成FeO、CO2、CO、H2O四种氧化物。某学习小组欲验证草酸亚铁晶体的分解产物。
I.甲组同学设计了如下实验装置:

(1)实验开始前,鼓入氮气的目的是____________。
(2)实验中,装置B中的现象是 。
(3)装置C中可观察到的现象是_________,由此可知草酸晶体分解的产物中有_______。
(4)设计实验验证装置A中黑色残留物不含有Fe3O4 (简要说明实验操作,现象和结论)。
II.乙组同学选用甲组实验中的装置A(接口用x表示)和下图所示的装置(可以重复选用)验证分解产物CO。
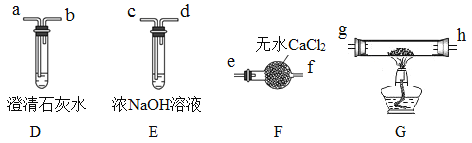
(5)乙组同学的实验装置中,依次连接的合理顺序为x→______g→h→a(用接口字母和“→”表示)。装置G反应管中盛有的物质是_______。能证明草酸晶体分解产物中有CO的现象是_______。
(6)按照题目提供的装置和要求设计的实验明显存在的一个不足是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把m mol的乙烯跟n mol H2混合于一密闭容器中,在适当条件下反应并生成p mol C2H6。若将所得的混合气体燃烧,并全部生成CO2和H2O,需要氧气的物质的量为(单位/mol) ( )
A. 3m+3p+![]()
![]() B. 3m+
B. 3m+![]()
![]() C. 3m+n D. 3m+
C. 3m+n D. 3m+![]()
![]() -2p
-2p
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用 NA 表示阿伏加德罗常数的值,下列说法正确的是( )
A. 17 g -OH 与 17 g OH-所含电子数均为 10NA
B. 标准状况下,11.2 L 的甲醇所含的氢原子数等于 2 NA
C. 在铅蓄电池放电时,正极增重 32g,转移的电子数为 NA
D. 1 mol 苯酚分子中含有的碳碳双键数为 3 NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com