
����Ŀ��25��ʱ���ı�0.1mol��L-1����RCOOH��Һ��pH����Һ��RCOOH���ӵ����ʵ���������(RCOOH)��֮�ı�[��֪��(RCOOH)=![]() ]��0.1mol��L-1����(HCOOH)��0.1mol��L-1����(CH3CH2COOH)��Һ����(RCOOH)��pH�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����(��֪���ԣ��������)( )
]��0.1mol��L-1����(HCOOH)��0.1mol��L-1����(CH3CH2COOH)��Һ����(RCOOH)��pH�Ĺ�ϵ��ͼ��ʾ������˵����ȷ����(��֪���ԣ��������)( )

A.ͼ��M�߶�Ӧ���DZ��ᣬN�߶�Ӧ�ļ���
B.CH3CH2COONa��ˮ��ƽ�ⳣ��Kh=10-10.25
C.��Ũ�ȵ�HCOONa��CH3CH2COONa������Һ�У�c(HCOO-)+c(OH-)��c(CH3CH2COO-)+c(OH-)
D.��0.1mol/L��HCOOH��Һ��0.1mol/L��HCOONa��Һ�������ϣ�������Һ�У�c(Na+)��c(HCOOH)��c(HCOO-)��c(OH-)��c(H+)
���𰸡�C
��������
A����֪���ԣ�������ᣬ����Խǿ������̶�Խ������RCOOH������ԽС����pH=3ʱ��M������RCOOH������С��N������RCOOH����������˵��M�ĵ���̶ȴ�����Һ��ͼ��M�߶�Ӧ���Ǽ��ᣬN�߶�Ӧ�ı��ᣬ��A����
B��pH=4.88ʱ�����������ӵ����ʵ�������Ϊ50%����c(CH3CH2COOH)=c(CH3CH2COO-)�����CH3CH2COOH)CH3CH2COO-+H+������̿�֪��lgK=lgc(H+)=-4.88��������ĵ��볣��Ka��c(H+)=10��4.88��CH3CH2COONa��ˮ��ƽ�ⳣ��Kh=![]() =10-9.12����B����
=10-9.12����B����
C��HCOONa��Һ�д��ڵ���غ㣺c(HCOO-)+c(OH-)=c(Na+)+c(H+)��CH3CH2COONa����Һ�д��ڵ���غ㣺c(CH3CH2COO-)+c(OH-)=c(Na+)+c(H+)����Ũ�ȵ�HCOONa��CH3CH2COONa������Һ��c(Na+)��ȣ���֪���ԣ�������ᣬ��HCOO-��ˮ��̶�С��CH3CH2COO-��ˮ��̶ȣ� HCOONa��Һ�е�c(OH-)С��CH3CH2COONa��Һ�е�c(OH-)��HCOONa��Һ�е�c(H+)����CH3CH2COONa��Һ�е�c(H+)����HCOONa��Һ��c(Na+)+c(H+)����CH3CH2COONa��Һ�е�c(Na+)+c(H+)����c(HCOO-)+c(OH-)��c(CH3CH2COO-)+c(OH-)����C��ȷ��
D����0.1mol/L��HCOOH��Һ��0.1mol/L��HCOONa��Һ�������ϣ�������̴���ˮ����̣�������Һ�����ԣ���c(OH-)��c(H+)����D����
��ѡC��


 ����˼ά�żӿ���ϵ�д�
����˼ά�żӿ���ϵ�д� �����Ծ�ϵ�д�
�����Ծ�ϵ�д� �ο�����������100��ϵ�д�
�ο�����������100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������仯�������ճ�����������Ӧ�ù㷺���о������仯�����Ӧ�������ش�
��1��������Ԫ�ص�����ֻ�л�ԭ����___��
A��Fe B��FeCl2 C��FeCl3 D��Fe2O3
��2��������ȱ��ʱ��������Ҫ�Բ�������Ʒ�������ܹ����յ���+2�۵���������+2�۵��������ױ�������
����μ���ij���岹��������Ԫ���ѱ�������д���������̡������ۡ���___��
�ڷ���ά����C����ʹʳ���е�����������ת��Ϊ���������ӡ��ɴ˿���֪��ά����C����___���ѧ���ʣ���
��3��������أ�K2FeO4����һ�����͡���Ч�������ɫˮ��������ʪ���Ʊ�������أ�K2FeO4���ķ�Ӧ��ϵ������������Fe(OH)3��C1O-��OH-��FeO42-��Cl-��H2O��д������ƽʪ���Ƹ�����ص����ӷ�Ӧ����ʽ��__Fe(OH)3+__ClO-+__=__FeO42-+__Cl-+___
��4����ҵ�����Ȼ�����ʴͭ���������·�塣ij����ʦΪ�˴�ʹ�ù��ĸ�ʴ��Һ�л���ͭ��������Ȼ������壬���������в��裺
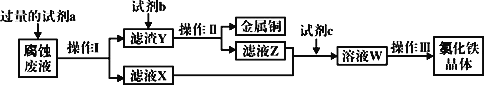
�ش��������⣺
���Լ�a��___������I�õ��IJ����������ձ�����������___��
����ҺX��Z�ж���ͬһ�����ʣ�����ת��Ϊ��ҺW�����ӷ���ʽΪ___��
��д��FeCl3��Һ�����ͭ������Ӧ�����ӷ���ʽ��___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)���Ѿ���SO2���ʹ����Ϊ0.25g��L��1��ȡ300.00mL���Ѿƣ�ͨ���ʵ��ķ���ʹ����SO2ȫ���ݳ�����H2O2����ȫ������ΪH2SO4��Ȼ����0.0900mol��L��1NaOH����Һ���еζ���
�ٵζ�ǰ������ʱ��Ӧѡ����ͼ�е�___(�����)

������50mL�ζ��ܽ���ʵ�飬���ζ����е�Һ���ڿ̶���10�����������Һ������___(�����)��
��=10mL ��=40mL ��<10 mL ��>40 mL��
�������ζ�ʵ�������ζ��յ�ʱ��Һ��pH=8.8����ѡ���ָʾ��Ϊ______��ѡ���ָʾ��ʱ����жϷ�Ӧ����ζ��յ㣺______��
�ܵζ����յ�ʱ������NaOH��Һ25.00mL�������Ѿ���SO2����Ϊ___g��L��1���ζ��յ����ʱ���ӿ̶��ߣ�����������ʵ��ֵ______������ƫ��������ƫ����������Ӱ��������
(2)ijѧ����0.100molL-1��KOH����Һ�ζ�δ֪Ũ�ȵ����ᣬ�����Ϊ��
A.��ȡ20mL����������Һע��ྻ����ƿ�У�������2��3�η�̪��
B.�ñ���Һ��ϴ�ζ���2��3�Σ�
C.��ʢ�б���Һ�ļ�ʽ�ζ��̶ܹ��ã����ڵζ���ʹ���촦������Һ��
D.ȡ��KOH��Һע���ʽ�ζ������̶���0������2��3cm ����
E.����Һ������0������0�����¿̶ȣ����¶�����
F.����ƿ���ڵζ������棬�ñ�KOH��Һ�ζ����յ㲢���¿̶ȡ�
ʵ���� | KOH��Һ��Ũ��(mol/L) | �ζ����ʱ��KOH��Һ��������(mL) | ����������Һ�����(mL) |
1 | 0.10 | 22.62 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
����ȷ���������˳���ǣ��������ĸ��д��_________��
�ڸ����������ݣ��ɼ�����������Ũ��ԼΪ_______��������λ��Ч���֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��GMA������Ϳ�ϡ����ӽ�����֬����ī���ϼ��ȣ�ͨ����������Ӧ�Ʊ�����Ӧ���£�
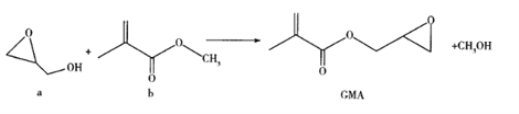
����˵��������ǣ� ��
A.��a��Ϊͬ���칹�������ֻ��1��
B.b�����е�����Cԭ�Ӻ�Oԭ�ӿ�����ͬһƽ���ڣ��������ֹ�����
C.GMA�ķ���ʽΪC7H10O3
D.GMA����NaOH��Һ����ˮ������KMnO4��Һ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA�ǰ����ӵ�������ֵ������˵����ȷ����
A. 16.25gFeCl3ˮ���γɵ�Fe(OH)3����������Ϊ0.1NA
B. ��״���£�11.2 L�������ϩ������к���ԭ����ĿΪ2NA
C. pH=1��H3PO4��Һ�У�����0.1NA��H+
D. 10 g��D2O�к��е����������������ֱ�Ϊ5NA��4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijС��Ƚ�Cl-��Br-��I- �Ļ�ԭ�ԣ�ʵ�����£�
ʵ��1 | ʵ��2 | ʵ��3 | |
װ�� |
|
|
|
���� | ��Һ��ɫ�����Ա仯����պŨ��ˮ�IJ����������Թܿڣ��������� | ��Һ��ƣ���ʪKI������ֽ�����Թܿڣ����� | ��Һ������ɫ����������Һ�����ʵ� |
���ж�ʵ��ķ�������������
A. ʵ��1�У�������NH4Cl B. ����ʵ��1��ʵ��2�жϻ�ԭ�ԣ�Br-��Cl-
C. ����ʵ��3�жϻ�ԭ�ԣ�I-��Br- D. ����ʵ��������ŨH2SO4��ǿ�����ԡ��ѻӷ��Ե�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ἰ�����ο������齺�����ࡢ����������ʳƷ���־�����Ҳ�ɹ㷺Ӧ������ҩ�ͻ�����ҵ��ijͬѧ�����üױ���������Ӧ�Ʊ������ᡣ��Ҫʵ��װ��(��������װ��)��ͼ��ʾ��
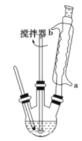
��Ӧԭ����
![]() +2KMnO4��
+2KMnO4��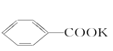 +KOH+2MnO2��+H2O
+KOH+2MnO2��+H2O
![]() +HCl��
+HCl��![]() +KCl
+KCl
ʵ�鷽������һ�����ļױ���KMnO4��Һ����������ƿ�У���90��ʱ��Ӧһ��ʱ���ֹͣ��Ӧ������ͼ���̷���������Ტ����δ��Ӧ�ļױ���
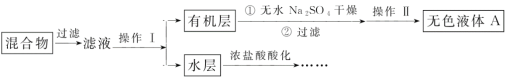
(1)��ɫҺ��A�Ľṹ��ʽΪ___��������Ϊ___��
(2)�����Һ����ɫ��Ҫ�ȼӱ������������Һ�����˺��ٽ��в��������ӱ������������Һ��Ŀ����___��д���÷�Ӧ�����ӷ���ʽ��___��
(3)��ȴˮӦ�ô�������___(����a������b��)�����룻
(4)Ҫ����ˮ�����õ������ᾧ�壬Ӧ�������в�������ȷ�IJ���˳����___(��ѡ����ĸ)��
A.�ữ B.���� C.����Ũ�� D.��ȴ�ᾧ
(5)���Ȳⶨ����ȡ1.22g��Ʒ�����100mL��Һ��ȡ����25.00mL��Һ����KOH��Һ���еζ�������KOH�����ʵ���Ϊ2.40��10-3mol�����Ʒ�б��������������Ϊ__��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ̽��Na2O2��H2O�ķ�Ӧ������������ʵ�飺
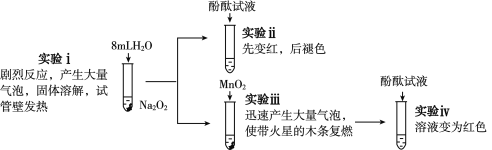
�й�˵������ȷ���ǣ� ��
A.ʵ�颡�з�����Ӧ�Ļ�ѧ����ʽΪ2Na2O2+2H2O===4NaOH+O2��
B.ʵ�颣��MnO2��H2O2�ֽⷴӦ�Ĵ���
C.�ۺ�ʵ�颡�͢�����˵��Na2O2��H2O��Ӧ��H2O2����
D.�ۺ�ʵ�颢�͢�����˵��ʹ��̪��ɫ����O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����º����ܱ������з�����Ӧ2A(g)��B(g)![]() 2C(g)������Ӧ��A��Ũ����0.1 mol��L��1����0.06 mol��L��1��20 s����ô��0.06 mol��L��1����0.036 mol��L��1�����ʱ��Ϊ(����)
2C(g)������Ӧ��A��Ũ����0.1 mol��L��1����0.06 mol��L��1��20 s����ô��0.06 mol��L��1����0.036 mol��L��1�����ʱ��Ϊ(����)
A. ����10 s B. ����12 s
C. ����12 s D. ��12 s
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com