
ЎѕМвДїЎїПЦУРAЎўBЎўCЎўDЎўEОеЦЦѕщїЙИЬУЪЛ®µД№ММеОпЦКЈ¬КЗУЙТФПВМṩµДјёЦЦАлЧУЧйіЙ![]() ГїЦЦАлЧУЦ»ДЬУГТ»ґО
ГїЦЦАлЧУЦ»ДЬУГТ»ґО![]() Јє
Јє
СфАлЧУ |
|
ТхАлЧУ |
|
ПЦ·Ц±рЅшРРИзПВКµСйЈє
![]() Ѕ«DУлEµДИЬТє»мєПјУИИЈ¬ІъЙъУРґМј¤РФЖшО¶µДЖшМе
Ѕ«DУлEµДИЬТє»мєПјУИИЈ¬ІъЙъУРґМј¤РФЖшО¶µДЖшМе
![]() Ѕ«BУлEµДИЬТє»мєПЈ¬ІъЙъ°ЧЙ«іБµнЈ¬ПтёГіБµнЦРјУИлЧгБїµДПЎПхЛбЈ¬іБµнІї·ЦИЬЅв
Ѕ«BУлEµДИЬТє»мєПЈ¬ІъЙъ°ЧЙ«іБµнЈ¬ПтёГіБµнЦРјУИлЧгБїµДПЎПхЛбЈ¬іБµнІї·ЦИЬЅв
![]() ФЪіЈОВПВУГpHКФЦЅІв¶ЁИЬТєAµД
ФЪіЈОВПВУГpHКФЦЅІв¶ЁИЬТєAµД![]()
ПВБРЛµ·ЁІ»ХэИ·µДКЗ![]()
A.ОпЦКEµД»ЇС§КЅОЄ![]() B.ОпЦКDЦРТ»¶Ёє¬УР
B.ОпЦКDЦРТ»¶Ёє¬УР![]()
C.ДСТФИ·¶ЁОпЦКAµДЧйіЙD.ОпЦКCµД»ЇС§КЅКЗ![]()
Ўѕґр°ёЎїC
ЎѕЅвОцЎї
![]() Ѕ«DУлEµДИЬТє»мєПјУИИЈ¬ІъЙъУРґМј¤РФЖшО¶µДЖшМеЈ¬У¦ОЄ°±ЖшЈ¬DУлEє¬УР
Ѕ«DУлEµДИЬТє»мєПјУИИЈ¬ІъЙъУРґМј¤РФЖшО¶µДЖшМеЈ¬У¦ОЄ°±ЖшЈ¬DУлEє¬УР![]() Ўў
Ўў![]() Ј¬ФтУРТ»ЦЦОЄNaOH»т
Ј¬ФтУРТ»ЦЦОЄNaOH»т![]() Ј»
Ј»
![]() Ѕ«BУлEµДИЬТє»мєПЈ¬ІъЙъ°ЧЙ«іБµнЈ¬ПтёГіБµнЦРјУИлЧгБїµДПЎПхЛбЈ¬іБµнІї·ЦИЬЅвЈ¬їЙЦЄEОЄ
Ѕ«BУлEµДИЬТє»мєПЈ¬ІъЙъ°ЧЙ«іБµнЈ¬ПтёГіБµнЦРјУИлЧгБїµДПЎПхЛбЈ¬іБµнІї·ЦИЬЅвЈ¬їЙЦЄEОЄ![]() Ј¬ЙъіЙіБµнОЄБтЛб±µЈ¬BОЄ
Ј¬ЙъіЙіБµнОЄБтЛб±µЈ¬BОЄ![]() Ј»
Ј»
![]() ФЪіЈОВПВУГpHКФЦЅІв¶ЁИЬТєAµД
ФЪіЈОВПВУГpHКФЦЅІв¶ЁИЬТєAµД ![]() Ј¬ИЬТєіКјоРФЈ¬У¦ОЄМјЛбСОЈ¬У¦ОЄМјЛбДЖЎЈ
Ј¬ИЬТєіКјоРФЈ¬У¦ОЄМјЛбСОЈ¬У¦ОЄМјЛбДЖЎЈ
УЙґЛїЙЦЄCЎўDє¬УР![]() Ўў
Ўў![]() БЅЦЦТхАлЧУЈ¬¶шCУ¦є¬УР
БЅЦЦТхАлЧУЈ¬¶шCУ¦є¬УР![]() Ј¬ФтЦ»ДЬОЄ
Ј¬ФтЦ»ДЬОЄ![]() Ј¬
Ј¬
јґAОЄМјЛбДЖЈ¬BОЄБтЛбГѕЈ¬CОЄВИ»ЇМъЈ¬DОЄµв»Їп§ Ј¬EОЄЗвСх»Ї±µЈ¬ТФґЛЅвґрёГМвЎЈ
A.УЙТФЙП·ЦОцїЙЦЄОпЦКEµД»ЇС§КЅОЄ![]() Ј¬№КAХэИ·Ј»
Ј¬№КAХэИ·Ј»
B.УЙ![]() їЙЦЄІъЙъУРґМј¤РФЖшО¶µДЖшМеЈ¬ОпЦКDЦРТ»¶Ёє¬УР
їЙЦЄІъЙъУРґМј¤РФЖшО¶µДЖшМеЈ¬ОпЦКDЦРТ»¶Ёє¬УР![]() Ј¬№КBХэИ·Ј»
Ј¬№КBХэИ·Ј»
C.УЙКµСй![]() їЙЦЄAµД
їЙЦЄAµД![]() Ј¬ИЬТєіКјоРФЈ¬У¦ОЄМјЛбСОЈ¬ОЄМјЛбДЖЈ¬№КCґнОуЈ»
Ј¬ИЬТєіКјоРФЈ¬У¦ОЄМјЛбСОЈ¬ОЄМјЛбДЖЈ¬№КCґнОуЈ»
D.УЙТФЙП·ЦОцїЙЦЄОпЦКCµД»ЇС§КЅКЗ![]() Ј¬№КDХэИ·ЎЈ
Ј¬№КDХэИ·ЎЈ
№КСЎЈєCЎЈ



| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїіЈОВПВЈ¬ПВБРёчЧйАлЧУФЪЦё¶ЁИЬТєДЬґуБї№ІґжµДКЗ
A.pHЈЅ1µДИЬТєЦРЈєFe2Ј«ЎўNO3-ЎўSO42-ЎўNaЈ«
B.УЙЛ®µзАлµДc(HЈ«)ЈЅ1ЎБ10Ј14molЎ¤LЈ1µДИЬТєЦРЈєCa2Ј«ЎўKЈ«ЎўClЈЎўHCO3-
C.![]() ЈЅ1012µДИЬТєЦРЈєNH4+ЎўAl3Ј«ЎўNO3-ЎўClЈ
ЈЅ1012µДИЬТєЦРЈєNH4+ЎўAl3Ј«ЎўNO3-ЎўClЈ
D.c(Fe3Ј«)ЈЅ0.1 molЎ¤LЈ1µДИЬТєЦРЈєKЈ«ЎўClOЈЎўSO42-ЎўSCNЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїТСЦЄБтґъБтЛбДЖФЪЛбРФМхјюПВ»б·ўЙъ·ґУ¦Јє![]() Ј¬ПВ±нЦРµДБЅЦЦИЬТє»мєПЈ¬іцПЦ»лЧЗµДПИєуЛіРтКЗЈЁ Ј©
Ј¬ПВ±нЦРµДБЅЦЦИЬТє»мєПЈ¬іцПЦ»лЧЗµДПИєуЛіРтКЗЈЁ Ј©
ЧйєЕ | БЅЦЦИЬТєµДОВ¶И |
| ПЎБтЛбµДМе»эЎўЕЁ¶И |
ўЩ | 15Ўж | 10mL0.1mol/L | 50mL0.05mol/L |
ўЪ | 15Ўж | 10mL0.05mol/L | 10mL0.1mol/L |
ўЫ | 25Ўж | 10mL0.05mol/L | 10mL0.1mol/L |
ўЬ | 25Ўж | 10mL0.1mol/L | 30mL0.07mol/L |
A.ўЬўЩўЪўЫB.ўЫўЬўЪўЩ
C.ўЬўЫўЪўЩD.ўЬўЫўЩўЪ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїБЧ»ЇВБЎўБЧ»ЇРїЎўБЧ»ЇёЖУлЛ®·ґУ¦ІъЙъёЯ¶ѕµДPH3ЖшМеЈЁИЫµгОЄ-132ЎжЈ¬»№ФРФЗїЎўТЧЧФИјЈ©Ј¬їЙУГУЪБёКіС¬ХфЙ±іжЎЈОАЙъ°ІИ«±кЧј№ж¶ЁЈєµ±БёКіЦРБЧ»ЇОпЈЁТФPH3јЖЈ©µДє¬БїµНУЪ0.05mgЎ¤kg-1К±ЛгєПёсЎЈїЙУГТФПВ·Ѕ·ЁІв¶ЁБёКіЦРІРБфµДБЧ»ЇОпє¬БїЈє
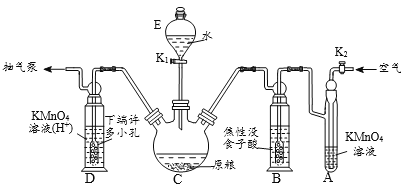
ЎѕІЩЧчБчіМЎї°ІЧ°ОьКХЧ°ЦГЎъPH3µДІъЙъУлОьКХЎъЧЄТЖKMnO4ОьКХИЬТєЎъСЗБтЛбДЖ±кЧјИЬТєµО¶ЁЎЈ
ЎѕКµСйЧ°ЦГЎїCЦРКў100 gФБёЈ¬DЦРКўУР 20.00 mL 1.12ЎБ10-4 mol L-1KMnO4ИЬЈЁH2SO4Лб»Ї)ЎЈ
Зл»ШґрПВБРОКМвЈє
ЈЁ1Ј©ТЗЖчCµДГыіЖКЗ_________Ј»ФБёЧоєГПИґтіЙ·ЫД©Ј¬ЖдФТтКЗ_____________ЎЈ
ЈЁ2Ј©БЧ»ЇёЖУлЛ®·ґУ¦УР»ЇС§·ЅіМКЅОЄ_____________________________________Ј»јмІйХыМЧЧ°ЦГЖшГЬРФБјєГµД·Ѕ·ЁКЗ_______________________________________ЎЈ
ЈЁ3Ј©AЦРКўЧ°KMnO4ИЬТєµДЧчУГКЗіэИҐїХЖшЦРµД»№ФРФЖшМеЈ»BЦРКўЧ°Ѕ№РФГ»КіЧУЛбµДјоРФИЬТєЈ¬ЖдЧчУГКЗОьКХїХЖшЦРµДO2Ј¬·АЦ№___________Ј»НЁИлїХЖшµДЧчУГКЗ____________ЎЈ
ЈЁ4Ј©DЦРPH3±»Сх»ЇіЙБЧЛбЈ¬Лщ·ўЙъ·ґУ¦µДАлЧУ·ЅіМКЅОЄ_________________________ЎЈ
ЈЁ5Ј©°СDЦРОьКХТєЧЄТЖЦБИЭБїЖїЦРЈ¬јУЛ®ПЎКНЦБ250mLЈ¬ИЎ25.00mLУЪЧ¶РОЖїЦРЈ¬УГ5.0ЎБ10-5mol L-1µДNa2SO3±кЧјИЬТєµО¶ЁКЈУаµДKMnO4ИЬТєЈ¬ПыєД±кNa2SO3ЧјИЬТє11.00mLЈ¬ФтёГФБёЦРБЧ»ЇОпЈЁТФPH3јЖЈ©µДє¬БїОЄ______mg kg-1Ј¬ёГФБёЦКБї________ЈЁМоЎ°єПёсЎ±»тЎ°І»єПёсЎ±Ј©ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїОТ№ъєЅМмєЅїХКВТµХфХфИХЙПЈ¬єЅМмєЅїХµД№ШјьјјКхКЗ»рјэЈ¬»рјэИјБПУРТєЗвЎўТТИІ![]() ЎўјЧНйЎўГєУНЎўлВ
ЎўјЧНйЎўГєУНЎўлВ![]() µИЎЈЗл»ШґрПВБРОКМвЈє
µИЎЈЗл»ШґрПВБРОКМвЈє
ЈЁ1Ј©ТСЦЄлВµДЅб№№јтКЅїЙ±нКѕОЄ![]() ЎЈ
ЎЈ
ўЩлВ·ЦЧУЦРµД»ЇС§јьАаРНОЄ _______________________ЎЈ
ўЪлВФЪСхЖшЦРИјЙХЙъіЙОЮ¶ѕµДОпЦКЈ¬Фт·ґУ¦ЦРлВ¶ПБСµД»ЇС§јьУРNЎЄHјьЎў_______________________Ј¬РВРОіЙµД»ЇС§јьУР_______________________ ЎЈ
ўЫёщѕЭлВИјЙХ№эіМЦРµДДЬБї±д»ЇЈ¬ЛµГч·ґУ¦ОпДЬБїЦ®єН_______________________ ЈЁМоЎ°ґуУЪЎ±Ў°µИУЪЎ±»тЎ°РЎУЪЎ±Ј©ЙъіЙОпДЬБїЦ®єНЎЈ
ЈЁ2Ј©ЗвИјБПЖыіµЦРЗвµДИјЙХУл»рјэЦРЗвµДИјЙХЧоґуµДІ»Н¬ФЪУЪЗ°ХЯК№УГµДКЗїХЖшЧчСх»ЇјБЈ¬¶шєуХЯК№УГµДКЗТєСхЎЈ»рјэЦРІ»ДЬК№УГТє»ЇїХЖшЈ¬ФТтКЗ_______________________ ЎЈ
ЈЁ3Ј©»рјэ·ўЙдЗ°Ј¬µ±ТєЗвЎўТєСхјУµЅТ»¶ЁБїєуЈ¬јјКхИЛФ±»№ТЄІ»НЈµШІ№јУЈ¬ЗлДгЛµіцХвЦЦЧц·ЁµДФТт_______________________ ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїТСЦЄH2O2ЎўKMnO4ЎўNaClOЎўK2Cr2O7ѕщѕЯУРЗїСх»ЇРФЎЈЅ«ИЬТєЦРµДCu2Ј«ЎўFe2Ј«ЎўFe3Ј«іБµнОЄЗвСх»ЇОпЈ¬РиИЬТєµДpH·Ц±рОЄ6.4Ўў9.6Ўў3.7ЎЈПЦУРє¬FeCl2ФУЦКµДВИ»ЇНѕ§Ме(CuCl2Ў¤2H2O)Ј¬ОЄЦЖИЎґїѕ»µДCuCl2Ў¤2H2OЈ¬КЧПИЅ«ЖдЦЖіЙЛ®ИЬТєЈ¬И»єу°ґНјКѕІЅЦиЅшРРМбґїЈє
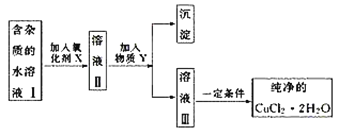
Зл»ШґрПВБРОКМвЈє
ЈЁ1Ј©±ѕКµСйЧоККєПµДСх»ЇјБXКЗ___(МоРтєЕ)ЎЈ
AЈ®K2Cr2O7 BЈ®NaClO CЈ®H2O2 DЈ®KMnO4
ЈЁ2Ј©ОпЦКYКЗ____ЎЈ
ЈЁ3Ј©±ѕКµСйУГјУјоіБµн·ЁДЬІ»ДЬґпµЅДїµДЈї___Ј¬ФТтКЗ___ЎЈ
ЈЁ4Ј©іэИҐFe3Ј«µДУР№ШАлЧУ·ЅіМКЅКЗ____ЎЈ
ЈЁ5Ј©јУСх»ЇјБµДДїµДКЗ____ЎЈ
ЈЁ6Ј©ЧоєуДЬІ»ДЬЦ±ЅУХф·ўЅбѕ§µГµЅCuCl2Ў¤2H2Oѕ§Ме___Ј¬У¦ИзєОІЩЧч___ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї·ыєП·ЦЧУКЅЎ°C6H6Ў±µД¶аЦЦїЙДЬЅб№№ИзНјЛщКѕЈ¬ПВБРЛµ·ЁХэИ·µДКЗ

A. 1Ў«5¶ФУ¦µДЅб№№ЦРДЬК№деµДЛДВИ»ЇМјИЬТєНКЙ«µДУР4ёц
B. 1Ў«5¶ФУ¦µДЅб№№ЦРТ»ВИИЎґъОпЦ»УР1ЦЦµДУР3ёц
C. 1Ў«5¶ФУ¦µДЅб№№ЦРЛщУРФЧУѕщїЙДЬґ¦УЪН¬Т»ЖЅГжµДУР1ёц
D. 1Ў«5¶ФУ¦µДЅб№№ѕщДЬУлЗвЖшФЪТ»¶ЁМхјюПВ·ўЙъјУіЙ·ґУ¦
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїДі100mLИЬТєїЙДЬє¬УР![]() Ўў
Ўў![]() Ўў
Ўў![]() Ўў
Ўў![]() Ўў
Ўў![]() Ўў
Ўў![]() ЦРµДИфёЙЦЦЈ¬ИЎёГИЬТєЅшРРБ¬РшКµСйЈ¬КµСй№эіМИзНјЛщКѕ
ЦРµДИфёЙЦЦЈ¬ИЎёГИЬТєЅшРРБ¬РшКµСйЈ¬КµСй№эіМИзНјЛщКѕ![]() ЛщјУКФјБѕщ№эБїЈ¬ЖшМеИ«ІїТЭіц
ЛщјУКФјБѕщ№эБїЈ¬ЖшМеИ«ІїТЭіц![]()

ПВБРЛµ·ЁТ»¶ЁХэИ·µДКЗ![]()
A.ИЬТєЦРТ»¶Ёє¬УР![]() Ј¬
Ј¬![]() ЕЁ¶ИКЗ
ЕЁ¶ИКЗ![]()
B.ИЬТєЦРЦ»УР![]() Ўў
Ўў![]() Ўў
Ўў![]() АлЧУ
АлЧУ
C.ИЬТєЦРїЙДЬє¬УР![]() Ј¬Т»¶ЁГ»УР
Ј¬Т»¶ЁГ»УР![]()
D.ИЎФИЬТєЙЩРнјУИлПхЛбЛб»ЇµД![]() ИЬТєјмСйКЗ·сУР
ИЬТєјмСйКЗ·сУР![]()
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїДіОЮЙ«ИЬТєЦРЦ»їЙДЬИЬУР![]() Ўў
Ўў![]() Ўў
Ўў![]() Ўў
Ўў![]() Ўў
Ўў![]() Ўў
Ўў![]() Ўў
Ўў![]() Ўў
Ўў![]() Ўў
Ўў![]() µИАлЧУЦРµДјёЦЦАлЧУЎЈОЄ·ЦОцЖдЧйіЙЈ¬ПЦЅшРРИзПВКµСйЈє
µИАлЧУЦРµДјёЦЦАлЧУЎЈОЄ·ЦОцЖдЧйіЙЈ¬ПЦЅшРРИзПВКµСйЈє
![]() ИЎ10mLёГИЬТєУЪКФ№ЬЦРµОјУЧгБїµД
ИЎ10mLёГИЬТєУЪКФ№ЬЦРµОјУЧгБїµД![]() ИЬТєЈ¬јУПЎПхЛбЛб»Їєу№эВЛµГµЅ
ИЬТєЈ¬јУПЎПхЛбЛб»Їєу№эВЛµГµЅ![]() °ЧЙ«іБµнјЧЈ®
°ЧЙ«іБµнјЧЈ®
![]() ИЎЙПКц·ґУ¦єуµДВЛТєЈ¬јУИл
ИЎЙПКц·ґУ¦єуµДВЛТєЈ¬јУИл![]() ИЬТєОґјыіБµнІъЙъЈ®
ИЬТєОґјыіБµнІъЙъЈ®
![]() БнИЎ10mLёГИЬТєУЪКФ№ЬЦРЈ¬µОјУNaOHИЬТєІъЙъ°ЧЙ«іБµнТТЈ¬µ±јУИлNaOHµДОпЦКµДБїОЄ
БнИЎ10mLёГИЬТєУЪКФ№ЬЦРЈ¬µОјУNaOHИЬТєІъЙъ°ЧЙ«іБµнТТЈ¬µ±јУИлNaOHµДОпЦКµДБїОЄ![]() К±Ј¬іБµнµДБїґпµЅЧоґуЈ»јМРшµОјУNaOHИЬТєІўјУИИЈ¬їЄКјІъЙъЖшМе±ыЈ¬КХјЇЖшМе±ыЈ¬Ме»э»»ЛгіЙ±кїцПВОЄ
К±Ј¬іБµнµДБїґпµЅЧоґуЈ»јМРшµОјУNaOHИЬТєІўјУИИЈ¬їЄКјІъЙъЖшМе±ыЈ¬КХјЇЖшМе±ыЈ¬Ме»э»»ЛгіЙ±кїцПВОЄ![]() јЩЙи±ыИ«ІїТЭіц
јЩЙи±ыИ«ІїТЭіц![]() Ј¬ЧоєуіБµнНкИ«ИЬЅвЎЈ
Ј¬ЧоєуіБµнНкИ«ИЬЅвЎЈ
ПВБРНЖ¶ПХэИ·µДКЗ![]()
A.їП¶ЁУР![]() Ўў
Ўў![]() Ўў
Ўў![]() Ўў
Ўў![]()
B.їП¶ЁУР![]() Ўў
Ўў![]() Ўў
Ўў![]()
C.їП¶ЁГ»УР![]() Ўў
Ўў![]() Ўў
Ўў![]()
D.їП¶ЁГ»УР![]() Ўў
Ўў![]() Ўў
Ўў![]()
Ійїґґр°ёєНЅвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com