
【题目】对于A2+3B2 ![]() 2C的反应来说,以下化学反应速率的表示中,反应速度最慢的是
2C的反应来说,以下化学反应速率的表示中,反应速度最慢的是
A. v(B2)=0.8 mol/(L·s)B. v(B2)= 3mol/(L·min)
C. v(C)=0.6 mol/(L·s)D. v(A2)=0.4 mol/(L·s)
【答案】B
【解析】
都转化为用B2物质表示的反应速率,速率单位用mol/(L·s)表示,然后再比较大小。
A. v(B2)=0.8 mol/(L·s),
B. v(B2)=3mol/(L·min)=0.05 mol/(L·s);
C. v(C)=0.6 mol/(L·s),则根据速率比等于化学方程式计量数的比,可知v(B2)=![]() v(C)=
v(C)=![]() ×0.6 mol/(L·s)=0.9 mol/(L·s);
×0.6 mol/(L·s)=0.9 mol/(L·s);
D. v(A2)=0.4 mol/(L·s),根据速率比等于化学方程式计量数的比,可知v(B2)=3v(A2)=1.2 mol/(L·s),故反应速率最慢的是v(B2)=3mol/(L·min)=0.05 mol/(L·s),
故选项B符合题意。


科目:高中化学 来源: 题型:
【题目】合理使用食品添加剂既不会影响人体健康,又能有效改善食物品质和色、香、味,但有 些物质严禁用作食品添加剂.下列做法正确的是( )
A.二氧化硫用作银耳的漂白剂B.胡萝卜素用作饮料的调味剂
C.次氯酸钠用作饼干的膨松剂D.苯甲酸钠用作火腿肠的防腐剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,请回答:
族 周期 | I A | II A | III A | IV A | V A | VI A | VII A | 0 |
1 | ① | |||||||
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
4 | ⑨ | ⑩ |
(1)元素⑦的原子结构示意图为_____;元素⑩的名称为______;
(2)在这些元素中,化学性质最活泼的金属元素是____(填元素符号,下同),最不活泼的元素是___;原子半径最小的元素是_____;
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是___(填化学式,下同);具有两性的是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学称取 9 g 淀粉溶于水,测定淀粉的水解百分率,其程序如下:
![]()
(1)各步所加的试剂A为__________,B__________,C__________。
(2)________(填“可以”或“不可以”)只加A溶液而不加B溶液,原因是____________________。
(3)当析出2.16g单质沉淀时,淀粉的水解率为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】砷为VA族元素,金属冶炼过程产生的含砷有毒废弃物需处理与检测。
I.冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:
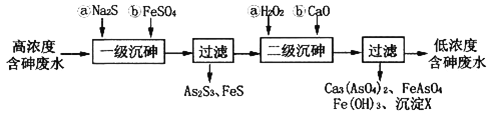
已知:①As2S3与过量的S2-存在以下反应:As2S3(s)+3S2-(aq) ![]() 2AsS33-(aq);
2AsS33-(aq);
②亚砷酸盐的溶解性大于相应砷酸盐。
(1)亚砷酸中砷元素的化合价为________;砷酸的第一步电离方程式为________________________。
(2)“一级沉砷”中FeSO4的作用是___________;“二级沉砷”中H2O2与含砷物质反应的化学方程式为______________________________________________________________。
(3)沉淀X为___________(填化学式)。
Ⅱ.冶炼废渣中的砷元素主要以As2S3的形式存在,可用古氏试砷法半定量检测(As的最低检出限为3.0×10-6g)。
步骤1:取10g废渣样品,粉碎后与锌粉混合,加入H2SO4共热,生成AsH3气体。
步骤2:将AsH3气体通入AgNO3溶液中,生成银镜和As2O3。
步骤3:取1g废渣样品,重复上述实验,未见银镜生成。
(4)AsH3的电子式为_______________.
(5)步骤2的离子方程式为______________________________________________。
(6)固体废弃物的排放标准中,砷元素不得高于4.0×10-5g·kg-1,则该排放的废渣中砷元素的含量_______(填“符合”、“不符合”)排放标准.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求书写
(1)氨气的电子式:_________,乙炔的结构简式:___________;
(2)工业上利用乙烯催化水化法制取乙醇,化学反应方程式:________反应类型:____________
(3)苯与浓硝酸在50~60℃下发生硝化反应:________反应类型:_____________;
(4)已知键能如下:
化学键 | H—H | N—N | N—H | N≡N |
键能kJ/mol | 432 | 247 | 389 | 942 |
写出N2和H2合成NH3的热化学方程式:_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铵明矾NH4Al(SO4)2·12H2O是分析化学常用基准试剂,其制备过程如下。下列分析不正确的是

A. 过程Ⅰ反应:2NH4HCO3+Na2SO4===2NaHCO3↓+(NH4)2SO4
B. 检验溶液B中阴离子的试剂仅需BaCl2溶液
C. 若省略过程Ⅱ则铵明矾产率明显减小
D. 向铵明矾溶液中逐滴加入NaOH溶液先后观察到:刺激性气体逸出→白色沉淀生成→白色沉淀消失
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com