
����Ŀ������������������۷���Ϣ�صijɷ�֮һ�������㽶����ζ��ʵ��������������촼�Ʊ������������ķ�Ӧ��װ��ʾ��ͼ���й��������£�
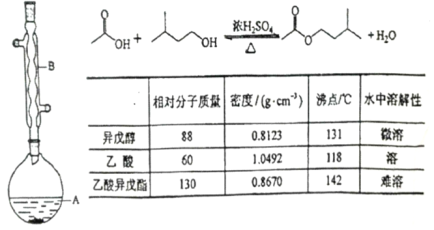
ʵ�鲽�裺
��A�м���4.4 g�����촼��6.0 g�����ᡢ����Ũ�����23Ƭ���Ƭ����ʼ��������A������50min����ӦҺ�������º����Һ©���У��ֱ�������ˮ������̼��������Һ��ˮϴ�ӣ��ֳ��IJ������������ˮMgSO4�� ���壬����Ƭ�̣����˳�ȥMgSO4���壬�����������ռ�140143����֣�������������3.9g.
�ش��������⣺
��1��װ��B�������� �������� .
��2�����Ƭ�������� .
��3����ϴ�Ӳ����У���һ��ˮϴ����ҪĿ���� ���ڶ���ˮϴ����ҪĿ���� .
��4����ϴ�ӡ���Һ�����У�Ӧ�����Ȼ���ã����ֲ��_________
A��ֱ�ӽ������������ӷ�Һ©���Ͽڵ���
B��ֱ�ӽ������������ӷ�Һ©���¿ڷų�
C���Ƚ�ˮ��ӷ�Һ©�����¿ڷų����ٽ��������������¿ڷų�
D���Ƚ�ˮ��ӷ�Һ©�����¿ڷų����ٽ��������������Ͽڵ���
��5��ʵ���м���������ˮMgSO4��Ŀ���� .
��6����ʵ��IJ����� .a��30% b��40% c��50% d��60%
���𰸡���1�������ܻ�����������������������ʹ��Ӧ�������� ����2�������У���3��ϴ��������ʹ����� ϴ��̼�����Ƶ��� ����4��d����5����������6��d��
��������
�����������1��Bװ�����������������ܻ������ܣ���������������ʹ��Ӧ�������ƿ����߷�Ӧ��������ʣ�(2)��Ϊ���ȵ���Һ�壬Ϊ��ֹ���У���Ҫ�������Ƭ���ʯ��(3) ��Ӧ��A������������������������������Ũ���������Ƭ�����Ե�һ��ˮϴ��ӦҺϴȥ���������������ڶ���ˮϴ����Һ����������̼��������Һϴȥ�ᣬ��Һ������ˮϴȥ̼���������Σ���4���÷�Һ©������Һ�壬�²�Һ����¿ڷų����ϲ�Һ����Ͽڵ������������������ܶ�С��ˮ�����ϲ㣬��ѡ��d��ȷ��(5)��ˮMgSO4�������Ǹ���������������(6)n(����)=6.0/60mol=0.1mol��n(���촼)=4.4/88mol=0.05mol�����촼���㣬�������촼���м��㣬����n(����������)=0.05mol��m(����������)=0.05��130g=6.5g�������Ϊ3.9/6.5��100%=60%����ѡ��d��ȷ��


 ��У����ϵ�д�
��У����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ǵ绯ѧԭ����Ӧ�����⡣
��1����A��B��C��D���ֽ������±�װ��ͼ����ʵ�飮
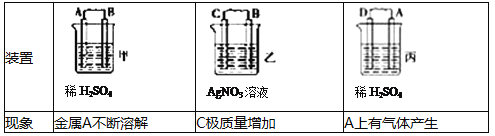
����ʵ������ش��������⣺���ֽ��������ǿ������˳������ ��
��2������ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ�á���ͼΪ���ʾ��ͼ��
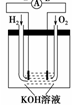
��ش�
������ȼ�ϵ�ص�����ת������Ҫ��ʽ����__________________��
�ڵ����е�����������Ϊ__________(��a��b��ʾ)��
��������ӦʽΪ____________________________��
��3����ͼ�е缫a��b�ֱ�ΪAg�缫��Pt�缫���缫c��d����ʯī�缫��ͨ��һ��ʱ�����c��d�����Ϲ��ռ���336mL����״�������壮�ش�
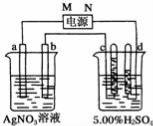
��ֱ����Դ�У�MΪ����������������
��AgNO3��Һ��Ũ�ȣ���������������С����������������ͬ����������
H2SO4��Һ��Ũ����������������
����ʱ��·��ת�Ƶ��ӵ����ʵ���Ϊ____________mol��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪1g������ȫȼ������ˮ����ʱ�ų�121kJ����������������1molO=O����ȫ����ʱ��Ҫ����496kJ��������ˮ������1mol H-O���γ�ʱ�ų�463kJ����������������1mol H-H������ʱ���յ�����Ϊ
A��920kJ B��557kJ C��436kJ D��181kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ij��������ɫ����Һ�����ܺ������������е������֣�
Na����NH4����Cl����Mg2����Ba2����CO32����SO42������ȡ���ݸ�100mL��Һ��������ʵ�飺
����һ�ݼ�������AgNO3��Һ�г���������������ϡ�������������ܽ⣻
���ڶ��ݼ�����NaOH��Һ��ּ��Ⱥ��ռ�������0.896L(��״��)��
�������ݼ�����BaCl2��Һ���˺��ָ���õ�����6.27g���پ�����ϡ����ϴ�ӡ��������������Ϊ2.33g����������ʵ��������й����ݣ��ش��������⣺
��1��ԭ��Һ��һ�����ڵ��������� ��һ�������ڵ������� �����ܴ��ڵ������� ��
��2�����з�����ѧ��Ӧ�����ӷ���ʽΪ ��
��3���������ɿ�����ϡ����ij�����ѧʽΪ �����ʵ���Ϊ mol,�ó�������ϡ��������ӷ���ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ȿ����������������ϩ���ֿ�������ȥ�����л��е���ϩ�ķ�����
A��ͨ��������ˮ��
B���ֱ��ڿ�����ȼ��
C��ͨ�����Ը��������Һ��
D����һ��������ͨ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���±���ʵ����Ԫ�����ڱ��IJ��ֱ߽磬�����ϱ߽粢δ��ʵ������
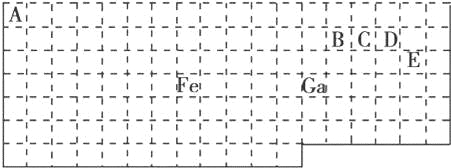
������Ϣ�ش��������⣺
��1����̬Gaԭ�ӵ����������Ų�ʽΪ
��2����Ԫ��λ��Ԫ�����ڱ��� ����Fe��CO���γ������Fe��CO��5����Fe��CO��5�����Ļ��ϼ�Ϊ ��
��3����֪��ԭ����Ŀ�ͼ۵�����������ͬ������Ϊ�ȵ����壬�ȵ�����������ƵĽṹ��������CO��Ϊ�ȵ�����ķ��Ӻ����ӷֱ�Ϊ �� ���ѧʽ����
��4����CH4��CO��CH3OH�У�̼ԭ�Ӳ�ȡsp3�ӻ��ķ����� ��
��5������VSEPRģ��Ԥ��ED4���Ŀռ乹��Ϊ ��B��C��D��Eԭ��������γɵķ����У�����ԭ�Ӷ����������8�����ȶ��ṹ�ķ���Ϊ ��д2�֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪ij���������к���NaCl���ʣ�Ϊ�ⶨ�����д��������������������ͼ�е�װ�ý���ʵ�飺
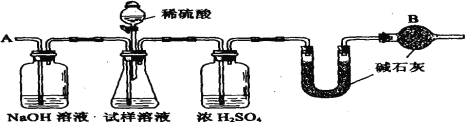
��Ҫ�������£�
����ͼ��װ�����������װ�õ�������
����a g����������ƿ�У�����������ˮ�ܽ⣬�õ�������Һ
������ʢ�м�ʯ�ҵ�U�ιܵ��������õ�b g
���ӷ�Һ©������6mol��1-1�����ᣬֱ�����ٲ�������ʱΪֹ
���ӵ���A����������һ�����Ŀ���
���ٴγ���ʢ�м�ʯ�ҵ�U�ܵ��������õ�c g
�� �ظ������������IJ���һֱ��U�ܵ������������䣬Ϊd g
����պͻش����⣺
��1������������ƽ������Ʒʱ�������ƽ��ָ������ƫת��˵��
��2��װ���и����B��������
��3���������Һ©���е����ỻ��Ũ����ͬ�����ᣬ���ԵĽ�� ����ƫ�ߡ�ƫ�ͻ䣩
��4����������Ŀ����
��5����������Ŀ����
��6���������д�������������ļ���ʽΪ
��7��������������ʵ�鷽���ⶨ�����д�������������������һ�ֲ�ͬ��ʵ�鷽��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵķ����ᴿ����ѡ����ȷ����
A | ��ȥ�Ȼ�����Һ�е���ɳ | ���� |
B | �����Ȼ�̼��ȡ��ˮ�е��� | ��ȡ |
C | �������ᣨ�е� 118�� ���������������е� 77�� �� | ��Һ |
D | �Ӻ��������Ȼ��Ƶ��������Һ����ȡ����� | �ᾧ |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Կ��淴Ӧ4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)��������������ȷ���ǣ� ��
4NO(g)+6H2O(g)��������������ȷ���ǣ� ��
A���ﵽ��ѧƽ��ʱ4v����O2��=5v�棨NO��
B������λʱ��������x mol NO��ͬʱ������x mol NH3����Ӧ��ƽ��״̬
C���ﵽ��ѧƽ��ʱ���������¶ȣ�������Ӧ���ʼ�С���淴Ӧ��������
D��ƽ�������и����ʵ���Ũ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com