
����Ŀ����ƻ�����㽶��ˮ���Ĺ����д�����������������ij��ѧ������ȤС�����������������Ϊԭ�Ϻϳ�������������ʵ�鲽�����£�
��һ���������������Ʊ�
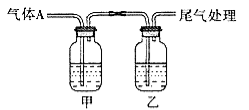
����50mL Բ����ƿ�У�����0.15mol�������� 0.12mol �����ᣬ�ټ���3��4��Ũ���ᣬҡ�ȣ�Ͷ��1��2����ʯ������ͼ��ʾ��װ����ˮ���Ļ�����Ӧװ�ã� ���ڷ�ˮ����Ԥ�ȼ���ˮ��ʹˮ���Ե��ڷ�ˮ����֧�ܿڡ�
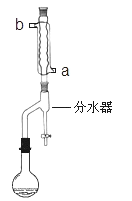
�ڴ�����ˮ��Բ����ƿ��ʯ��������С����ȡ��ڷ�Ӧ�����У�ͨ����ˮ���²����������Ϸֳ����ɵ�ˮ��ע�Ᵽ�ַ�ˮ����ˮ��Һ��ԭ���ĸ߶ȣ�ʹ�Ͳ㾡���ص�Բ����ƿ�С���Ӧ�ﵽ�յ��ֹͣ���ȣ���¼�ֳ���ˮ�������
��������Ʒ�ľ���
�۽���ˮ���ֳ�������ͷ�ӦҺһ�����Һ©���У��� 10 mL ��ˮϴ�ӡ��л��������10 mL10% Na2CO3 ϴ�������ԣ����� 10 mL ��ˮϴ�ӣ�����л���ת������ƿ�У�������ˮ����þ���
�ܽ���������������������50 mL ��ƿ�У���ѹ�����ռ� 124��126 �����֣���11.6g��Ʒ��
��1����ˮӦ�ô�������_____���� a �� b���ܿ�ͨ�롣
��2��������в��ϴӷ�ˮ���²��ֳ����ɵ�ˮ��Ŀ����_____��
��3�����й��ڷ�Һ©����ʹ��������ȷ����_____��
a����Һ©��ʹ��ǰ����Ҫ��©��ֻҪ��Һ©��������о����©ˮ����ʹ��
b����Һʱ����������Ӧ���Ͽڵ���
c����ȡ����Ӧ��ͼ��ʾ![]()
d���ų�Һ��ʱ���轫��������ʹ���ϵİ��۶�©�����ϵ�С��
��4����ʵ������У�������������������Է������� 116���IJ�����_____��
���𰸡�a ʹ�÷�ˮ�������ˮ��ʹƽ�������ƶ�����߷�Ӧ���� bd 83.3%
��������
�÷�Ӧ�����������������Ʊ�����������������Բ����ƿʹ���߷�Ӧ�������������������Լ��������������ӷ������Լ�װ����������ʹ��Ӧ���������������������߷�Ӧ���������ͬʱ������Բ����ƿ���ռ������֮����в�Ʒ�ľ��ƣ�������Ҫ������δ��Ӧ�������������ᣬ��һ�μ�ˮϴȥ���������ټ�̼���ƿ���ϴȥ��������������������ټ�ˮϴȥ̼���ƣ�֮���Һ����ˮ����þ����������������һ���������õ�������������������
(1)Ϊ����ǿ����Ч����ˮ��Ҫ����������ˮ��a��b����
(2)������ӦΪ���淴Ӧ�������������������ƽ�������ƶ�����߲��ʣ�
(3)a�������벣�������������Ƿ�©ˮ����a����
b���������������ܶȱ�ˮС��Ӧ���ϲ㣬���Դ��Ͽڵ�������b��ȷ��
c�� Ӧʹ��Һ©���ڳ��£�ʹ��Һ©���������ϣ����ڷ������ͷ�Һ©������ѹ����c����
d���ų�Һ��ʱ���轫��������ʹ���ϵİ��۶�©�����ϵ�С�ף�ƽ���Һ©������ѹ������Һ������d��ȷ��
��������ѡbd��
(4)�Ʊ������������ķ�Ӧ����ʽΪ��CH3COOH+CH3CH2CH2CH2OH![]() CH3COOCH2CH2CH2CH3+H2O�����ݷ�Ӧ����ʽ��֪��0.15mol�������� 0.12mol �����ᷴӦ����Ӧ����0.12mol CH3COOCH2CH2CH2CH3��������������Ϊ0.12mol��116g/mol=13.92g�����Բ���Ϊ
CH3COOCH2CH2CH2CH3+H2O�����ݷ�Ӧ����ʽ��֪��0.15mol�������� 0.12mol �����ᷴӦ����Ӧ����0.12mol CH3COOCH2CH2CH2CH3��������������Ϊ0.12mol��116g/mol=13.92g�����Բ���Ϊ![]() =83.3%��
=83.3%��


 ��������ܸ�ϰϵ�д�
��������ܸ�ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ҵ�ϳ���ͭ������(��Ҫ�ɷ���Cu2Te����Ag��Au������)Ϊԭ����ȡ�ڲ����ս������乤���������£�
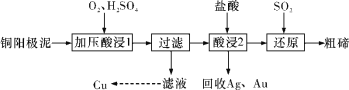
��֪��TeO2���������������ˮ�������ڽ�Ũ��ǿ���ǿ�����˵����������
A.����ѹ���1�������н���Ԫ��ת����TeO2��Ӧ�ϸ������Һ��pHֵ
B.�����2���������¶Ȳ��ܹ��ߣ������ʹ�ڵĽ����ʽ���
C.��Ag��Au�з����Au��Ӧ������յ�Ag��Au�м���ϡ��ˮ
D.����ԭ����Ӧ�з��������ӷ���ʽΪ��TeO2+2SO2+2H2O=Te+2SO42-+4H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25��ʱ��H2CO3��Ka1=4.2��10-7��Ka2=5.0��10-11����������20mL0.1mol/LNa2CO3��Һ����μ���40mL0.1mol/L'HCl��Һ����Һ�к�̼Ԫ�صĸ�����(CO2���ݳ�δ����)���ʵ�������(����)����ҺpH�仯�IJ��������ͼ��ʾ��
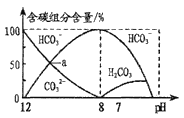
����˵����ȷ����
A. ��ͬһ��Һ�У�H2CO3��HCO3-��CO32-�ܴ�������
B. a��ʱ:c(Na+)+c(H+)=c(OH-)+3c(CO32-)
C. ��pH=7ʱ����Һ��c(Na+)=c(HCO3-)+2c(CO32-)
D. ����Һ��c(HCO3-):c(CO32-)=2:1ʱ����Һ��pH=10
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪���ױ��Ľṹ�� 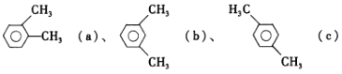 ������˵����ȷ����
������˵����ȷ����
A.a��ͬ���칹��ֻ��b��c����
B.�����ֶ��ױ��У�b��һ�ȴ����������
C.a��b��c ����ʹ���� KMnO4��Һ����ˮ������ѧ��Ӧ����ɫ
D.a��b��c ��ֻ��c ������ԭ�Ӵ���ͬһƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1��2һ���ȱ��飨CH2ClCHClCH3����һ����Ҫ�Ļ���ԭ�ϣ���ҵ�Ͽ��ñ�ϩ�ӳɷ��Ʊ�����Ҫ������Ϊ3һ�ȱ�ϩ��CH2=CHCH2Cl������Ӧԭ��Ϊ��
i .CH2 =CHCH3��g�� +C12��g��CH2ClCHClCH3��g�� ��H1=-134kJmol-1
ii . CH2 =CHCH3��g�� +C12��g��CH2= CHCH2Cl��g�� +HCl��g�� ��H2 =-102kJmol-1
��ش��������⣺
��1����֪��CH2 =CHCH2Cl ��g�� + HCl �� g��CH2ClCHClCH3��g��������Ӧ�Ļ��Ea������Ϊ132 kJmol-1�����淴Ӧ�Ļ��Ea���棩Ϊ__________ kJmol-1 ��
��2��ij�о�С�����ܱ������г���һ������C12��g����CH2 =CHCH3 �� g�����ֱ��� A��B���ֲ�ͬ���������·�����Ӧ��һ��ʱ�����CH2ClCHClCH3�IJ������¶ȵĹ�ϵ��ͼ1��ʾ��
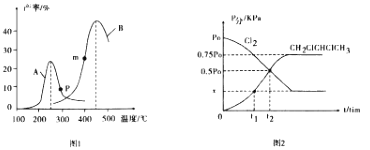
������˵����ȷ����______������ţ���
a .ʹ�ô���A��B������¶ȣ�A <B
b .p��m��ֱ��Ƕ�Ӧ�¶���CH2ClCHClCH3��ƽ�����
c. ʹ�ô��������˷�Ӧ�Ļ�ܺ��ʱ�
d. �¶Ȳ��䣬����ѹǿ��ʹCH2ClCHClCH3�IJ������
����250���Ժ�A�����в����½���ԭ�������________��д����������
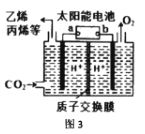
��3��T��ʱʹ��ѡ���Ը��ߵĴ������ں����ܱ������ڳ�������ʵ�����C12 �� g�� ��CH2=CHCH3 ��g�����з�Ӧi�������������ֵķ�ѹǿ��p��=p���������������ʱ��ı仯��ϵ��ͼ2��ʾ���ش��������⣺
�����õ�λʱ���������ѹ�ı仯����ʾ��Ӧ���ʣ�����= ![]() ����t1~t2ʱ�����ƽ����Ӧ��������CH2=CHCH3��= _______ kPamin-1���������ĸ��ʾ����ƽ��ʱCH2ClCHClCH3���������________��
����t1~t2ʱ�����ƽ����Ӧ��������CH2=CHCH3��= _______ kPamin-1���������ĸ��ʾ����ƽ��ʱCH2ClCHClCH3���������________��
�ڷ�Ӧ��ƽ�ⳣ��KP=_____________����ƽ���ѹ����ƽ��Ũ�ȣ������ĸ��ʾ�������
��4����ͼ3�������Ե������Һ�У��ö��Ե缫��CO2ת��Ϊ��̼ϩ���ĵ绯ѧװ�ã��ش��������⣺
��̫���ܵ�صĸ����� __________������a������b������
�����ɱ�ϩ�ĵ缫��Ӧʽ��____________��
����ͬʱ���ڣ���ͬ�����£����ĵ�CO2�����ɵ�O2 �����֮��Ϊ_________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ�� X��Y��Z��W ԭ��������������Y �� W ͬ�塣X��Y��Z ����ԭ�������������Ĺ�ϵ Ϊ X+Z=Y����� Z �� W �γɵĻ������ˮ��Һ������ W Ԫ�ص����嵥�ʣ�������ͬ���ռ���Һ�� �ã��ɵõ������� ZWX ����Һ������˵����ȷ����
A.W ���⻯���ȶ���ǿ�� Y ���⻯��
B.Z����������Ԫ�طֱ��γɵĻ�������ֻ�������Ӽ�
C.Z �� Y �γɵĻ������ˮ��Һ�ʼ���
D.��Ӧ�ļ����Ӱ뾶��СΪ W >Z > X>Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ PAA�� ![]() �����и���ˮ�ԣ���״ PAA �ڿ�ѹ�ԡ���ˮ�Եȷ����������� PAA����״ PAA ���Ʊ������ǣ�����ϩ���� NaOH �кͣ��������������� a���������ۺϡ��䲿�ֽṹƬ�� ��ͼ��ʾ����˵���������
�����и���ˮ�ԣ���״ PAA �ڿ�ѹ�ԡ���ˮ�Եȷ����������� PAA����״ PAA ���Ʊ������ǣ�����ϩ���� NaOH �кͣ��������������� a���������ۺϡ��䲿�ֽṹƬ�� ��ͼ��ʾ����˵���������
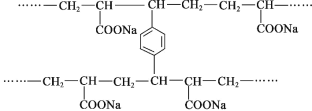
A.���� PAA �ĵ��岻����˳���칹����
B.�γ���״�ṹ�Ĺ��̷����˼Ӿ۷�Ӧ
C.������ a �Ľṹ��ʽ��![]()
D.PAA �ĸ���ˮ������COONa �й�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ˮ���к��е� CaSO4�������� Na2CO3 ��Һ������ʹ֮ת��Ϊ���ɡ���������� CaCO3��ij��ѧ�� ȤС����ijŨ�ȵ� Na2CO3 ��Һ����һ������ CaSO4 ���壬������� Na2CO3 ��Һ�������Һ��-lgc(CO32-) �Ĺ�ϵ��ͼ��ʾ����֪Ksp(CaSO4)=9��10��6��Ksp(CaCO3)=3��10��9��lg3=0.5������˵������ȷ����
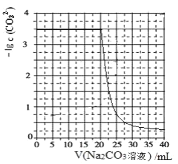
A.�����ϸ������Һ�����ϵʽ��c(Ca2��)��c(SO42��)=Ksp(CaSO4)
B.CaSO4(s)��CO32��(aq) ![]() CaCO3(s)��SO42��(aq) K=3��103
CaCO3(s)��SO42��(aq) K=3��103
C.��Na2CO3��Һ��Ũ��Ϊ1.5mol��L��1
D.��ͬ�����£�����Na2CO3��Һ��Ũ�ȸ�ΪԭŨ�ȵ�2��������ͼ������������ƽ��1����λ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾװ�ý���ʵ�飬�й�����ͽ��;���ȷ����
ѡ�� | ����A | �����Լ� | �����Լ� | ���� | ���� |
A | CO2 | Na2SiO3��Һ | BaCl2 | ���ǡ��ҳ��� | ������HCl��H2CO3��H2SiO3 |
B | Cl2 | ��ɫʯ�� | Fe��SCN��3 | ��ʼ����� | Cl2����ˮ������ |
C | SO2 | Ʒ����Һ | KMnO4 | ����ɫ | SO2����Ư���� |
D | NH3 | AgNO3��Һ | AlCl3 | ������ͬ | NH3��H2O�����OH- |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com