
【题目】下表是A、B、C、D、E 五种有机物的有关信息:
A | ①能使溴的四氯化碳溶液褪色;②空间充填模型 |
B | ① 由 C、H 两种元素组成;②空间充填模型为 |
C | ① 由 C、H、O 三种元素组成;②能与 Na 反应,但不能与 NaOH 溶液反应;③ 能与 E 反应生成酯 |
D | ① 相对分子质量比 C 少 2;②能由 C 氧化而成 |
E | ① 由 C、H、O 三种元素组成;②球棍模型为 |
回答下列问题:
(1)A 在一定条件下发生聚合反应生成的高分子化合物的名称为_____。
(2)A 与氢气发生加成反应后生成 F,与 F 在分子组成和结构上相似的有机物有很多,它们均符合通式CnH2n+2(n为正整数)。当 n=_____时,这类有机物开始出现同分异构体。
(3)B 具有的性质是_____(填序号)。
①无色无味液体 ②密度比水的大 ③难溶于水 ④有毒 ⑤与酸性KMnO4溶液和溴水反应褪色 ⑥在一定条件下可与氢气反应
(4)在铁作用下,B 与液溴反应的化学方程式为_____。
(5)C能与E反应生成 酯 ,该反应的反应类型为_________; 其化学方程式为_______。
(6)由C氧化生成D 的化学方程式为_______。
【答案】聚乙烯 4 ①③④⑥ ![]() +Br2
+Br2![]()
![]() +HBr 酯化(取代)反应 CH3CH2OH+CH2=CHCOOH
+HBr 酯化(取代)反应 CH3CH2OH+CH2=CHCOOH![]() CH2=CHCOOCH2CH3+H2O 2CH3CH2OH+O2
CH2=CHCOOCH2CH3+H2O 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
【解析】
根据题干信息,B由C、H两种元素组成,空间充填模型为![]() ,则B为苯,E由C、H、O三种元素组成,球棍模型为
,则B为苯,E由C、H、O三种元素组成,球棍模型为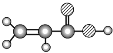 ,则E为CH2=CHCOOH,C由C、H、O 三种元素组成,能与Na反应,但不能与NaOH溶液反应,能与E反应生成酯,则C为一种醇,A能使溴的四氯化碳溶液褪色,空间充填模型
,则E为CH2=CHCOOH,C由C、H、O 三种元素组成,能与Na反应,但不能与NaOH溶液反应,能与E反应生成酯,则C为一种醇,A能使溴的四氯化碳溶液褪色,空间充填模型![]() ,能与水在一定条件下反应生成,则A为CH2=CH2,C为CH3CH2OH,D的相对分子质量比C少2,能由C氧化而成,则D为CH3CHO,据此分析解答。
,能与水在一定条件下反应生成,则A为CH2=CH2,C为CH3CH2OH,D的相对分子质量比C少2,能由C氧化而成,则D为CH3CHO,据此分析解答。
(1)根据上述分析可知,A为乙烯(CH2=CH2),在一定条件下发生聚合反应生成的高分子化合物的名称为聚乙烯;
(2)乙烯与氢气发生加成反应后生成乙烷,与乙烷在分子组成和结构上相似的有机物有很多,它们均符合通式CnH2n+2(n为正整数),当n=4时,这类有机物开始出现同分异构体;
(3)B为苯,苯是一种无色无味、密度比水小、难溶于水的有毒液体,苯不能与酸性高锰酸钾溶液和溴水反应褪色,苯在一定条件下可与氢气发生加成反应生成环己烷,故答案选①③④⑥;
(4)在Fe的作用下,苯与液溴发生取代反应生成溴苯,反应的化学方程式为![]() +Br2
+Br2![]()
![]() +HBr;
+HBr;
(5)C(CH3CH2OH)可与E(CH2=CHCOOH)发生酯化(取代)反应生成CH2=CHCOOCH2CH3,化学方程式为CH3CH2OH+CH2=CHCOOH![]() CH2=CHCOOCH2CH3+H2O;
CH2=CHCOOCH2CH3+H2O;
(6)CH3CH2OH催化氧化生成CH3CHO,反应的化学方程式为2CH3CH2OH+O2![]() 2CH3CHO+2H2O。
2CH3CHO+2H2O。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】
化合物G是治疗高血压的药物“比索洛尔”的中间体,一种合成G的路线如下:

已知以下信息:
①A的核磁共振氢谱为单峰;B的核磁共振氢谱为三组峰,峰面积比为6∶1∶1。
②D的苯环上仅有两种不同化学环境的氢;1molD可与1mol NaOH或2mol Na反应。
回答下列问题:
(1)A的结构简式为____________。
(2)B的化学名称为____________。
(3)C与D反应生成E的化学方程式为____________。
(4)由E生成F的反应类型为____________。
(5)G是分子式为____________。
(6)L是D的同分异构体,可与FeCl3溶液发生显色反应,1mol的L可与2mol的Na2CO3反应,L共有______种;其中核磁共振氢谱为四组峰,峰面积比为3∶2∶2∶1的结构简式为___________、____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是丁醇的两种同分异构体,其结构简式、沸点及熔点如下表所示:
异丁醇 | 叔丁醇 | |
结构简式 |
|
|
沸点/℃ | 108 | 82.3 |
熔点/℃ | -108 | 25.5 |
下列说法不正确的是
A. 用系统命名法给异丁醇命名为:2-甲基-1-丙醇
B. 异丁醇的核磁共振氢谱有三组峰,且面积之比是1∶2∶6
C. 用降温结晶的方法可将叔丁醇从二者的混合物中结晶出来
D. 两种醇发生消去反应后得到同一种烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】色酮类化合物K具有抗菌、降血脂等生理活性,其合成路线如下:
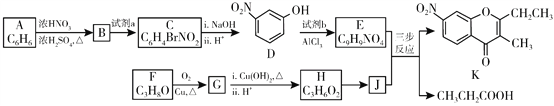
已知: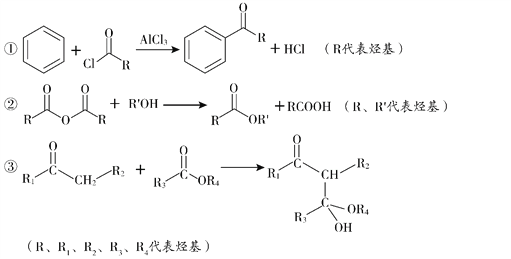
(1)A的结构简式是_________;根据系统命名法,F的名称是__________。
(2)B→C所需试剂a是__________;试剂b的结构简式是_________。
(3)C与足量的NaOH反应的化学方程式为__________。
(4)G与新制Cu(OH)2反应的化学方程式为__________。
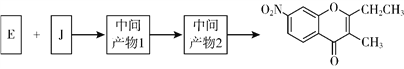
(5)已知:①2H![]() J+H2O;②J的核磁共振氢谱只有两组峰。以E和J为原料合成K分为三步反应,写出有关化合物的结构简式:________。
J+H2O;②J的核磁共振氢谱只有两组峰。以E和J为原料合成K分为三步反应,写出有关化合物的结构简式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表述正确的是
A. 苯和氯气生成C6H6Cl6的反应是取代反应
B. 乙烯与溴水发生加成反应的产物是CH2CH2Br2
C. 等物质的量的甲烷与氯气反应的产物是CH3Cl
D. 硫酸作催化剂,CH3CO18OCH2CH3水解所得乙醇分子中有18O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在抗击新冠肺炎的过程中,科研人员研究了法匹拉韦、利巴韦林、氯硝柳胺等药物的疗效,三种药物主要成分的结构简式如下。下列说法不正确的是
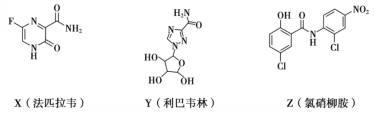
A.X的分子式为C5H4O2N3F
B.Z中含有6种官能团
C.Y和Z都有羟基,但性质不完全相同
D.X和Z都能发生加成反应和水解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备溴苯的反应装置如下图所示,关于实验操作的叙述错误的是
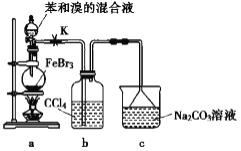
A. 向圆底烧瓶中滴加苯和溴的混合液前需先打开 K
B. 实验中装置 b 中的液体逐渐变为浅红色
C. 反应后的混合液经稀碱溶液洗涤、结晶,得到溴苯
D. 装置 c 中的碳酸钠溶液的作用是吸收溴化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水氯化锰![]() 在电子技术和精细化工领域有重要应用。一种由粗锰粉(主要杂质为Fe、Ni、Pb等金属单质)制备无水氯化锰的工艺如下(部分操作和条件略)。
在电子技术和精细化工领域有重要应用。一种由粗锰粉(主要杂质为Fe、Ni、Pb等金属单质)制备无水氯化锰的工艺如下(部分操作和条件略)。
I.向粗锰粉中加入盐酸,控制溶液的pH约为5,测定离子的初始浓度。静置一段时间后锰粉仍略有剩余,过滤;
II.向I的滤液中加入一定量盐酸,再加入![]() 溶液,充分反应后加入
溶液,充分反应后加入![]() 固体调节溶液的pH约为5,过滤;
固体调节溶液的pH约为5,过滤;
III.向II的滤液中通入![]() 气体,待充分反应后加热一段时间,冷却后过滤;
气体,待充分反应后加热一段时间,冷却后过滤;
IV.浓缩、结晶、过滤、洗涤、脱水得到无水MnCl2。
各步骤中对杂质离子的去除情况
|
|
| |
初始浓度/mg·L–1 | 21.02 | 4.95 | 5.86 |
步骤I后/ mg·L–1 | 12.85 | 3.80 | 3.39 |
步骤II后/ mg·L–1 | 0.25 | 3.76 | 3.38 |
步骤III后/ mg·L–1 | 0.10(达标) | 3.19(未达标) | 0.12(达标) |
已知:金属活动性Mn>Fe>Ni>Pb
(1)锰和盐酸反应的化学方程式是_______。
(2)步骤I中:
①Fe2+浓度降,滤渣中存在![]() 。结合离子方程式解释原因:_______。
。结合离子方程式解释原因:_______。
②Pb2+浓度降低,分析步骤I中发生的反应为:Pb + 2H+ = Pb2+ + H2↑、______。
(3)步骤II中:
①![]() 酸性溶液的作用:_______。
酸性溶液的作用:_______。
②结合离子方程式说明MnCO3的作用: _______。
(4)步骤III通入H2S后, Ni2+不达标而![]() 达标。推测溶解度:PbS_____NiS(填“>”或“<”)。
达标。推测溶解度:PbS_____NiS(填“>”或“<”)。
(5)测定无水![]() 的含量:将a g 样品溶于一定量硫酸和磷酸的混合溶液中,加入稍过量
的含量:将a g 样品溶于一定量硫酸和磷酸的混合溶液中,加入稍过量![]() ,使
,使![]() 氧化为
氧化为![]() 。待充分反应后持续加热一段时间,冷却后用b mol/L硫酸亚铁铵
。待充分反应后持续加热一段时间,冷却后用b mol/L硫酸亚铁铵![]() 滴定
滴定![]() ,消耗c mL 硫酸亚铁铵。(已知:滴定过程中发生的反应为:Fe2+ + Mn3+ = Fe3+ + Mn2+)
,消耗c mL 硫酸亚铁铵。(已知:滴定过程中发生的反应为:Fe2+ + Mn3+ = Fe3+ + Mn2+)
①样品中MnCl2的质量分数是_____(已知:MnCl2的摩尔质量是126 g·mol-1)。
②“持续加热”的目的是使过量的![]() 分解。若不加热,测定结果会______(填“偏高”、“偏低”或“无影响”)。
分解。若不加热,测定结果会______(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关下列四个常用电化学装置的叙述正确的是( )
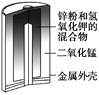
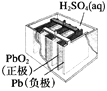
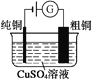
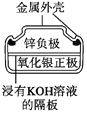
图1 碱性锌锰电池 图2 铅—硫酸蓄电池 图3 电解精炼铜 图4 银锌纽扣电池
A. 图1所示电池中,MnO2的作用是催化剂
B. 图2所示电池放电过程中,硫酸浓度不断增大
C. 图3所示装置工作过程中,电解质溶液中Cu2+浓度始终不变
D. 图4所示电池中,Ag2O是氧化剂,电池工作过程中还原为Ag
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com