
| A.NH4+:加NaOH溶液,加热,滴入酚酞溶液检验所得溶液 |
| B.CO32-:加入稀盐酸,产生无色能使澄清石灰水变浑浊的气体 |
| C.Fe3+:加入KSCN溶液,溶液呈血红色 |
| D.Cl-:加入AgNO3溶液,产生白色沉淀 |
科目:高中化学 来源:不详 题型:填空题
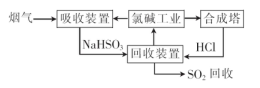
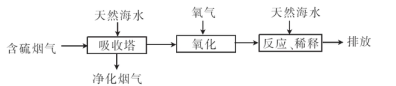
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
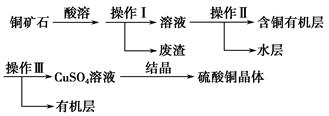
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量悬浊液,过滤,充分洗涤后,取滤渣于试管中,______________________ | ____________,说明悬浊液中混有Cu4(OH)6SO4 |
| 步骤2:另取少量悬浊液于试管中,____________________ | ____________,说明悬浊液中混有Cu(OH)2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①④②⑤③ | B.⑤④②①③ | C.②⑤④①③ | D.⑤②④①③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.加入稀盐酸产生无色气体,将气体通入澄清石灰水,溶液变浑浊,一定有CO32- |
| B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- |
| C.加入足量稀盐酸无现象,再加入氯化钡溶液,有白色沉淀产生,一定有SO42- |
| D.加入碳酸钠溶液产生白色沉淀,再加盐酸沉淀消失,一定有Ba2+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
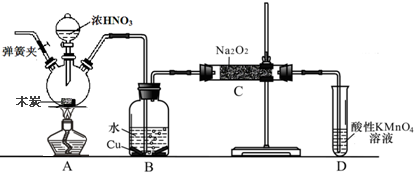
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
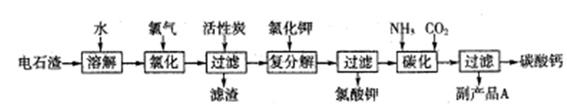

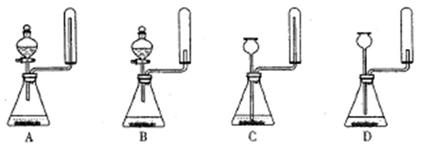
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
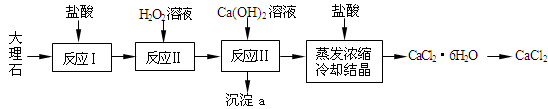
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加入滴加BaCl2溶液,立即产生白色沉淀。 | 原溶液中一定有SO42- |
| B | 在K2CrO7溶液中加入NaOH溶液,溶液由橙色变为黄色。 | K2CrO7与NaOH溶液发生了氧化还原反应 |
| C | 在滴有酚酞的Na2CO3溶液中,滴加入BaC12溶液,溶液红色逐渐褪去。 | Na2CO3溶液中存在水解平衡 |
| D | 用铂丝蘸取溶液进行颜色反应,观察到火焰呈黄色。 | 该溶液一定是钠盐溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com