
把4mol A和2.5mol B混合于2L密闭容器中,发生反应:3A(g)+2B(s) 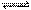 xC(g)+D(g) 5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.05mol•L-1•min-1 ,下列结论错误的是( )
xC(g)+D(g) 5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.05mol•L-1•min-1 ,下列结论错误的是( )
A.A的平均反应速率为0.15 mol•L-1•min-1 B.平衡时,C的浓度为0.25mol•L-1
C.B的平均反应速率为0.1 mol•L-1•min-1 D.平衡时,容器内压强为原来的0.875倍
【考点】本题考查化学反应速率的计算、平衡浓度的计算,压强与物质的量之间的关系等知识点。
【解析】2L密闭容器中,4mol A和2.5mol B发生反应:3A(g)+2B(s) 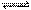 xC(g)+D(g),
xC(g)+D(g),
反应时间为5分钟达到平衡,容器内压强变小,说明反应是气体总体积减小的反应,注意B为固体,则X=1,D的平均反应速率为0.05mol•L-1•min-1 ,根据反应速率之比等于方程式系数比,A的平均反应速率为0.15 mol•L-1•min-1 A选项正确;X=1平衡时,C的浓度为0.05mol•L-1•min-1×5=0.25mol•L-1B正确;B物质为固体,不用固体表示反应速率,C错误;平衡时,容器内压强之比等于物质的量之比,反应前为6.5mol,反应后为6.5-0.5=6mol,容器内压强为原来的0.875倍,D正确。
【答案】C


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:
下列关于氯气的说法中不正确的是
A.尽管氯气的化学性质很活泼,但是干燥的液氯能用钢瓶贮存
B.氯气和液氯是两种不同的物质
C.可以用浓硫酸除去氯气中的水蒸气
D.氯气有毒,它曾在战争中被用于制造毒气弹
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组利用图一装置制取氨气并探究氨气的有关性质。

(1)装置A中烧瓶内试剂可选用________(填序号)。
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱
(2)若探究氨气的溶解性,需在K2的导管末端连接图二装置中的________装置(填序号),当装置D中集满氨气后,关闭K1、K2,打开K3,引发喷泉的实验操作是____________________________________________。
(3)若探究氨气的还原性,需打开K1、K3,K2处导管连接制取纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气,生成气体必须通过盛有____________________试剂的洗气瓶;
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为_____________________________________________________________;
③从K3处导管逸出的气体中含有少量Cl2,则C装置中应盛放________溶液(填化学式),反应的离子方程式为_____________________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅰ.如图,在光照条件下,将盛有CH4和Cl2的量筒倒扣于盛有饱和食盐水的水槽中进行实验,对实验现象及产物分析中错误的是( )
 A.混合气体的颜色变浅,量筒中液面上升
A.混合气体的颜色变浅,量筒中液面上升
B.量筒内壁上出现的油状液滴,应是三氯甲烷、四氯甲烷的混合物
C.水槽中有白色固体物质析出
D.甲烷与氯气反应后的产物只有CCl4
Ⅱ.根据烯烃的性质回答下列问题。
(1)一瓶无色气体,可能含有CH4和CH2===CH2或其中的一种,与一瓶Cl2混合后光照,观察到黄绿色逐渐褪去,瓶壁有少量无色油状小液滴。
①由上述实验现象推断出该瓶气体中一定含有CH4,你认为是否正确,为什么?_________________________________ _______________________________________
_______________________________________
________________________________________________________________________。
②上述实验可能涉及的反应类型有___________________________________。
(2)含有 的化合物与CH2===CH2一样,在一定条件下可聚合成高分子化合物。
的化合物与CH2===CH2一样,在一定条件下可聚合成高分子化合物。
①广泛用作农用薄膜的聚氯乙烯塑料,是由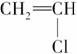 聚合而成的,其化学方程式是________________________________________________________________________
聚合而成的,其化学方程式是________________________________________________________________________
________________________________________________________________________。
②电器包装中大量使用的泡沫塑料的主要成分是聚苯乙烯(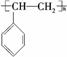 ),它是由________________(写结构简式)聚合而成的。
),它是由________________(写结构简式)聚合而成的。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关热化学方程式的评价合理的是( )
| 实验事实 | 热化学方程式 | 评价 | |
| A | 已知H+(aq)+OH-(aq)===H2O(l) △H=-57.3 kJ·mol-1,将稀硫酸与稀氢氧化钡溶液混合 | H2SO4(aq)+Ba(OH)2(aq) ===BaSO4(s)+ 2H2O(l) △H=-114.6 kJ·mol-1 | 正确 |
| B | 醋酸与稀氢氧化钠溶液混合 | CH3COOH(aq)+NaOH(aq) ===NaCl(aq)+H2O(l) △H=-57.3kJ·mol-1 | 不正确;因为醋酸状态为“aq”,而不是“l”。 |
| C | 160 g SO3气体与适量水恰好完全反应生成H2SO4,放出热量260.6 kJ | SO3(g)+H2O(l)===H2SO4(aq) △H=-130.3 kJ·mol-1 | 不正确;因为反应热为△H=-260.6kJ·mol-1 |
| D | 已知25℃、101 kPa下,120g石墨完全燃烧放出热量3935.1 kJ | C(s)+O2(g)===CO2(g) △H=-393.51 kJ·mol-1 | 不正确;同素异形体要注名称:C(石墨) |
查看答案和解析>>
科目:高中化学 来源: 题型:
某温度下,在一容积不变的密闭容器中,反应A(g) + 2B (g) 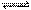 3C(g)达平衡时,A、B、C的物质的 量分别为3 mol,2 mol和4 mol,若温度不变,向容器内的平衡混合物中再加入A、C各1mol,此时该平衡移动的方向是( )
3C(g)达平衡时,A、B、C的物质的 量分别为3 mol,2 mol和4 mol,若温度不变,向容器内的平衡混合物中再加入A、C各1mol,此时该平衡移动的方向是( )
A.向左移动 B.向右移动 C.不移动 D.无法判断
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学研究性学习小组学习了化学反应与能量的内容后,对
CaCO3与稀盐酸的反应进行了相关探究。他们在室温条件下,将CaCO3
块状固体放入1L、1mol•L-1稀盐酸中,记录下了随反应时间的变化生成
CO2气体的物质的量情况,绘制成如图曲线。假设溶液的体积变化忽略
不计,请分析以下问题:
(1)若想加快该反应的速率,可以采取的措施是 、
(答两种)。
(2)0~2min内,用HCl浓度变化表示的平均反应速率为 ,比较0~2min、2~4min、4~6min三个时间段,反应速率最大的是 。
(3)根据定量的数据,定性的描述0~6min内该反应的化学反应速率的变化情况
呈现这种变化的原因是 。
(4)根据图像中曲线的变化趋势,第8min时,该反应的反应速率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:
X2(g)+3Y2(g) 2XY3(g) △H=-92.6kJ·mol-1
2XY3(g) △H=-92.6kJ·mol-1
起始时各物质物质的量如下表所示:
| 容器 编号 | 起始时各物质物质的量/mol | ||
| X2 | Y2 | XY3 | |
| ① | 1 | 3 | 0 |
| ② | 0.6 | 1.8 | 0.8 |
达到平衡后,①容器中XY3的物质的量为0.5mol。下列叙述正确的是
A.容器①、②中反应的平衡常数不相等
B.达平衡时,容器②中 XY3的物质的量浓度为2mol·L—1
C.容器①中反应达到平衡时放出的热量为23.15 kJ
D.容器②中反应达到平衡时放出热量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com