
在一定温度下,在10L密闭容器中加入5molSO2和一定量的氧气,在一定条件下发生反应: 2SO2(g)+O2(g) 2SO3(g)。达平衡时容器中SO3的物质的量浓度为0.4mol/L,还剩余氧气3.0mol。
2SO3(g)。达平衡时容器中SO3的物质的量浓度为0.4mol/L,还剩余氧气3.0mol。
(1)氧气的起始浓度为 。
(2)平衡时剩余SO2 mol;
(3)该条件下SO2的最大转化率为 ;
(4)平衡时体系中SO3的百分含量(体积分数)为 ;
(5)平衡体系中SO2、O2和SO3的物质的量之比为 。
(5分)(1)0.5mol/L;(2)1; (3)80%;(4)50%;(5)1:3:4
【解析】
试题分析:
2SO2(g)+O2(g) 2SO3(g)
2SO3(g)
起始浓度(mol/L) 0.5 x 0
转化浓度(mol/L) 0.4 0.2 0.4
平衡浓度(mol/L) 0.1 0.3 0.4
所以氧气的起始浓度为0.2mol/L+0.3mol/L=0.5mol/L
平衡时剩余SO2的物质的量是0.1mol/L×10L=1mol
该条件下SO2的最大转化率为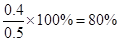
平衡时体系中SO3的百分含量(体积分数)为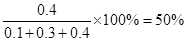
平衡体系中SO2、O2和SO3的物质的量之比为0.1:0.3:0.4=1:3:4
考点:考查可逆反应的有关计算
点评:在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某深刻的量,然后依据已知条件列式计算即可。


 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案科目:高中化学 来源: 题型:
| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(O2)/mol | 0.20 | 0.16 | 0.13 | 0.11 | 0.10 | 0.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| T/s | 0 | 500 | 1000 |
| c(N2O5)/mol?L-1 | 5.00 | 3.50 | 2.42 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:
碘钨灯具有使用寿命长、节能环保等优点.一定温度下,在碘钨灯灯泡内封存的少量碘与沉积在灯泡壁上的钨可以发生如下的可逆反应:查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| 加热 |
| t/min | CH4(mol?L-1) | H2O(mol?L-1) | CO(mol?L-1) | H2(mol?L-1) |
| 0 | 0.2 | 0.3 | 0 | 0 |
| 2 | n1 | n2 | n3 | 0.3 |
| 3 | n1 | n2 | n3 | 0.3 |
| 4 | 0.09 | 0.19 | x | 0.33 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应达平衡时N2的转化率为10% | B、该反应达到平衡时,N2的平衡浓度为0.45 mol?L-1 | C、该反应达到平衡时的压强是起始压强的0.95 倍 | D、反应进行到10 s末时,消耗 H2的平均反应速率是 0.03 mol?(L?s)-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com